1 . 硫代硫酸钠( Na2S2O3)俗称海波,广泛应用于照相定影及纺织业等领域。某实验小组制备硫代硫酸钠并探究其性质。
Ⅰ.硫代硫酸钠的制备
实验小组设计如下装置制备硫代硫酸钠

信息:Na2S2O3,中S元素的化合价分别为-2和+6
(1)仪器a的名称是___________ 。B中发生的化学反应方程式为___________ (该反应理论上钠元素的利用率为100%)。
Ⅱ.产品纯度的测定
①溶液配制:准确称取该硫代硫酸钠样品8. 000 g,配制成50. 00 mL溶液。
②滴定:向锥形瓶中加入20. 00 mL 0.10 mol·L-1KIO3溶液,加入过量KI溶液和H2SO4溶液,然后加入淀粉作指示剂,用硫代硫酸钠样品溶液滴定碘单质,发生反应: I2+2 =2I-+
=2I-+ 
(2)生成碘单质的离子方程式为___________ 。滴定终点现象为___________ , 消耗样品溶液25. 00 mL,则样品纯度为___________ %。
Ⅲ.硫代硫酸钠性质的探究
①取Na2S2O3晶体,溶解,配成0. 20 mol·L-1溶液。
②取4mL溶液,向其中加入1.0mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑浊物为S。
实验小组研究S产生的原因,提出了以下假设:
假设1:氧化剂氧化:Cl2、HClO等含氯的氧化性微粒氧化了-2价硫元素。
假设2:___________ ( 不考虑空气中氧气氧化)。

设计实验方案:
(3)假设2是___________ 。
(4)第②组实验中胶头滴管加入的试剂是___________ 。
(5)依据现象,S产生的主要原因是___________ 。
(6)结合Ⅱ、Ⅲ分析纯度较低的原因是___________ 。
Ⅰ.硫代硫酸钠的制备
实验小组设计如下装置制备硫代硫酸钠

信息:Na2S2O3,中S元素的化合价分别为-2和+6
(1)仪器a的名称是
Ⅱ.产品纯度的测定
①溶液配制:准确称取该硫代硫酸钠样品8. 000 g,配制成50. 00 mL溶液。
②滴定:向锥形瓶中加入20. 00 mL 0.10 mol·L-1KIO3溶液,加入过量KI溶液和H2SO4溶液,然后加入淀粉作指示剂,用硫代硫酸钠样品溶液滴定碘单质,发生反应: I2+2
 =2I-+
=2I-+ 
(2)生成碘单质的离子方程式为
Ⅲ.硫代硫酸钠性质的探究
①取Na2S2O3晶体,溶解,配成0. 20 mol·L-1溶液。
②取4mL溶液,向其中加入1.0mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑浊物为S。
实验小组研究S产生的原因,提出了以下假设:
假设1:氧化剂氧化:Cl2、HClO等含氯的氧化性微粒氧化了-2价硫元素。
假设2:___________ ( 不考虑空气中氧气氧化)。

设计实验方案:
| 胶头滴管 | 现象 | |
| 第①组 | 1.0 mL饱和氯水 | 立即出现浑浊 |
| 第②组 | ___________ | 一段时间后出现浑浊,且浑浊度比①组小 |
(4)第②组实验中胶头滴管加入的试剂是
(5)依据现象,S产生的主要原因是
(6)结合Ⅱ、Ⅲ分析纯度较低的原因是
您最近一年使用:0次
名校
2 . 某研究小组设计如图所示实验装置(夹持装置已略去)分别探究NO与铜粉、Na2O2的反应。
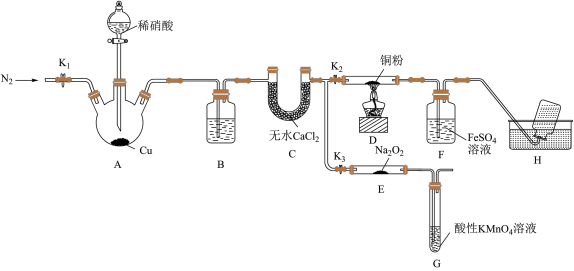
已知:①NO与Na2O2可发生反应2NO+Na2O2 =2NaNO2。
②NO、NO 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是________ 。
(2)装置B中盛放的试剂为水,其作用是________ 。
(3)装置F中的实验现象为______ 。装置H中收集的气体为N2和_______ (填化学式)。
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是________ 。
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有NO2和_____ (填化学式)。
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO 可将MnO
可将MnO 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①判断滴定终点的方法________ 。
②样品中NaNO2的质量分数为___________ (用含有a、b的代数式表示)。
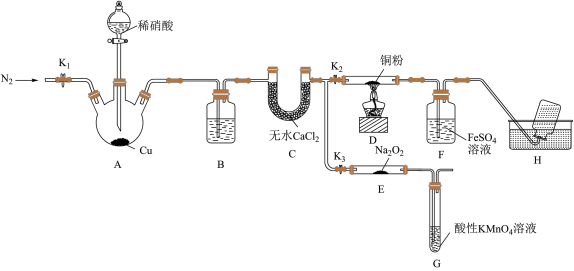
已知:①NO与Na2O2可发生反应2NO+Na2O2 =2NaNO2。
②NO、NO
 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO
 Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是
(2)装置B中盛放的试剂为水,其作用是
(3)装置F中的实验现象为
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有NO2和
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO
 可将MnO
可将MnO 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。①判断滴定终点的方法
②样品中NaNO2的质量分数为
您最近一年使用:0次
2020-11-04更新
|
690次组卷
|
5卷引用:新疆克拉玛依克拉玛依市独山子第二中学2021-2022学年高三上学期12月月考化学试题
2011·新疆乌鲁木齐·三模
解题方法
3 . (Ⅰ)某化学兴趣小组的同学得上用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
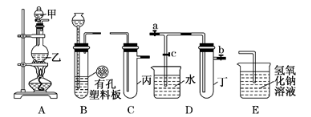
(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱。
①选择合理的装置连接:___________ →____________ →__________ (填字母编号)。
②选择所需的试剂:__________ (填字母编号)。
a.固体氯化钠 b.固体二氧化锰 c.浓硫酸
d.浓盐酸 e.稀盐酸 f.溴化钠溶液
③实验现象及结论:_________ 。
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4·7H2O晶体,设计实验流程如下: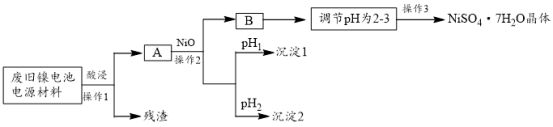
已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
回答下列问题:
(1)根据上表数据判断操作2依次析出的沉淀1是_______ 沉淀2是________ (填化学式),pH1___________ pH2(填“>”、“<”或“=”);
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为___________ 。
(3)“调节pH为2-3”的目的是_______ ;
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料—NiOOH。该反应的离子方程式是______________ 。

(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱。
①选择合理的装置连接:
②选择所需的试剂:
a.固体氯化钠 b.固体二氧化锰 c.浓硫酸
d.浓盐酸 e.稀盐酸 f.溴化钠溶液
③实验现象及结论:
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4·7H2O晶体,设计实验流程如下:

已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
回答下列问题:
(1)根据上表数据判断操作2依次析出的沉淀1是
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为
(3)“调节pH为2-3”的目的是
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料—NiOOH。该反应的离子方程式是
您最近一年使用:0次
名校
解题方法
4 . 用下列装置进行相应的实验,不能达到实验目的的是


| A.用图甲装置验证NH3易溶于水 |
| B.用图乙装置提纯I2 |
| C.用图丙装置测定KMnO4溶液物质的量浓度(锥形瓶中Na2C2O4质量已知) |
| D.用图丁装置检验该条件下铁发生了析氢腐蚀 |
您最近一年使用:0次
2020-06-09更新
|
768次组卷
|
4卷引用:新疆维吾尔自治区2021届高三下学期诊断性自测(第一次)化学试题
新疆维吾尔自治区2021届高三下学期诊断性自测(第一次)化学试题江苏省七市(南通、泰州、扬州、徐州、淮安、连云港、宿迁)2020届高三第三次调研考试(6月) 化学 试题山东师范大学附属中学2020届普通高等学校招生全国统一考试化学试题(模拟一)(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-测试
名校
解题方法
5 . 如图装置可用于收集气体并验证其某些化学性质能达到目的的是


选项 | 气体 | 试剂 | 现象 | 结论 |
A |
| 酚酞试液 | 溶液变红色 | 氨水显碱性 |
B |
| 紫色石蕊试液 | 溶液先变红后褪色 |  有酸性和漂白性 有酸性和漂白性 |
C |
| 溴水 | 溶液褪色 |  有氧化性 有氧化性 |
D | X | KI淀粉溶液 | 溶液变蓝 | X可能是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 二氧化硫是国内外允许使用的一种食品添加剂,可用于食物的增白、防腐等,但必须严格遵守国家有关标准使用。某学习小组设计了如图1装置用于制取 并验证其性质。
并验证其性质。
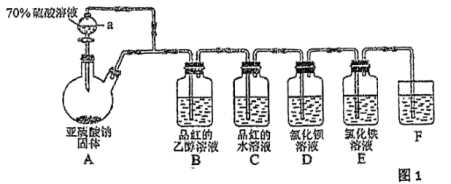
(1)仪器a的名称为___________ 。
(2)装置A中反应的化学方程式___________ 。
(3)烧杯F中的试剂可以是___________。(填序号)
(4)实验时装置E中溶液变为浅绿色,检验该离子产物的实验操作及现象是___________ 。
(5)实验时观察到装置B无明显现象,装置C红色褪去,则使品红的水溶液褪色的微粒一定不是___________ 。(填化学式)
(6)学生甲预测装置D中没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的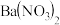 和
和 溶液,进行如图2实验:
溶液,进行如图2实验:

如图2实验中G、H、I烧杯中观察到的现象如表:
①据G中现象得出的结论是___________ 。
②H中发生反应的离子方程式___________ 。
③I中出现白色沉淀的速率比H中快很多的原因可能是___________ 。
 并验证其性质。
并验证其性质。
(1)仪器a的名称为
(2)装置A中反应的化学方程式
(3)烧杯F中的试剂可以是___________。(填序号)
A.饱和 溶液 溶液 | B.饱和 溶液 溶液 | C. 溶液 溶液 | D.饱和 溶液 溶液 |
(5)实验时观察到装置B无明显现象,装置C红色褪去,则使品红的水溶液褪色的微粒一定不是
(6)学生甲预测装置D中没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的
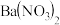 和
和 溶液,进行如图2实验:
溶液,进行如图2实验:
如图2实验中G、H、I烧杯中观察到的现象如表:
| 烧杯 | 实验现象 |
| G | 无白色沉淀产生, 传感器测得溶液 传感器测得溶液 |
| H | 有白色沉淀产生 |
| I | 有白色沉淀产生,I中出现白色沉淀比H中快很多 |
②H中发生反应的离子方程式
③I中出现白色沉淀的速率比H中快很多的原因可能是
您最近一年使用:0次
2021-08-15更新
|
253次组卷
|
2卷引用:新疆喀什第二中学2021-2022学年高三上学期11月份摸底考试化学试题
名校
解题方法
7 . (Ⅰ)分别向盛有:①紫色石蕊试液 ②澄清石灰水 ③品红溶液 ④酸性高锰酸钾溶液的试管中通入SO2气体。
(1)试管①中的实验现象为___________ 。
(2)试管②中发生反应的离子方程式为___________ (通入少量的SO2)。
(3)上述实验中,出现溶液褪色现象的是___________ (填试管标号)。
(4)上述实验中,SO2表现出酸性氧化物性质的是___________ (填试管序号,下同)。SO2表现出漂白性的是___________ ,SO2表现出还原性的是___________ 。
(Ⅱ)硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)写出通信中硅的氧化物的一种用途:___________ 。
(2)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为8Na + CCl4 + SiCl4 = SiC + 8NaCl。
①该反应中Si元素的化合价为___________ 价。
②其中还原产物的化学式为___________ 。
③高温真空环境中,C与SiO2反应也可以生成SiC,写出该反应的化学方程式:___________ 。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作___________ ;设计简单实验比较醋酸与H2SiO3酸性的强弱,画出装置图,并指明所用试剂和药品:___________ 。
(1)试管①中的实验现象为
(2)试管②中发生反应的离子方程式为
(3)上述实验中,出现溶液褪色现象的是
(4)上述实验中,SO2表现出酸性氧化物性质的是
(Ⅱ)硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)写出通信中硅的氧化物的一种用途:
(2)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为8Na + CCl4 + SiCl4 = SiC + 8NaCl。
①该反应中Si元素的化合价为
②其中还原产物的化学式为
③高温真空环境中,C与SiO2反应也可以生成SiC,写出该反应的化学方程式:
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作
您最近一年使用:0次
2021-08-03更新
|
196次组卷
|
2卷引用:新疆维吾尔自治区和田地区和田县2022-2023学年高三上学期11月期中考试化学试题
8 . 三硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子。某化学兴趣小组对Na2CS3的一些性质进行了探究性实验。
实验I.探究Na2CS3的性质:
(1)H2CS3是___ (填“强”或“弱”)酸。
(2)已知步骤③中反应的氧化产物是SO42-,则该反应的离子方程式为___ 。
(3)某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测定产生的白色沉淀的质量即可求出实验中所用的Na2CS3的质量。你是否同意他的观点并说明理由:___ 。
实验Ⅱ.测定Na2CS3溶液的浓度:
按如图所示装置进行实验:将50.0mLNa2CS3溶液置于三颈烧瓶中,打开仪器M的活塞,滴入足量2.0mol•L-1的稀H2SO4,关闭活塞。
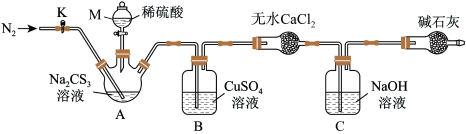
已知:CS32-+2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(4)仪器M的名称是___ 。反应开始前需要先通入一段时间N2,其作用为___ 。
(5)B中发生反应的离子方程式为___ 。
(6)反应结束后打开活塞K,再缓慢通入一段时间的热N2,其目的是___ 。
(7)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉淀质量之前需要进行的实验操作是___ 。若B中生成沉淀的质量为8.4g,则Na2CS3溶液的物质的量浓度是___ 。
实验I.探究Na2CS3的性质:
| 步骤 | 操作及现象 |
| ① | 取少量Na2CS3固体溶于蒸馏水中,配制成溶液并分成两等份 |
| ② | 向其中一份溶液中滴加几滴酚酞试剂,溶液变成红色 |
| ③ | 向另一份溶液中滴加硫酸酸化的KMnO4溶液,紫色褪去 |
(2)已知步骤③中反应的氧化产物是SO42-,则该反应的离子方程式为
(3)某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测定产生的白色沉淀的质量即可求出实验中所用的Na2CS3的质量。你是否同意他的观点并说明理由:
实验Ⅱ.测定Na2CS3溶液的浓度:
按如图所示装置进行实验:将50.0mLNa2CS3溶液置于三颈烧瓶中,打开仪器M的活塞,滴入足量2.0mol•L-1的稀H2SO4,关闭活塞。

已知:CS32-+2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(4)仪器M的名称是
(5)B中发生反应的离子方程式为
(6)反应结束后打开活塞K,再缓慢通入一段时间的热N2,其目的是
(7)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉淀质量之前需要进行的实验操作是
您最近一年使用:0次
2020-02-03更新
|
247次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2022-2023学年高三上学期11月月考化学试题
9 . 某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置:(部分夹持装置已略去)
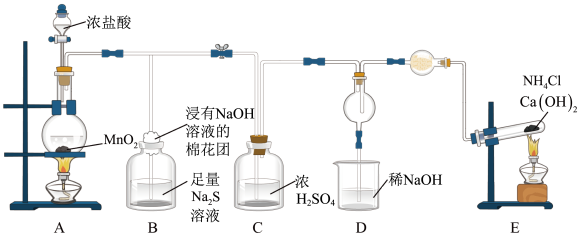
(1)写出A中反应的离子方程式___________________________ 。
(2)写出F中反应的化学方程式_________________________ 。
(3)B中浸有NaOH溶液的棉花作用___________________ ,B中溶液出现现象_______________ ,写出B中发生的离子反应_________________ 。
(4)E中干燥管装的干燥剂是________ ,检验F中气体的方法______________ 。
(5)D中干燥管中出现的现象______________ ,D中干燥管中化学方程式_________________ 。

(1)写出A中反应的离子方程式
(2)写出F中反应的化学方程式
(3)B中浸有NaOH溶液的棉花作用
(4)E中干燥管装的干燥剂是
(5)D中干燥管中出现的现象
您最近一年使用:0次
10 . 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。

请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是________ ,其中发生反应的化学方程式为_____ 。
(2)实验过程中,装置B、C中发生的现象分别是_____ 、 ____ ,这些现象分别说明SO2具有的性质是____ 和____ 。
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_________ 。
(4)尾气可采用________ 溶液吸收。(写化学式)

请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是
(2)实验过程中,装置B、C中发生的现象分别是
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
(4)尾气可采用
您最近一年使用:0次
2019-08-02更新
|
99次组卷
|
3卷引用:新疆维吾尔自治区和田地区策勒县2022-2023学年高三上学期11月期中考试化学试题
新疆维吾尔自治区和田地区策勒县2022-2023学年高三上学期11月期中考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (练)-《2020年高考一轮复习讲练测》安徽省亳州市第二中学2018-2019学年高二下学期期末考试化学试题




