1 . 下列关于溴苯制备,并验证反应类型的实验,说法正确的是
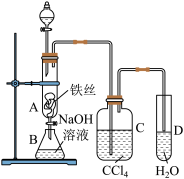
| A.分液漏斗中的试剂是苯和水的混合物 |
| B.B中NaOH用于反应后萃取产品溴苯 |
| C.CCl4中可观察到分层现象 |
| D.反应结束后还需向D中加入AgNO3溶液或石蕊 |
您最近一年使用:0次
2023-12-04更新
|
328次组卷
|
4卷引用:上海市新中高级中学2023-2024学年高二上学期期中考试化学试题
上海市新中高级中学2023-2024学年高二上学期期中考试化学试题(已下线)2.3.1 芳香烃(巩固)(已下线)2.3.2苯的同系物云南省昆明市第一中学2023-2024学年高二下学期4月月考化学试题
名校
2 . 下列实验操作、现象及得出的结论均正确的是
选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向紫色石蕊溶液中通入 | 溶液紫色逐渐变浅 |  具有漂白性 具有漂白性 |
| B | 向盛有 溶液的试管中加入KSCN溶液,再加入少量铁粉 溶液的试管中加入KSCN溶液,再加入少量铁粉 | 溶液先变红,后红色又变浅 |  与 与 反应生成的无色物质,导致溶液红色变浅 反应生成的无色物质,导致溶液红色变浅 |
| C | 在试管中加入0.5g淀粉和  溶液,加热。冷却后再加入少量银氨溶液,水浴加热片刻 溶液,加热。冷却后再加入少量银氨溶液,水浴加热片刻 | 试管内壁有银镜生成 | 淀粉发生了水解 |
| D | 将石蜡油裂解产物通入酸性 溶液中 溶液中 | 溶液紫红色褪去 | 石蜡油裂解产物中含有不饱和烃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-26更新
|
46次组卷
|
2卷引用:辽宁省部分学校2023-2024学年高二上学期10月月考化学试卷
名校
解题方法
3 . 实验小组探究 溶液与
溶液与 溶液的反应及其速率,实验操作和现象如下。
溶液的反应及其速率,实验操作和现象如下。
已知:i. 能完全电离,且具有强氧化性,
能完全电离,且具有强氧化性, 易被还原为
易被还原为 ;
;
ⅱ.淀粉检测 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝:
即可快速变蓝:
ii. 可与
可与 发生反应:
发生反应: 。
。
(1)实验1-1的目的是_______ 。
(2) 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
为了研究 与
与 反应的速率,小组同学分别向两支试管中加入下列试剂,并记录变色时间,如下表。
反应的速率,小组同学分别向两支试管中加入下列试剂,并记录变色时间,如下表。
(3)加入 溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:
溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:
猜想1: 先与
先与 反应,使
反应,使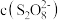 降低;
降低;
猜想2: 先与
先与 反应,_______。
反应,_______。
请回答:
①甲同学提出猜想1的依据:由信息i推测, 的还原性
的还原性_______ (填“强于”或“弱于”) 的。
的。
②乙同学根据实验2-2中数据认为,假定 与
与 反应,溶液中剩余
反应,溶液中剩余 的浓度
的浓度_______ (填“大于”或“小于”)实验2-1中 的起始浓度,由此证明猜想1不成立。
的起始浓度,由此证明猜想1不成立。
③补全 猜想2:_______ 。
(4)查阅文献表明猜想2成立。
①实验2-2中,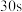 内未检测到
内未检测到 与
与 反应,从反应机理角度分析可能的原因是
反应,从反应机理角度分析可能的原因是_______ 。
②根据实验2-2的数据,计算30s内的平均反应速率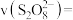
_______  (写出计算式)。
(写出计算式)。
 溶液与
溶液与 溶液的反应及其速率,实验操作和现象如下。
溶液的反应及其速率,实验操作和现象如下。已知:i.
 能完全电离,且具有强氧化性,
能完全电离,且具有强氧化性, 易被还原为
易被还原为 ;
;ⅱ.淀粉检测
 的灵敏度很高,遇低浓度的
的灵敏度很高,遇低浓度的 即可快速变蓝:
即可快速变蓝:ii.
 可与
可与 发生反应:
发生反应: 。
。| 编号 | 1-1 | 1-2 |
| 实验操作 |  |  |
| 现象 | 无明显现象 | 溶液立即变蓝 |
(1)实验1-1的目的是
(2)
 与
与 反应的离子方程式为
反应的离子方程式为为了研究
 与
与 反应的速率,小组同学分别向两支试管中加入下列试剂,并记录变色时间,如下表。
反应的速率,小组同学分别向两支试管中加入下列试剂,并记录变色时间,如下表。| 编号 |   溶液 溶液 |   溶液 溶液 | 蒸馏水 | 淀粉溶液/滴 |   溶液 溶液 | 变色时间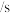 |
| 2-1 | 2 | 0 | 2.8 | 2 | 0.2 | 立即 |
| 2-2 | 2 | 0.8 | 0.2 | 2 | 2 | 30 |
(3)加入
 溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:
溶液后溶液变蓝的时间明显增长,甲同学对此提出猜想:猜想1:
 先与
先与 反应,使
反应,使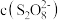 降低;
降低;猜想2:
 先与
先与 反应,_______。
反应,_______。请回答:
①甲同学提出猜想1的依据:由信息i推测,
 的还原性
的还原性 的。
的。②乙同学根据实验2-2中数据认为,假定
 与
与 反应,溶液中剩余
反应,溶液中剩余 的浓度
的浓度 的起始浓度,由此证明猜想1不成立。
的起始浓度,由此证明猜想1不成立。③
(4)查阅文献表明猜想2成立。
①实验2-2中,
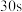 内未检测到
内未检测到 与
与 反应,从反应机理角度分析可能的原因是
反应,从反应机理角度分析可能的原因是②根据实验2-2的数据,计算30s内的平均反应速率
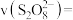
 (写出计算式)。
(写出计算式)。
您最近一年使用:0次
解题方法
4 . 下列各组实验中,化学反应速率最快的是
| 选项 | 反应物 | 催化剂 | 温度 |
| A | 5 mL 10%  溶液 溶液 | 无 | 20℃ |
| B | 5 mL 10%  溶液 溶液 | 无 | 30℃ |
| C | 5 mL 10%  溶液 溶液 |  粉末 粉末 | 20℃ |
| D | 5 mL 10%  溶液 溶液 |  粉末 粉末 | 30℃ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-02更新
|
180次组卷
|
2卷引用:新疆乌鲁木齐市六校联考2023-2024学年高二上学期期末考试化学试题
5 . 高中化学学科核心素养要求进行科学探究。现对二氧化硫的性质进行深入探究。
I.实验、类比、推理是化学学习的重要方法。某课外活动小组根据 与
与 的反应,用如图所示装置探究
的反应,用如图所示装置探究 与
与 的反应,并探究其产物成分。(已知:
的反应,并探究其产物成分。(已知: 与水蒸气在加热时会发生反应)
与水蒸气在加热时会发生反应)
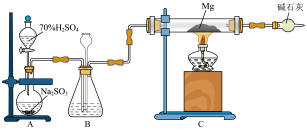
(1)装置B的作用之一是观察 的生成速率,为保证实验的严谨性其中的液体最好选择
的生成速率,为保证实验的严谨性其中的液体最好选择___________ (填序号)
a.饱和 溶液 b.饱和
溶液 b.饱和 溶液
溶液
c.饱和 溶液 d.浓硫酸
溶液 d.浓硫酸
(2)依据 与
与 的反应,三位同学对
的反应,三位同学对 与
与 反应的产物提出不同假设,并将装置
反应的产物提出不同假设,并将装置 中玻璃管内固体产物加入如下图所示的装置
中玻璃管内固体产物加入如下图所示的装置 中大试管,进一步设计实验探究
中大试管,进一步设计实验探究 与
与 反应的产物,若固体产物只有两种,依据充分反应后的现象,完成下列表格:
反应的产物,若固体产物只有两种,依据充分反应后的现象,完成下列表格:

为进一步验证假设③中 的存在,可将
的存在,可将 中试剂换成
中试剂换成___________ 。(填试剂的化学式)
II.某兴趣小组欲探究 与
与 的反应。
的反应。
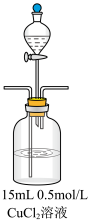
(3)甲为了确认现象II中白色沉淀的成分,进行如下探究。查阅资料:
并进行如下实验:
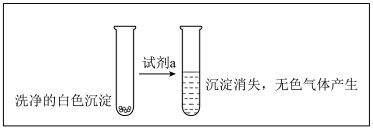
①试剂 是
是___________ 。
②现象II中生成白色沉淀的离子方程式是___________ 。
(4)乙认为实验存在干扰,欲探究纯净的 悬浊液与
悬浊液与 的反应。
的反应。
①乙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,___________ (填操作和现象),证明已洗涤干净。再进行如下实验:
②乙预测产物是 ,取砖红色沉淀,洗涤后,
,取砖红色沉淀,洗涤后,___________ (填操作和现象),证明产物是 。
。
(5)纯净的 悬浊液与
悬浊液与 发生反应的化学方程式是
发生反应的化学方程式是___________ 。
I.实验、类比、推理是化学学习的重要方法。某课外活动小组根据
 与
与 的反应,用如图所示装置探究
的反应,用如图所示装置探究 与
与 的反应,并探究其产物成分。(已知:
的反应,并探究其产物成分。(已知: 与水蒸气在加热时会发生反应)
与水蒸气在加热时会发生反应)
(1)装置B的作用之一是观察
 的生成速率,为保证实验的严谨性其中的液体最好选择
的生成速率,为保证实验的严谨性其中的液体最好选择a.饱和
 溶液 b.饱和
溶液 b.饱和 溶液
溶液c.饱和
 溶液 d.浓硫酸
溶液 d.浓硫酸(2)依据
 与
与 的反应,三位同学对
的反应,三位同学对 与
与 反应的产物提出不同假设,并将装置
反应的产物提出不同假设,并将装置 中玻璃管内固体产物加入如下图所示的装置
中玻璃管内固体产物加入如下图所示的装置 中大试管,进一步设计实验探究
中大试管,进一步设计实验探究 与
与 反应的产物,若固体产物只有两种,依据充分反应后的现象,完成下列表格:
反应的产物,若固体产物只有两种,依据充分反应后的现象,完成下列表格:
| 假设 |  中现象 中现象 |  中现象 中现象 |
① | 固体不完全溶解,无气泡产生 | 溶液不褪色 |
② | 固体不完全溶解,且有气泡产生 | 溶液褪色 |
③ 和 和 | 固体完全溶解,且有气泡产生 |
 的存在,可将
的存在,可将 中试剂换成
中试剂换成II.某兴趣小组欲探究
 与
与 的反应。
的反应。
| 实验步骤 | 现象 |
步骤1:打开分液漏斗,向烧瓶中加入 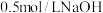 溶液 溶液 | I.有蓝色絮状沉淀,静置后分层。 |
步骤2:从左侧导管通入 气体 气体 | II.静置后分层,底部有白色沉淀 |
| 物质 | 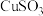 |  |  |
| 溶解性 | 不溶于水,浅黄色沉淀 | 不溶于水,白色沉淀 | 不溶于水,砖红色沉淀 |
| 性质 | 与酸反应 | 能溶于浓盐酸 | 酸性体系中不稳定,进一步反应生成Cu和 |

①试剂
 是
是②现象II中生成白色沉淀的离子方程式是
(4)乙认为实验存在干扰,欲探究纯净的
 悬浊液与
悬浊液与 的反应。
的反应。①乙过滤I中的蓝色沉淀,洗涤,取最后一次洗涤液于试管中,
| 实验 | 实验步骤 | 现象 |
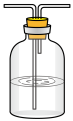 纯净的  悬浊液 悬浊液 | 从左侧导管通入 气体 气体 | III.静置后分层,上层溶液为蓝色,底部有砖红色沉淀 |
 ,取砖红色沉淀,洗涤后,
,取砖红色沉淀,洗涤后, 。
。(5)纯净的
 悬浊液与
悬浊液与 发生反应的化学方程式是
发生反应的化学方程式是
您最近一年使用:0次
2023-08-19更新
|
111次组卷
|
2卷引用:江西省宜春市丰城拖船中学2023-2024学年高二上学期开学化学试题
6 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
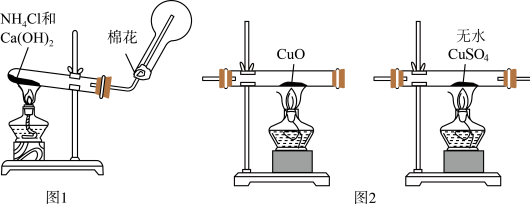
Ⅰ.实验室制取氨气
(1)图1装置中生成NH3的化学方程式为_______ ,棉花的作用是_______ ;
Ⅱ.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(2)无水硫酸铜的作用是_______ ;
(3)该实验缺少尾气吸收装置,如图中能用来吸收尾气的装置是_______ (填字母)。

(4)实验中观察到a中 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为_______ ,证明氨气具有_______ (填“氧化”或“还原”)性;氨与氧气在加热、催化剂作用下的反应也体现了这一性质,该反应的化学方程式为_______ 。

Ⅰ.实验室制取氨气
(1)图1装置中生成NH3的化学方程式为
Ⅱ.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(2)无水硫酸铜的作用是
(3)该实验缺少尾气吸收装置,如图中能用来吸收尾气的装置是

(4)实验中观察到a中
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
您最近一年使用:0次
2023-08-10更新
|
103次组卷
|
2卷引用:四川省双流棠湖中学2023-2024学年高二上学期9月月考化学试题
名校
解题方法
7 . 回答下列问题:
Ⅰ.某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
资料:单质硫可溶于过量硫化钠溶液形成淡黄色的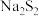 溶液。
溶液。
(1)根据实验可知, 具有
具有___________ 性。
(2)甲同学预测实验Ⅰ中 被氧化成
被氧化成 。
。
①根据实验现象,乙同学认为甲的预测不合理,理由是___________ 。
②乙同学取实验Ⅰ中少量溶液进行实验,检测到有 ,得出
,得出 被氧化成
被氧化成 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是___________ 。
③同学们经讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。
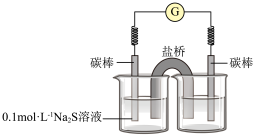
右侧烧杯中的溶液是___________ ;连通后电流计指针偏转,一段时间后,取左侧烧杯中的溶液,用盐酸酸化后,滴加 溶液,观察到有白色沉淀生成,证明
溶液,观察到有白色沉淀生成,证明 氧化成了
氧化成了 。
。
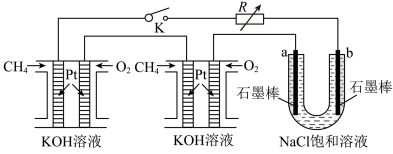
Ⅱ.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

通入a物质的电极是原电池的___________ (填“正”或“负”)极,其电极反应式为___________ 。
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验:如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为___________ (法拉第常数 ),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为___________ (假设反应后溶液体积不变)。
Ⅰ.某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | Ⅰ | Ⅱ |
| 实验过程 | 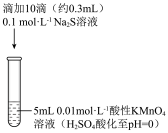 |  |
| 实验 现象 | 紫色变浅(pH>1),生成棕褐色沉淀( ) ) | 溶液呈淡黄色(pH≈8),生成浅粉色沉淀( ) ) |
 溶液。
溶液。(1)根据实验可知,
 具有
具有(2)甲同学预测实验Ⅰ中
 被氧化成
被氧化成 。
。①根据实验现象,乙同学认为甲的预测不合理,理由是
②乙同学取实验Ⅰ中少量溶液进行实验,检测到有
 ,得出
,得出 被氧化成
被氧化成 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是③同学们经讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。
右侧烧杯中的溶液是
 溶液,观察到有白色沉淀生成,证明
溶液,观察到有白色沉淀生成,证明 氧化成了
氧化成了 。
。Ⅱ.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

通入a物质的电极是原电池的
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验:如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为
 ),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
您最近一年使用:0次
8 . 探究甲醛与新制Cu(OH)2的反应:①向6mL6mol/LNaOH溶液中滴加8滴2%CuSO4溶液,振荡,加入0.5mL15%甲醛溶液,混合均匀,水浴加热,迅速产生红色沉淀,产生无色气体;②反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解;③相同条件下,甲酸钠溶液与新制Cu(OH)2共热,未观察到明显现象:已知: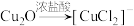 ,甲醛是具有强还原性的气体,下列说法正确的是
,甲醛是具有强还原性的气体,下列说法正确的是
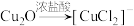 ,甲醛是具有强还原性的气体,下列说法正确的是
,甲醛是具有强还原性的气体,下列说法正确的是| A.红色沉淀的主要成分不是Cu2O,可能是Cu |
| B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO |
C.从甲醛的结构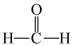 推测,其氧化产物可能为碳酸( 推测,其氧化产物可能为碳酸(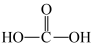 ) ) |
| D.实验中会得到大量含有CO2的无色气体 |
您最近一年使用:0次
9 . 置换反应
(1)乙醇与金属钠反应的实验探究:
实验1:向小烧杯中加入无水乙醇,再放入一小块金属钠。
实验现象:金属钠___________ 烧杯底部,金属钠表面有___________ 产生,并逐渐消失。
实验结论:乙醇与钠反应生成___________ ,并放出___________ 。
实验2:向两支试管中分别加入3mL水和3mL乙醚(CH3-O-CH3),再分别加入一小块金属钠。实验现象:①金属钠加入水中,金属钠浮在水面上,___________ 反应,金属钠___________ ,有___________ 产生;
②金属钠加入乙醚中,金属钠___________ 试管底部,无明显现象。
实验结论:金属钠与水___________ 反应,与乙醚___________ 反应。
(2)乙醇与金属钠的反应:
①化学方程式:反应方程式为___________ 。
②金属钠与水和乙醇反应,与乙醚不反应,说明金属钠能与水的氢原子和乙醇___________ 上的氢原子发生置换反应,不能与___________ 上的氢原子反应。
③金属钠与水反应比与乙醇反应剧烈得多,说明水中的氢原子比乙醇___________ 的氢原子活泼。
(1)乙醇与金属钠反应的实验探究:
实验1:向小烧杯中加入无水乙醇,再放入一小块金属钠。
实验现象:金属钠
实验结论:乙醇与钠反应生成
实验2:向两支试管中分别加入3mL水和3mL乙醚(CH3-O-CH3),再分别加入一小块金属钠。实验现象:①金属钠加入水中,金属钠浮在水面上,
②金属钠加入乙醚中,金属钠
实验结论:金属钠与水
(2)乙醇与金属钠的反应:
①化学方程式:反应方程式为
②金属钠与水和乙醇反应,与乙醚不反应,说明金属钠能与水的氢原子和乙醇
③金属钠与水反应比与乙醇反应剧烈得多,说明水中的氢原子比乙醇
您最近一年使用:0次
名校
10 . 向乙醛溶液中加入含 的物质的量为1
的物质的量为1 的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。
的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。
为探究哪一种猜想正确,某研究性学习小组设计了如下2种实验方案。
方案1:检验褪色后溶液的酸碱性。方案2:测定反应后溶液中的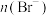 。
。
下列说法正确的是
 的物质的量为1
的物质的量为1 的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。
的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。为探究哪一种猜想正确,某研究性学习小组设计了如下2种实验方案。
方案1:检验褪色后溶液的酸碱性。方案2:测定反应后溶液中的
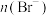 。
。下列说法正确的是
| A.若检验褪色后的溶液显酸性,说明溴水将乙醛氧化成乙酸 |
B.若测得反应后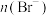 为0 为0 ,说明溴水与乙醛发生加成反应 ,说明溴水与乙醛发生加成反应 |
C.若测得反应后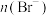 为2 为2 ,说明溴水与乙醛发生取代反应 ,说明溴水与乙醛发生取代反应 |
D.若溴水能将乙醛氧化为乙酸,反应的离子方程式为: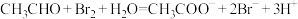 |
您最近一年使用:0次
2023-07-18更新
|
345次组卷
|
4卷引用:山西省名校联合测评2022-2023学年高二下学期7月期末化学试题



