1 . 某化学兴趣小组欲制备氨气并探究其相关性质。请回答下列问题:
(1)如图是制取少量氨气的实验装置:
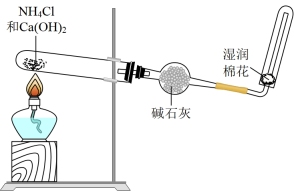
①在制取氨气的实验装置中,使用湿润棉花(棉花团外侧滴有少量蒸馏水)的作用是____ (填一条)。
②干燥管中的碱石灰____ (填“能”或“不能”)用无水CaCl2、P2O5代替。
(2)如图为探究氨气的还原性实验装置:
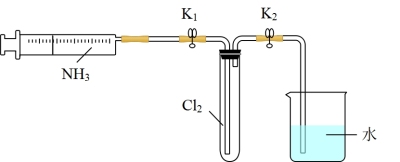
①试管中气体的颜色为____ 。
②打开K1,室温下将过量的氨气推入试管中,可能出现的现象为____ ,反应的化学方程式为____ 。
③检验试管中固体是否含有氮元素一定用不到的试纸或试剂是____ (填字母)。
a.蒸馏水 b.NaOH溶液 c.红色石蕊试纸 d.蓝色石蕊试纸 e.稀硫酸
(3)如图为探究NH3和HCl的有关性质的实验装置:
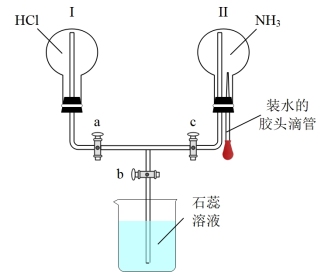
①得到蓝色喷泉的原因是____ 。
②该装置中产生“红蓝双色喷泉”现象的操作方法是____ 。
(1)如图是制取少量氨气的实验装置:

①在制取氨气的实验装置中,使用湿润棉花(棉花团外侧滴有少量蒸馏水)的作用是
②干燥管中的碱石灰
(2)如图为探究氨气的还原性实验装置:

①试管中气体的颜色为
②打开K1,室温下将过量的氨气推入试管中,可能出现的现象为
③检验试管中固体是否含有氮元素一定用不到的试纸或试剂是
a.蒸馏水 b.NaOH溶液 c.红色石蕊试纸 d.蓝色石蕊试纸 e.稀硫酸
(3)如图为探究NH3和HCl的有关性质的实验装置:

①得到蓝色喷泉的原因是
②该装置中产生“红蓝双色喷泉”现象的操作方法是
您最近一年使用:0次
名校
2 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制得Cl2,进而制备少量KClO3和NaClO。
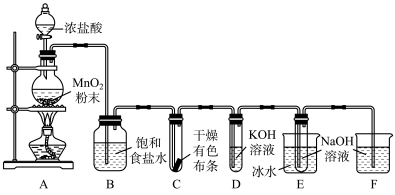
已知:Cl2与KOH溶液在70~80℃时反应生成KClO3,而在温度较低时会反应生成KClO。
回答下列问题:
(1)装置A中盛放浓盐酸的仪器名称是____ 。
(2)A中制备Cl2的化学方程式为____ ,该反应中氧化剂与还原剂的物质的量之比为____ 。
(3)Cl2还可以用高锰酸钾与浓盐酸反应得到:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。用双线桥法 表示该反应电子转移的方向和数目:____ 。
(4)B中饱和食盐水的作用是___ 。C中的实验现象是____ 。
(5)D需要进行加热,采用适宜的加热方式是___ 。
(6)E中反应的化学方程式为___ 。
(7)F的作用是____ 。
(8)若A装置后连接如图所示装置,当反应结束关闭分液漏斗活塞后,关闭止水夹K,该装置的作用是____ 。


已知:Cl2与KOH溶液在70~80℃时反应生成KClO3,而在温度较低时会反应生成KClO。
回答下列问题:
(1)装置A中盛放浓盐酸的仪器名称是
(2)A中制备Cl2的化学方程式为
(3)Cl2还可以用高锰酸钾与浓盐酸反应得到:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。用
(4)B中饱和食盐水的作用是
(5)D需要进行加热,采用适宜的加热方式是
(6)E中反应的化学方程式为
(7)F的作用是
(8)若A装置后连接如图所示装置,当反应结束关闭分液漏斗活塞后,关闭止水夹K,该装置的作用是

您最近一年使用:0次
21-22高一·全国·课时练习
解题方法
3 . 设计实验证明二氧化碳溶于水生成的酸性物质不稳定___ 。
您最近一年使用:0次
名校
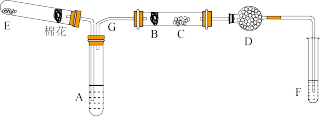
4 . 下图所示为某化学兴趣小组设计的乙醇氧化的实验装置并验证其产物(图中加热仪器、铁架台、铁夹等均未画出)。
(1)E处是一种纯净物,其发生反应的化学方程式为_____ 。
(2)为使A中乙醇平稳汽化成乙醇蒸气,常采用的方法是____ 。D处使用碱石灰的作用是_____ 。
(3)能证明乙醇反应后产物的实验现象是____ 。写出F处对应现象的化学方程式_____ 。
(4)本实验中若不加热E处,其他操作不变,则发现C处无明显变化,而F处现象与(3)相同。推断B处发生反应的化学方程式____ 。
(1)E处是一种纯净物,其发生反应的化学方程式为
(2)为使A中乙醇平稳汽化成乙醇蒸气,常采用的方法是
(3)能证明乙醇反应后产物的实验现象是
(4)本实验中若不加热E处,其他操作不变,则发现C处无明显变化,而F处现象与(3)相同。推断B处发生反应的化学方程式
您最近一年使用:0次
2021-04-29更新
|
558次组卷
|
7卷引用:湖南省邵阳邵东市第一中学2020-2021学年高二下学期期中考试化学试题
名校
解题方法
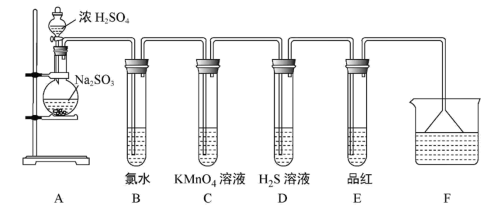
5 . 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是___ 、___ 。
(2)反应后,装置B中发生的现象是___ ,反应的离子方程式为___ ,装置C中的现象是___ ,表现了SO2的___ ;装置D中现象是__ ,发生反应的化学方程式为___ 。
(3)漏斗的作用是___ 。
(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)

请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是
(2)反应后,装置B中发生的现象是
(3)漏斗的作用是
您最近一年使用:0次
2021-04-08更新
|
733次组卷
|
3卷引用:山西省太原市五十六中2020-2021学年高一下学期第一次月考化学试题
6 . 某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:蒸馏烧瓶内有白雾,烧杯中出现白色沉淀。请回答:
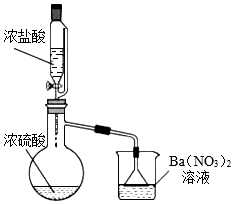
(1)将浓硫酸和浓盐酸混合可产生HCl气体的原因是___ 。
(2)烧杯中出现白色沉淀的原因是__ 。

(1)将浓硫酸和浓盐酸混合可产生HCl气体的原因是
(2)烧杯中出现白色沉淀的原因是
您最近一年使用:0次
2021-03-11更新
|
485次组卷
|
8卷引用:【浙江新东方】高中化学20210304-020
(已下线)【浙江新东方】高中化学20210304-020(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记(已下线)第11讲 硫及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 硫及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)第四章 非金属及其化合物 第21讲 硫酸 含硫物质的转化(已下线)题型51 浓硫酸的性质(已下线)第4讲 浓硫酸 不同价态含硫物质的转化
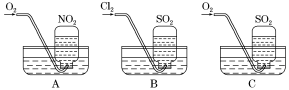
7 . 为了探究三种气态氧化物(SO2、NO2、CO2)的性质,某同学设计了一组实验:用三只集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量O2或Cl2,如图A、B、C所示。一段时间后,A、B装置的集气瓶中充满溶液,C装置的集气瓶中还有气体剩余。
(假设瓶内液体不扩散):
①写出装置B中反应的离子方程式:___________ 。
②假设该实验条件下,气体摩尔体积为a L·mol-1。则装置A的集气瓶中所得溶液溶质的物质的量浓度为___________ 。
③通入氧气前在C装置的水槽里滴加几滴紫色石蕊溶液,观察到的现象是___________ ,通入氧气后,可能观察到的实验现象是___________ ,写出反应的总化学方程式:___________ 。

(假设瓶内液体不扩散):
①写出装置B中反应的离子方程式:
②假设该实验条件下,气体摩尔体积为a L·mol-1。则装置A的集气瓶中所得溶液溶质的物质的量浓度为
③通入氧气前在C装置的水槽里滴加几滴紫色石蕊溶液,观察到的现象是
您最近一年使用:0次
名校
解题方法
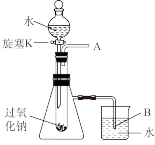
8 . 用脱脂棉包住约0.2g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加少量水,结果脱脂棉剧烈燃烧。
(1)由脱脂棉剧烈燃烧可得出过氧化钠与水反应的结论是:
a._____________________ ;b.____________________ 。
(2)写出过氧化钠与水反应的化学方程式:_________________________ 。
(3)某研究性学习小组,拟用如图所示的装置进行实验,以证明上述2个结论。实验的操作方法___________ 。
(1)由脱脂棉剧烈燃烧可得出过氧化钠与水反应的结论是:
a.
(2)写出过氧化钠与水反应的化学方程式:
(3)某研究性学习小组,拟用如图所示的装置进行实验,以证明上述2个结论。实验的操作方法

您最近一年使用:0次
19-20高一·浙江·阶段练习
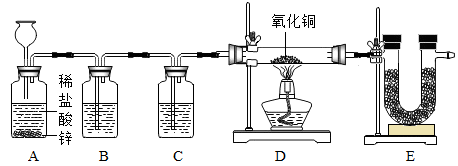
9 . 实验室用如图所示装置制取纯净、干燥的氢气,并进行还原氧化铜的实验(发生装置生成的氢气可能含有氯化氢和水)。
回答下列问题:
(1)装置B、C内所盛的液体分别是浓硫酸和氢氧化钠中的一种,则装置C中溶液的作用是______ 。
(2)为检验氢气还原氧化铜有水生成,装置E中所盛试剂是__________ 。
(3)为证实生成的气体中混有氯化氢气体,装置B应该盛________ 溶液。
(4)氢气还原氧化铜的主要操作步骤有:①加热氧化铜 ②检验氢气纯度 ③停止加热 ④通入氢气 ⑤停止通入氢气。正确的操作顺序(序号)是_____________ 。

回答下列问题:
(1)装置B、C内所盛的液体分别是浓硫酸和氢氧化钠中的一种,则装置C中溶液的作用是
(2)为检验氢气还原氧化铜有水生成,装置E中所盛试剂是
(3)为证实生成的气体中混有氯化氢气体,装置B应该盛
(4)氢气还原氧化铜的主要操作步骤有:①加热氧化铜 ②检验氢气纯度 ③停止加热 ④通入氢气 ⑤停止通入氢气。正确的操作顺序(序号)是
您最近一年使用:0次
解题方法
10 . 回答下列问题。_________ 。
(2)用如图所示装置进行实验。打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是_______ (填字母)。
A.钠块始终保持在a处,直至完全消失
B.钠块始终保持在c处,直到完全消失
C.钠块在煤油和水的交界处上下浮动
D.随着反应的进行,U形管中煤油的液面下降,漏斗中液面上升
E.最终钠块在煤油中燃烧起来
(3)装置中漏斗在反应过程中的主要作用是____________ 。

(2)用如图所示装置进行实验。打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是
A.钠块始终保持在a处,直至完全消失
B.钠块始终保持在c处,直到完全消失
C.钠块在煤油和水的交界处上下浮动
D.随着反应的进行,U形管中煤油的液面下降,漏斗中液面上升
E.最终钠块在煤油中燃烧起来
(3)装置中漏斗在反应过程中的主要作用是
您最近一年使用:0次



