1 . 草酸(H2C2O4)是一种还原性的二元弱酸(常温下,草酸的电离常数K1=5.4x10-2,K2=5.4x10-5 ),主要存在于菠菜等植物中。
(1)常温下,用0.1000mol·L-1 NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,图中c点所示溶液中: 2c( )+2c(
)+2c( )+2c(H2C2O4)=c(Na+)
)+2c(H2C2O4)=c(Na+)

则a点所示溶液中各离子的浓度由大到小的顺序为___________ 。
(2) 中碳元素的化合价是+3价,推测其有还原性。为了验证
中碳元素的化合价是+3价,推测其有还原性。为了验证 与Fe2+ 的还原性强弱,某小组同学进行了如下实验:向10mL 0.5mol•L-1 FeCl3溶液中缓慢加入0.5mol•L-1 K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
与Fe2+ 的还原性强弱,某小组同学进行了如下实验:向10mL 0.5mol•L-1 FeCl3溶液中缓慢加入0.5mol•L-1 K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
资料:三水三草酸合铁酸钾[K3Fe(C2O4)3•3H2O]为翠绿色晶体,Fe3++3 =[Fe(C2O4)3]3- K=1.6×1020
=[Fe(C2O4)3]3- K=1.6×1020
①该小组同学学并未检出反应后的溶液中有Fe2+,从反应原理的角度解释 和Fe3+ 未发生氧化还原反应的可能的原因是
和Fe3+ 未发生氧化还原反应的可能的原因是___________ 。
② 经进一步研究分析,同学们改进了实验方案。设计了如图所示的装置,验证了 的还原性强于Fe2+。
的还原性强于Fe2+。

i.闭合K,电流计指针偏转,一段时间后,取少许左侧溶液,滴加_______ 溶液(填化学式),生成蓝色沉淀,证明左池有Fe2+生成。
ii.写出右池电极反应式:___________ 。
iii.该装置的优点是___________ 。
(1)常温下,用0.1000mol·L-1 NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,图中c点所示溶液中: 2c(
 )+2c(
)+2c( )+2c(H2C2O4)=c(Na+)
)+2c(H2C2O4)=c(Na+)
则a点所示溶液中各离子的浓度由大到小的顺序为
(2)
 中碳元素的化合价是+3价,推测其有还原性。为了验证
中碳元素的化合价是+3价,推测其有还原性。为了验证 与Fe2+ 的还原性强弱,某小组同学进行了如下实验:向10mL 0.5mol•L-1 FeCl3溶液中缓慢加入0.5mol•L-1 K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。
与Fe2+ 的还原性强弱,某小组同学进行了如下实验:向10mL 0.5mol•L-1 FeCl3溶液中缓慢加入0.5mol•L-1 K2C2O4溶液至过量,充分反应后得到翠绿色溶液和翠绿色晶体。资料:三水三草酸合铁酸钾[K3Fe(C2O4)3•3H2O]为翠绿色晶体,Fe3++3
 =[Fe(C2O4)3]3- K=1.6×1020
=[Fe(C2O4)3]3- K=1.6×1020①该小组同学学并未检出反应后的溶液中有Fe2+,从反应原理的角度解释
 和Fe3+ 未发生氧化还原反应的可能的原因是
和Fe3+ 未发生氧化还原反应的可能的原因是② 经进一步研究分析,同学们改进了实验方案。设计了如图所示的装置,验证了
 的还原性强于Fe2+。
的还原性强于Fe2+。
i.闭合K,电流计指针偏转,一段时间后,取少许左侧溶液,滴加
ii.写出右池电极反应式:
iii.该装置的优点是
您最近一年使用:0次
2 . 探究氮及其化合物的性质,下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 常温下,将Fe片分别插入稀硝酸和浓硝酸中 | 一段时间后,前者有气体产生,后者无明显现象 | 稀硝酸的氧化性强于浓硝酸 |
| B | 将 样品溶于稀硫酸后,滴加KSCN溶液 样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变红 |  晶体已氧化变质 晶体已氧化变质 |
| C | 向两个同规格烧瓶中分别装入同比例的 和 和 气体,并分别浸泡于热水和冷水中 气体,并分别浸泡于热水和冷水中 | 一段时间后,两烧瓶内颜色深浅不同 | 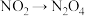 的转化存在限度 的转化存在限度 |
| D | 将盛有 固体的试管加热 固体的试管加热 | 试管底部固体消失,试管口有晶体凝结 |  固体受热易升华 固体受热易升华 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-10更新
|
1479次组卷
|
5卷引用:山西省晋中市平遥县第二中学校2023-2024学年高三上学期适应性训练四理科综合试题
山西省晋中市平遥县第二中学校2023-2024学年高三上学期适应性训练四理科综合试题浙江省温州市普通高中2024届高三上学期第一次适应性考试(一模)化学试题(已下线)热点08 表格型实验方案的设计与评价(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题03 化学实验基础(3大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
名校
解题方法
3 . 为探究氨及铵盐性质,将 晶体装入如图所示
晶体装入如图所示 形三通管两端进行微型实验(无水
形三通管两端进行微型实验(无水 可吸附
可吸附 ,形成
,形成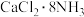 )。下列说法错误的是
)。下列说法错误的是
 晶体装入如图所示
晶体装入如图所示 形三通管两端进行微型实验(无水
形三通管两端进行微型实验(无水 可吸附
可吸附 ,形成
,形成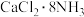 )。下列说法错误的是
)。下列说法错误的是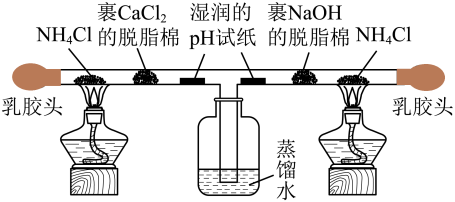
A. 晶体受热分解的化学方程式为 晶体受热分解的化学方程式为 |
B.同时点燃两个酒精灯后,两端湿润的 试纸均有颜色变化 试纸均有颜色变化 |
| C.实验过程中,竖直支管上方未见白烟产生 |
| D.停止加热后可以交替挤压两边乳胶头,使剩余的气体更充分吸收,减少污染 |
您最近一年使用:0次
2023-10-02更新
|
65次组卷
|
3卷引用:山西省晋中市平遥县第二中学校2023-2024学年高三上学期11月质检化学试题
名校
4 . 一氧化二氯( )是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。
)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。 的熔点是-120.6℃,沸点是2.0℃。利用反应
的熔点是-120.6℃,沸点是2.0℃。利用反应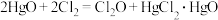 可制备
可制备 ,某同学利用如图所示装置制备
,某同学利用如图所示装置制备 。
。
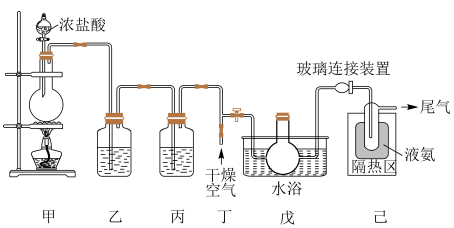
回答下列问题:
(1)装置甲的作用是为该制备反应提供 ,写出该装置中制备
,写出该装置中制备 的离子方程式为
的离子方程式为_______ 。
(2)装置乙的洗气瓶中盛放的试剂是_______ ;装置丙的作用是_______ 。
(3)反应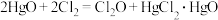 中,每生成1 mol
中,每生成1 mol  转移电子的物质的量为
转移电子的物质的量为_______ mol。若实验开始前称量装置戊中的玻璃丝与HgO的混合物的质量为48.0g,实验结束后玻璃丝及其附着物的质量为53.5g,则制备的 为
为_______ mol。
(4)25℃下, 的
的 ,HClO的
,HClO的 ,则:
,则:
①温度、浓度相同的 和HClO溶液,水的电离程度:前者
和HClO溶液,水的电离程度:前者_______ 后者(填“>”“=”或“<”)。
②相同温度下,pH相同的NaClO和 两种溶液中,
两种溶液中,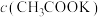
_______  (填“>”“=”或“<”,下同),
(填“>”“=”或“<”,下同),
_______ 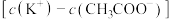 。
。
 )是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。
)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。 的熔点是-120.6℃,沸点是2.0℃。利用反应
的熔点是-120.6℃,沸点是2.0℃。利用反应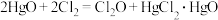 可制备
可制备 ,某同学利用如图所示装置制备
,某同学利用如图所示装置制备 。
。
回答下列问题:
(1)装置甲的作用是为该制备反应提供
 ,写出该装置中制备
,写出该装置中制备 的离子方程式为
的离子方程式为(2)装置乙的洗气瓶中盛放的试剂是
(3)反应
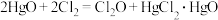 中,每生成1 mol
中,每生成1 mol  转移电子的物质的量为
转移电子的物质的量为 为
为(4)25℃下,
 的
的 ,HClO的
,HClO的 ,则:
,则:①温度、浓度相同的
 和HClO溶液,水的电离程度:前者
和HClO溶液,水的电离程度:前者②相同温度下,pH相同的NaClO和
 两种溶液中,
两种溶液中,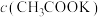
 (填“>”“=”或“<”,下同),
(填“>”“=”或“<”,下同),
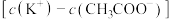 。
。
您最近一年使用:0次



