解题方法
1 . 硼酸(H3BO3)是一种一元弱酸,微溶于水,回答下列问题.
(1)H3BO3本身不能电离,只能通过结合来自水中的OH-而释放出H+,试写出H3BO3溶液的电离方程式______ ,该物质的电离方式和中学另一种常见物质的电离相似,该物质是(写化学式)______ ;
(2)硼砂(Na2B4O7▪10H2O)是硼酸的一种重要钠盐,工业上可利用碳碱法制取,以下是某化工集团利用合成氨脱碳尾气生产硼砂及其它化工产品的流程图.

回答下列问题:
①合成氨常用CH4与水蒸气反应,制取H2的同时获得脱碳尾气(上述流程图中的某物质),所发生的化学方程式为___________________ .
②轻质碳酸镁的组成可表示为xMgCO3.yMg(OH)2.zH2O,某小组为测定其成份,准确称取2.33g样品,充分加热后称得剩余物质质量为1.00g,所得气体经浓硫酸吸收,浓硫酸增重0.45g,则该轻质碳酸镁的化学式为:______________________ .
③结合②中的结论,推测该工厂生产硼砂溶液的化学方程式为:_________________ .
④a处的操作为:____________________ .
⑤该工艺可实现多种产品的联产,其中属于联产产品的是_______________________ .
a.轻质碳酸镁 b.轻质氧化镁 c.液态二氧化碳 d.纯碱.
(1)H3BO3本身不能电离,只能通过结合来自水中的OH-而释放出H+,试写出H3BO3溶液的电离方程式
(2)硼砂(Na2B4O7▪10H2O)是硼酸的一种重要钠盐,工业上可利用碳碱法制取,以下是某化工集团利用合成氨脱碳尾气生产硼砂及其它化工产品的流程图.

回答下列问题:
①合成氨常用CH4与水蒸气反应,制取H2的同时获得脱碳尾气(上述流程图中的某物质),所发生的化学方程式为
②轻质碳酸镁的组成可表示为xMgCO3.yMg(OH)2.zH2O,某小组为测定其成份,准确称取2.33g样品,充分加热后称得剩余物质质量为1.00g,所得气体经浓硫酸吸收,浓硫酸增重0.45g,则该轻质碳酸镁的化学式为:
③结合②中的结论,推测该工厂生产硼砂溶液的化学方程式为:
④a处的操作为:
⑤该工艺可实现多种产品的联产,其中属于联产产品的是
a.轻质碳酸镁 b.轻质氧化镁 c.液态二氧化碳 d.纯碱.
您最近一年使用:0次
解题方法
2 . 氨基甲酸铵(H2NCOONH4)是一种重要的化工原料,可用作化学肥料、灭火剂、洗涤剂等。某化学兴趣小组用以下装置制取氨基甲酸铵。
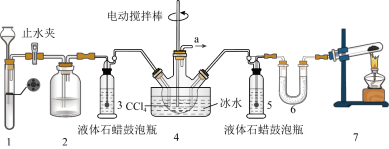
已知:①制取氨基甲酸铵反应为: 2NH3(g)+CO2(g)⇌H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是_______
(2)装置6中的试剂是_______ ,导管a出口直接与尾气处理装置连接,该尾气处理装置中的试剂是_______ 。
(3)装置7中发生反应的化学方程式为_______
(4)三颈烧瓶需用冰水浴冷却,其目的是_______
(5) CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是_______ ,从三颈烧瓶中分离出粗产品的操作是_______
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是_______ [Mr(H2NCOONH4)=78、Mr(NH4HCO3)=79]

已知:①制取氨基甲酸铵反应为: 2NH3(g)+CO2(g)⇌H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是
(2)装置6中的试剂是
(3)装置7中发生反应的化学方程式为
(4)三颈烧瓶需用冰水浴冷却,其目的是
(5) CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是
您最近一年使用:0次
名校
解题方法
3 . 三氯化铬(CrCl3)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取CrCl3的反应为Cr2O3(s)+3CCl4(g) 2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
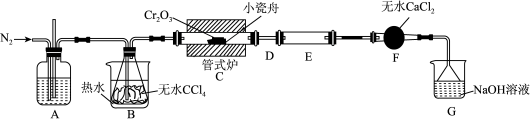
已知:①COCl2(俗称光气)有毒,遇水发生水解:COCl2+H2O=CO2+2HCl;
②碱性条件下,H2O2可将Cr3+氧化为 ;酸性条件下,H2O2将
;酸性条件下,H2O2将 还原为Cr3+。
还原为Cr3+。
请回答下列问题:
(1)A中的试剂为_______ ;无水CaCl2的作用是_______ ;反应结束后要继续通入一段时间氮气,主要目的是_______ 。
(2)装置E用来收集产物。实验过程中若D处出现堵塞,可观察到的现象是_______ ;可通过_______ (填操作)使实验继续进行。
(3)装置G中发生反应的离子方程式为_______ 。
(4)测定产品中CrCl3质量分数的实验步骤如下:
I.取mgCrCl3产品,在强碱性条件下,加入过量的30%H2O2溶液,小火加热使CrCl3完全转化为 ,继续加热一段时间;
,继续加热一段时间;
II.冷却后加适量的蒸馏水,再滴入适量的浓硫酸和浓磷酸(加浓磷酸的目的是为了防止指示剂提前变色),使 转化为
转化为 ;
;
III.用新配制的cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2标准溶液VmL(已知 被Fe2+还原为Cr3+)。
被Fe2+还原为Cr3+)。
①产品中CrCl3质量分数表达式为_______ %。
②下列操作将导致产品中CrCl3质量分数测定值偏低的是_______ (填字母标号)。
A.步骤I中未继续加热一段时间
B.步骤III中所用(NH4)2Fe(SO4)2溶液已变质
C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
 2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
已知:①COCl2(俗称光气)有毒,遇水发生水解:COCl2+H2O=CO2+2HCl;
②碱性条件下,H2O2可将Cr3+氧化为
 ;酸性条件下,H2O2将
;酸性条件下,H2O2将 还原为Cr3+。
还原为Cr3+。请回答下列问题:
(1)A中的试剂为
(2)装置E用来收集产物。实验过程中若D处出现堵塞,可观察到的现象是
(3)装置G中发生反应的离子方程式为
(4)测定产品中CrCl3质量分数的实验步骤如下:
I.取mgCrCl3产品,在强碱性条件下,加入过量的30%H2O2溶液,小火加热使CrCl3完全转化为
 ,继续加热一段时间;
,继续加热一段时间;II.冷却后加适量的蒸馏水,再滴入适量的浓硫酸和浓磷酸(加浓磷酸的目的是为了防止指示剂提前变色),使
 转化为
转化为 ;
;III.用新配制的cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2标准溶液VmL(已知
 被Fe2+还原为Cr3+)。
被Fe2+还原为Cr3+)。①产品中CrCl3质量分数表达式为
②下列操作将导致产品中CrCl3质量分数测定值偏低的是
A.步骤I中未继续加热一段时间
B.步骤III中所用(NH4)2Fe(SO4)2溶液已变质
C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
您最近一年使用:0次
2021-06-05更新
|
1281次组卷
|
11卷引用:山东省临沂市2021届高三第一次模拟考试化学试题
山东省临沂市2021届高三第一次模拟考试化学试题山东省济南市平阴县第一中学2021届高三下学期3月月考化学试题山东省2020-2021学年普通高中学业水平等级考试化学试题(已下线)重点7 化学实验综合题-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)2021年高考化学押题预测卷(新课标Ⅱ卷)(02)(含考试版、答题卡、参考答案、全解全析)(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)山西省阳泉市2021届高三下学期第三次教学质量检测(三模)理综化学试题四川省成都市第七中学高2022届高三10月阶段考试理综测试化学试题(已下线)专题17 综合实验设计、探究和评价-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题10 化学实验综合—2022年高考化学二轮复习讲练测(全国版)-测试山东省菏泽市单县第二中学2023届高三第一次模拟考试化学试题
名校
解题方法
4 .  是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备化肥X和
是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备化肥X和 的工艺流程如下:
的工艺流程如下:
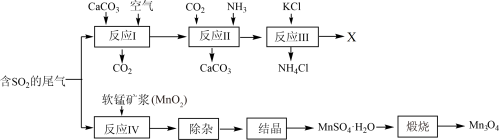
请回答下列问题:
(1)几种盐的溶解度见下图1,化肥X的化学式为_____ ;
(2)为获得固体X,加入KCl溶液后需对混合溶液进行蒸发浓缩,当析出大量晶体后,应_____ (填操作名称),再洗涤、干燥晶体。
(3)反应Ⅳ中发生反应的方程式为_____ 。
(4)图2是隔绝空气条件煅烧 时剩余固体质量与温度的变化曲线,请写出A→B的化学方程式:
时剩余固体质量与温度的变化曲线,请写出A→B的化学方程式:_____ 。
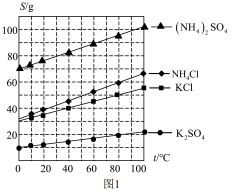

(5)为测定产品中 的纯度,取2.500g样品与浓盐酸共热(杂质不与盐酸反应),将产生的气体通入足量淀粉-KI溶液中,稀释至250mL,从中取25.00mL用
的纯度,取2.500g样品与浓盐酸共热(杂质不与盐酸反应),将产生的气体通入足量淀粉-KI溶液中,稀释至250mL,从中取25.00mL用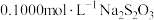 标准溶液滴定至终点时,消耗20.00mL标准溶液(
标准溶液滴定至终点时,消耗20.00mL标准溶液(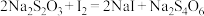 )。
)。
①样品与浓盐酸发生反应( 的还原产物为
的还原产物为 )的离子方程式为
)的离子方程式为_____ 。
②求样品的纯度(写出计算过程,计算结果保留1位小数)_____ 。
 是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备化肥X和
是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备化肥X和 的工艺流程如下:
的工艺流程如下:
请回答下列问题:
(1)几种盐的溶解度见下图1,化肥X的化学式为
(2)为获得固体X,加入KCl溶液后需对混合溶液进行蒸发浓缩,当析出大量晶体后,应
(3)反应Ⅳ中发生反应的方程式为
(4)图2是隔绝空气条件煅烧
 时剩余固体质量与温度的变化曲线,请写出A→B的化学方程式:
时剩余固体质量与温度的变化曲线,请写出A→B的化学方程式:

(5)为测定产品中
 的纯度,取2.500g样品与浓盐酸共热(杂质不与盐酸反应),将产生的气体通入足量淀粉-KI溶液中,稀释至250mL,从中取25.00mL用
的纯度,取2.500g样品与浓盐酸共热(杂质不与盐酸反应),将产生的气体通入足量淀粉-KI溶液中,稀释至250mL,从中取25.00mL用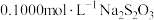 标准溶液滴定至终点时,消耗20.00mL标准溶液(
标准溶液滴定至终点时,消耗20.00mL标准溶液(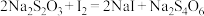 )。
)。①样品与浓盐酸发生反应(
 的还原产物为
的还原产物为 )的离子方程式为
)的离子方程式为②求样品的纯度(写出计算过程,计算结果保留1位小数)
您最近一年使用:0次
解题方法
5 .  是一种黄色油状液体,熔点
是一种黄色油状液体,熔点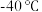 ,沸点
,沸点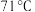 ,不溶于冷水,常温下密度为
,不溶于冷水,常温下密度为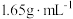 。
。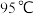 以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用
以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用 和
和 溶液在常温下反应制取,所用装置如下:
溶液在常温下反应制取,所用装置如下:
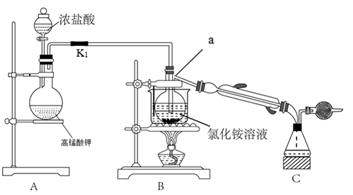
回答下列问题:
(1) 的分子构型为
的分子构型为___________ 。
(2)仪器a的名称为___________ ;实验室利用装置A还可以制备下列哪些物质___________ (填字母)。
a、乙炔b、硝基苯c、溴苯d、乙酸乙酯
(3)打开活塞 ,将浓盐酸滴入圆底烧瓶中,仪器a中制备
,将浓盐酸滴入圆底烧瓶中,仪器a中制备 的化学反应方程式为
的化学反应方程式为___________ ,待反应至仪器a中有大量油状液体生成,关闭活塞 。将产物分离并用无水
。将产物分离并用无水 干燥后,利用B、C装置将
干燥后,利用B、C装置将 提纯,提纯过程中水浴温度应控制在
提纯,提纯过程中水浴温度应控制在___________ 。
(4)将提纯后的 滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是
滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是___________ (使用化学用语结合文字解释)。
(5)液氯储罐中常混有 。为测定氯气中的
。为测定氯气中的 含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为:
含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为: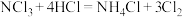 ),产生的气体通过饱和食盐水后再用足量
),产生的气体通过饱和食盐水后再用足量 溶液吸收,测得吸收后
溶液吸收,测得吸收后 溶液增重
溶液增重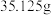 。经测定
。经测定 吸收管内
吸收管内 质量为
质量为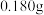 。该样品中
。该样品中 的质量分数为
的质量分数为___________ %(保留三位有效数字);若产生的气体未通过饱和食盐水,则测定结果___________ (填“偏高”“偏低”或“无影响”)。
 是一种黄色油状液体,熔点
是一种黄色油状液体,熔点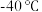 ,沸点
,沸点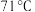 ,不溶于冷水,常温下密度为
,不溶于冷水,常温下密度为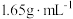 。
。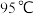 以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用
以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用 和
和 溶液在常温下反应制取,所用装置如下:
溶液在常温下反应制取,所用装置如下:
回答下列问题:
(1)
 的分子构型为
的分子构型为(2)仪器a的名称为
a、乙炔b、硝基苯c、溴苯d、乙酸乙酯
(3)打开活塞
 ,将浓盐酸滴入圆底烧瓶中,仪器a中制备
,将浓盐酸滴入圆底烧瓶中,仪器a中制备 的化学反应方程式为
的化学反应方程式为 。将产物分离并用无水
。将产物分离并用无水 干燥后,利用B、C装置将
干燥后,利用B、C装置将 提纯,提纯过程中水浴温度应控制在
提纯,提纯过程中水浴温度应控制在(4)将提纯后的
 滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是
滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是(5)液氯储罐中常混有
 。为测定氯气中的
。为测定氯气中的 含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为:
含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为: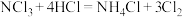 ),产生的气体通过饱和食盐水后再用足量
),产生的气体通过饱和食盐水后再用足量 溶液吸收,测得吸收后
溶液吸收,测得吸收后 溶液增重
溶液增重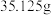 。经测定
。经测定 吸收管内
吸收管内 质量为
质量为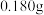 。该样品中
。该样品中 的质量分数为
的质量分数为
您最近一年使用:0次
6 . 为探究不同价态铜的氧化物对电化学还原CO2产生的影响,某兴趣小组进行以下活动。
Ⅰ.制备过氧化铜(CuO2)
在含有0.5 gPVP(做稳定剂)的5 mL 0.01 mmol·L−1的CuCl2水溶液中,加入5 mL 0.03 mmol·L−1的NaOH溶液反应得到Cu(OH)2。随后在强磁力搅拌和0℃条件下,逐滴加入1 mL 30% H2O2反应0.5h,经一系列操作得到黄褐色的CuO2沉淀。
(1)由Cu(OH)2生成CuO2的化学方程式为___________ 。
(2)反应控制在0℃,原因是___________ 。
(3)为了探究CuO2的性质,分别向一定量的KMnO4溶液中缓慢加入(滴入)CuO2样品或H2O2溶液,实验结果如下 (已知:实验4与实验7均恰好反应完全):
CuO2样品和H2O2与酸性KMnO4溶液反应的用量及现象
①1mg CuO2样品与___________ μL的H2O2溶液还原能力相当
②若CuO2纯度为96%,过氧化氢物质的量浓度约为___________ mol·L−1.(1μL = 10−6L)
③“实验4”中,最终溶液的颜色是___________ 。
Ⅱ.制备CuO
将CuO2置于管式炉中(如下图所示),在O2气氛下300℃处理2 h,得到黑色的CuO。

已知:a. 加热时试管内会产生少量黄绿色单质气体
b. 高温下有如下反应:4CuO(s) 2Cu2O(s) + O2(g)。
2Cu2O(s) + O2(g)。
(4)装置D中盛放的试剂为___________ 。
(5)管式炉中CuO2反应的化学方程式为___________ 。
(6)通入氧气的目的是___________ 。
Ⅲ.探究CuO2催化电化学还原CO2的结果
(7)以KHCO3溶液为电解液,在指定的电势区间,利用CuO2催化还原CO2,测得阴极产物组成及电流效率( )如下表所示:(
)如下表所示:( =
= )
)
①该条件下,CO2还原产物有___________ 种
②CH4与C2H4物质的量之比为___________ 。
Ⅰ.制备过氧化铜(CuO2)
在含有0.5 gPVP(做稳定剂)的5 mL 0.01 mmol·L−1的CuCl2水溶液中,加入5 mL 0.03 mmol·L−1的NaOH溶液反应得到Cu(OH)2。随后在强磁力搅拌和0℃条件下,逐滴加入1 mL 30% H2O2反应0.5h,经一系列操作得到黄褐色的CuO2沉淀。
(1)由Cu(OH)2生成CuO2的化学方程式为
(2)反应控制在0℃,原因是
(3)为了探究CuO2的性质,分别向一定量的KMnO4溶液中缓慢加入(滴入)CuO2样品或H2O2溶液,实验结果如下 (已知:实验4与实验7均恰好反应完全):
CuO2样品和H2O2与酸性KMnO4溶液反应的用量及现象
| 编号 | m(CuO2)/mg | V(H2O2)/ μL | V(H2SO4)/mL | V(KMnO4)/ μL | 实验结束时溶液的颜色 |
| 1 | - | - | 2 | 10 | 紫色 |
| 2 | 1 | - | 2 | 10 | 浅紫色 |
| 3 | 2 | - | 2 | 10 | 浅紫色 |
| 4 | 4 | - | 2 | 10 | - |
| 5 | - | 10 | 2 | 10 | 浅紫色 |
| 6 | - | 20 | 2 | 10 | 浅紫色 |
| 7 | - | 40 | 2 | 10 | 无色 |
②若CuO2纯度为96%,过氧化氢物质的量浓度约为
③“实验4”中,最终溶液的颜色是
Ⅱ.制备CuO
将CuO2置于管式炉中(如下图所示),在O2气氛下300℃处理2 h,得到黑色的CuO。

已知:a. 加热时试管内会产生少量黄绿色单质气体
b. 高温下有如下反应:4CuO(s)
 2Cu2O(s) + O2(g)。
2Cu2O(s) + O2(g)。 (4)装置D中盛放的试剂为
(5)管式炉中CuO2反应的化学方程式为
(6)通入氧气的目的是
Ⅲ.探究CuO2催化电化学还原CO2的结果
(7)以KHCO3溶液为电解液,在指定的电势区间,利用CuO2催化还原CO2,测得阴极产物组成及电流效率(
 )如下表所示:(
)如下表所示:( =
= )
)| 阴极产物 | CO | CH4 | C2H4 | H2 |
| 电流效率/% | 5 | 18 | 30 | 15 |
②CH4与C2H4物质的量之比为
您最近一年使用:0次
2023-05-09更新
|
333次组卷
|
2卷引用:福建省龙岩市2023届高中毕业班五月教学质量检测化学试题
解题方法
7 . 已知;S4N4是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与SCl2反应制得。某同学利用如图装置制取SCl2,然后制取S4N4。已知:SCl2为红棕色液体,有刺激性臭味,熔点:-78℃,沸点:60℃,易水解。
反应步骤:①反应时先向三颈烧瓶中通入干燥的氯气,使硫粉与氯气在50℃下反应生成SCl2。
②待三颈烧瓶中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉A、B装置。
③连接制氨气的装置,通入氨气,反应制得S4N4。
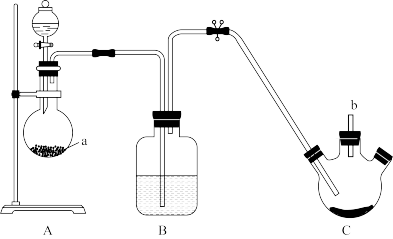
试回答下列问题。
(1)仪器a的名称为___________ ,a中次氯酸钙可与浓盐酸反应制备氯气,写出反应的化学方程式___________ 。
(2)B装置中应选择的试剂为___________ 。
(3)制取SCl2过程中,b导管末端连接装有碱石灰的干燥管,其作用是___________ 。
(4)向制得的SCl2中通入NH3,生成S4N4的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式___________ 。所得产物分离后,检验所得盐中阳离子的具体操作步骤和现象___________ 。
(5)S4N4在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定S4N4的纯度。称取5.00gS4N4;样品,加入NaOH溶液,并加热,释放出的氨气用足量100mL1.00mol·L-1硼酸溶液吸收[反应方程式为2NH3+4H3BO3=(NH4)2B4O7+5H2O,假定反应过程中溶液体积不变]。取反应后的硼酸溶液25.00mL,以甲基红-亚甲蓝为指示剂,再用1.00mol·L-1的盐酸[滴定反应方程式为(NH4)2B4O7+2HCl+5H2O =2NH4Cl+4H3BO3]进行滴定,达到滴定终点时消耗盐酸体积为20.00mL。则制得的S4N4的纯度为___________ 。
(6)下列实验操作可能使S4N4测定结果偏低的是___________ 。
A.滴定时未用盐酸标准溶液润洗滴定管
B.滴定前滴定管尖嘴处无气泡,滴定结束后产生气泡
C.读数时,滴定前平视,滴定后仰视
反应步骤:①反应时先向三颈烧瓶中通入干燥的氯气,使硫粉与氯气在50℃下反应生成SCl2。
②待三颈烧瓶中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉A、B装置。
③连接制氨气的装置,通入氨气,反应制得S4N4。

试回答下列问题。
(1)仪器a的名称为
(2)B装置中应选择的试剂为
(3)制取SCl2过程中,b导管末端连接装有碱石灰的干燥管,其作用是
(4)向制得的SCl2中通入NH3,生成S4N4的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式
(5)S4N4在碱性条件下发生水解反应氮元素转化为氨气,用硼酸吸收,滴定氨气释放量可进一步测定S4N4的纯度。称取5.00gS4N4;样品,加入NaOH溶液,并加热,释放出的氨气用足量100mL1.00mol·L-1硼酸溶液吸收[反应方程式为2NH3+4H3BO3=(NH4)2B4O7+5H2O,假定反应过程中溶液体积不变]。取反应后的硼酸溶液25.00mL,以甲基红-亚甲蓝为指示剂,再用1.00mol·L-1的盐酸[滴定反应方程式为(NH4)2B4O7+2HCl+5H2O =2NH4Cl+4H3BO3]进行滴定,达到滴定终点时消耗盐酸体积为20.00mL。则制得的S4N4的纯度为
(6)下列实验操作可能使S4N4测定结果偏低的是
A.滴定时未用盐酸标准溶液润洗滴定管
B.滴定前滴定管尖嘴处无气泡,滴定结束后产生气泡
C.读数时,滴定前平视,滴定后仰视
您最近一年使用:0次
解题方法
8 .  (三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备
(三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备 ,然后再制备三草酸合铁酸钾。
,然后再制备三草酸合铁酸钾。
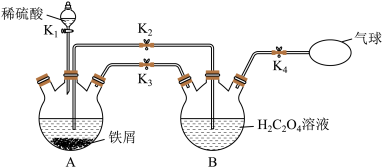
回答下列问题:
(1)打开 、
、 和
和 ,关闭
,关闭 ,制备
,制备 。为使生成的
。为使生成的 溶液与
溶液与 溶液接触,应进行的操作为
溶液接触,应进行的操作为___________ ,B中生成 沉淀的离子方程式为
沉淀的离子方程式为___________ 。
(2)向 中加入过量饱和
中加入过量饱和 溶液,水浴加热并缓慢滴加
溶液,水浴加热并缓慢滴加 溶液,制得
溶液,制得 ,同时有红褐色沉淀生成,该反应的化学方程式为
,同时有红褐色沉淀生成,该反应的化学方程式为___________ ;将上述混合物煮沸,加入饱和 溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是
溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是___________ ; 的作用是
的作用是___________ 。
(3)制备的 中可能含有
中可能含有 ,采用
,采用 滴定法测定产品纯度,实验步骤如下。
滴定法测定产品纯度,实验步骤如下。
I.取a g样品于锥形瓶中,加入稀 溶解,水浴加热至75℃。用
溶解,水浴加热至75℃。用 的
的 溶液趁热滴定,消耗
溶液趁热滴定,消耗 溶液
溶液 。
。
II.向上述溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,在75℃继续用
酸化后,在75℃继续用 溶液滴定,又消耗
溶液滴定,又消耗 溶液
溶液 。
。
若省略步骤II,能否测定 的质量分数
的质量分数___________ (若能,写出表达式;若不能,说明原因);若样品中不含 ,则
,则 与
与 的关系为
的关系为___________ ;若步骤I中滴入 不足,则测得样品中Fe元素含量
不足,则测得样品中Fe元素含量___________ (填“偏高”、“偏低”或“不变”)。
 (三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备
(三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备 ,然后再制备三草酸合铁酸钾。
,然后再制备三草酸合铁酸钾。
回答下列问题:
(1)打开
 、
、 和
和 ,关闭
,关闭 ,制备
,制备 。为使生成的
。为使生成的 溶液与
溶液与 溶液接触,应进行的操作为
溶液接触,应进行的操作为 沉淀的离子方程式为
沉淀的离子方程式为(2)向
 中加入过量饱和
中加入过量饱和 溶液,水浴加热并缓慢滴加
溶液,水浴加热并缓慢滴加 溶液,制得
溶液,制得 ,同时有红褐色沉淀生成,该反应的化学方程式为
,同时有红褐色沉淀生成,该反应的化学方程式为 溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是
溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是 的作用是
的作用是(3)制备的
 中可能含有
中可能含有 ,采用
,采用 滴定法测定产品纯度,实验步骤如下。
滴定法测定产品纯度,实验步骤如下。I.取a g样品于锥形瓶中,加入稀
 溶解,水浴加热至75℃。用
溶解,水浴加热至75℃。用 的
的 溶液趁热滴定,消耗
溶液趁热滴定,消耗 溶液
溶液 。
。II.向上述溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,在75℃继续用
酸化后,在75℃继续用 溶液滴定,又消耗
溶液滴定,又消耗 溶液
溶液 。
。若省略步骤II,能否测定
 的质量分数
的质量分数 ,则
,则 与
与 的关系为
的关系为 不足,则测得样品中Fe元素含量
不足,则测得样品中Fe元素含量
您最近一年使用:0次
解题方法
9 . 无水 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水 的实验装置如图所示:
的实验装置如图所示:

E和G用来收集产物。回答下列问题:
(1)通入氯气后,A中观察到有酸雾产生,C中 的作用是
的作用是_______ 。
(2)在E、G处收集产物是利用了
_______ 的性质。
(3)实验过程中若F处出现堵塞,则在B处可观察到的现象是_______ 。可通过_______ (填简单操作),使实验能继续进行。
(4)Ⅰ中反应的离子方程式为_______ 。
(5)某同学用 干燥铁粉制得无水
干燥铁粉制得无水 样品
样品 ,该次实验的产率是
,该次实验的产率是_______ 。
(6)实验室中还常用 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为_______ .检验水合三氯化铁原料中是否存在 的试剂是
的试剂是_______ 。
 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水 的实验装置如图所示:
的实验装置如图所示:
E和G用来收集产物。回答下列问题:
(1)通入氯气后,A中观察到有酸雾产生,C中
 的作用是
的作用是(2)在E、G处收集产物是利用了

(3)实验过程中若F处出现堵塞,则在B处可观察到的现象是
(4)Ⅰ中反应的离子方程式为
(5)某同学用
 干燥铁粉制得无水
干燥铁粉制得无水 样品
样品 ,该次实验的产率是
,该次实验的产率是(6)实验室中还常用
 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为 的试剂是
的试剂是
您最近一年使用:0次
解题方法
10 . POCl3遇水强烈水解: ,是一种重要的化工原料。某兴趣小组准备在实验室中进行POC13制备实验。
,是一种重要的化工原料。某兴趣小组准备在实验室中进行POC13制备实验。
(1)小组同学在如图装置中分别加入三氯化磷、氧气、二氧化硫来制备POC13,产物中还有一种遇水强烈水解的物质SOCl2,写出SOCl2水解的化学方程式:______ 。

(2)仪器乙的名称为______ 。
(3)反应温度需控制在60~65℃,应采取的加热方法为______ ,温度不能过高或过低的原因是______ 。
(4)小组同学查阅资料后,用以下方法测定POCl3含量:准确称取4.00 g POCl3样品溶于水中(杂质不参与反应),加水稀释至250.00mL;取25.00mL溶液置于锥形瓶中,滴加几滴甲基橙作指示剂,用0.60mol·L-1NaOH标准溶液滴定,当滴定至终点时,溶质为NaCl和NaH2PO4,共用去NaOH标准溶液16.00mL。已知常温时,0.1mol·L-1下列溶液的pH如下表:
①滴定终点时的现象为______ 。
②滴定中若改用酚酞为指示剂,则滴定至终点时,溶液中溶质主要为______ ;此时消耗0.60mol·L-1NaOH标准溶液的体积为______ mL。
③产品中POCl3的百分含量为______ 。
 ,是一种重要的化工原料。某兴趣小组准备在实验室中进行POC13制备实验。
,是一种重要的化工原料。某兴趣小组准备在实验室中进行POC13制备实验。(1)小组同学在如图装置中分别加入三氯化磷、氧气、二氧化硫来制备POC13,产物中还有一种遇水强烈水解的物质SOCl2,写出SOCl2水解的化学方程式:

(2)仪器乙的名称为
(3)反应温度需控制在60~65℃,应采取的加热方法为
(4)小组同学查阅资料后,用以下方法测定POCl3含量:准确称取4.00 g POCl3样品溶于水中(杂质不参与反应),加水稀释至250.00mL;取25.00mL溶液置于锥形瓶中,滴加几滴甲基橙作指示剂,用0.60mol·L-1NaOH标准溶液滴定,当滴定至终点时,溶质为NaCl和NaH2PO4,共用去NaOH标准溶液16.00mL。已知常温时,0.1mol·L-1下列溶液的pH如下表:
| 溶液 | Na3PO4 | Na2HPO4 | NaH2PO4 |
| pH | 12.67 | 9.73 | 4.66 |
②滴定中若改用酚酞为指示剂,则滴定至终点时,溶液中溶质主要为
③产品中POCl3的百分含量为
您最近一年使用:0次



