真题
名校
1 . 单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
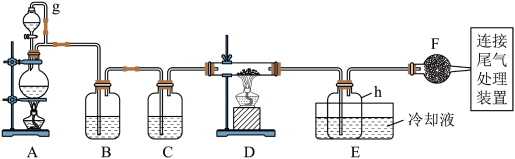
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:____________________________ 。
(2)装置A中g管的作用是______________ ;装置C中的试剂是____________ ;装置E中的h瓶需要冷却的理由是________________________________________ 。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是____________ (填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式为5Fe2++MnO +8H+===5Fe3++Mn2++4H2O。
+8H+===5Fe3++Mn2++4H2O。
①滴定前是否要滴加指示剂?________ (填“是”或“否”),请说明理由:
____________________________________________________________ 。
②某同学称取5.000 g残留物,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000×10-2 mol· L-1 KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是________ 。

相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:
(2)装置A中g管的作用是
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式为5Fe2++MnO
 +8H+===5Fe3++Mn2++4H2O。
+8H+===5Fe3++Mn2++4H2O。①滴定前是否要滴加指示剂?
②某同学称取5.000 g残留物,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000×10-2 mol· L-1 KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是
您最近一年使用:0次
2016-12-09更新
|
503次组卷
|
10卷引用:2020年安徽省全省教学质量检测统一考试(练习检测一)
2020年安徽省全省教学质量检测统一考试(练习检测一)2009年普通高等学校招生统一考试理综试题化学部分(浙江卷)09真题汇编-物质的制备、分离与提纯、鉴别与检验2009高考真题分类汇编-碳族元素 无机非金属材料(已下线)2011-2012学年黑龙江省大庆实验中学高二上学期期中考试化学试卷(已下线)2014年高考化学苏教版总复习 3-3 含硅矿物与信息材料练习卷2018届高三一轮复习化学:微考点24-硅的制取及应用(已下线)二轮复习 专题6 非金属及其化合物 押题专练(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(押题专练)新疆吾尔自治区乌鲁木齐市第七十中学、哈密二中2019-2020学年高二下学期期末考试化学试题
名校
解题方法
2 . 以二氧化锰和浓盐酸为主要原料制取氯气,并设计了如图所示装置(其中A是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)。
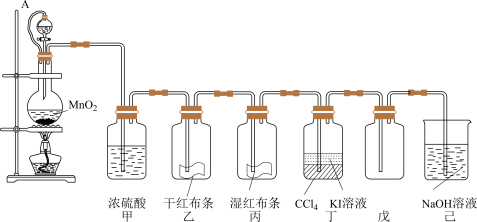
试回答下列问题:
(1)乙和丙中的现象分别是_____ ;由上述现象可得出结论:_____ (写化学式)具有漂白作用;
(2)圆底烧瓶内发生反应的化学方程式为_____ ;分液漏斗与烧瓶连接橡皮管的目的是_____ ;
(3)ClO2气体是一种新型高效含氯消毒剂。实验室可通过以下反应制2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。若反应共产生了0.2mol气体,消耗还原剂的质量为_____ g。ClO2的有效氯含量为_____ (有效氯含量指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力)。
(4)用ClO2气体可去除地下水中Mn2+,生成难溶于水的MnO2,该反应的离子方程式为_____ 。

试回答下列问题:
(1)乙和丙中的现象分别是
(2)圆底烧瓶内发生反应的化学方程式为
(3)ClO2气体是一种新型高效含氯消毒剂。实验室可通过以下反应制2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。若反应共产生了0.2mol气体,消耗还原剂的质量为
(4)用ClO2气体可去除地下水中Mn2+,生成难溶于水的MnO2,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 芳香酸是分子中羧基与苯环直接相连的一类有机物,通常用芳香烃的氧化来制备。反应原理如下:
 +2KMnO4
+2KMnO4
 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
 +HCl→
+HCl→ +KCl
+KCl
反应试剂、产物的物理常数:
主要实验装置和流程如图:

实验方法:一定量的甲苯和KMnO4溶液加入图1装置中,在90℃时,反应一段时间后,停止反应,按如图流程分离出苯甲酸并回收未反应的甲苯。

(1)白色固体B中主要成分的分子式为______ ,操作Ⅱ为______ 。
(2)下列关于仪器的组装或者使用正确的是______ 。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.如图回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是上进下出
(3)除去残留在苯甲酸中的甲苯应先加入______ ,分液,然后再向水层中加入______ ,抽滤,洗涤,干燥即可得到苯甲酸。
(4)纯度测定:称取2.440g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为4.5×10-3mol。产品中苯甲酸质量分数为______ 。
 +2KMnO4
+2KMnO4
 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O +HCl→
+HCl→ +KCl
+KCl反应试剂、产物的物理常数:
| 名称 | 相对分子质量 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) | 水中的溶解性 |
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 |

实验方法:一定量的甲苯和KMnO4溶液加入图1装置中,在90℃时,反应一段时间后,停止反应,按如图流程分离出苯甲酸并回收未反应的甲苯。

(1)白色固体B中主要成分的分子式为
(2)下列关于仪器的组装或者使用正确的是
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.如图回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是上进下出
(3)除去残留在苯甲酸中的甲苯应先加入
(4)纯度测定:称取2.440g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为4.5×10-3mol。产品中苯甲酸质量分数为
您最近一年使用:0次
4 . 碘元素被称为“智力元素”,海洋植物如海带、海藻中存在丰富的碘元素,一般以碘离子形式存在。某小组设计实验从20.00g海藻中提取碘单质,实验流程如下:
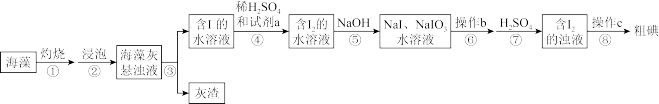
试回答下列问题:
(1)灼烧海藻时,将海藻用___________ (填化学式)润湿后,置于___________ (填装置名称)中烧成灰烬。
(2)从下列试剂中选择可做试剂a的是___________ (填序号)。
A.H2O2 B.MnO2 C.FeCl2 D.SO2
有人提出试剂a可以是Cl2,但是使用时必须控制用量,否则生成的I2,又被Cl2氧化为+5价,该反应的化学方程式为___________
(3)操作b是___________ ,滴加稀硫酸时发生的离子反应方程式为___________ 操作c为过滤,滤液可返回至___________ (填步骤序号)操作后溶液中循环利用。
(4)碘量法常用于测量草药中可能残余的有毒元素As的含量:
①取1000g草药样品进行前期处理制得待测溶液1000mL,此时样品中含有的砷元素转化为H3AsO3;
②转移100mL待测液至250mL锥形瓶中,加入1.000×10-3mol·L-1标准I2溶液20.00mL(H3AsO3转化为H3AsO4),并加入少量的淀粉溶液;
③用1.000×103mol·L-1的硫代硫酸钠标准溶液滴定过量的碘(已知:2 +I2=2I-+
+I2=2I-+ )。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为
)。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为___________ mg/kg;若滴定时溶液酸性过强,会导致测量结果___________ (填“偏高”或“偏低”)。

试回答下列问题:
(1)灼烧海藻时,将海藻用
(2)从下列试剂中选择可做试剂a的是
A.H2O2 B.MnO2 C.FeCl2 D.SO2
有人提出试剂a可以是Cl2,但是使用时必须控制用量,否则生成的I2,又被Cl2氧化为+5价,该反应的化学方程式为
(3)操作b是
(4)碘量法常用于测量草药中可能残余的有毒元素As的含量:
①取1000g草药样品进行前期处理制得待测溶液1000mL,此时样品中含有的砷元素转化为H3AsO3;
②转移100mL待测液至250mL锥形瓶中,加入1.000×10-3mol·L-1标准I2溶液20.00mL(H3AsO3转化为H3AsO4),并加入少量的淀粉溶液;
③用1.000×103mol·L-1的硫代硫酸钠标准溶液滴定过量的碘(已知:2
 +I2=2I-+
+I2=2I-+ )。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为
)。滴定终点时消耗22.00mL硫代硫酸钠标准溶液,则草药中砷的含量为
您最近一年使用:0次
真题
名校
5 . 医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%~103.0%)的主要流程如下:
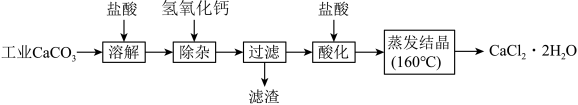
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是________________ 。
(2)酸化操作是加入盐酸,调节溶液的pH为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③_______________ 。
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测液于锥形瓶中;c.用0.05000mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
①上述测定过程中需用溶液润洗的仪器有:____________________ 。
②计算上述样品中CaCl2·2H2O的质量分数为:____________________ 。
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:__________ ;___________ 。

(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是
(2)酸化操作是加入盐酸,调节溶液的pH为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测液于锥形瓶中;c.用0.05000mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
①上述测定过程中需用溶液润洗的仪器有:
②计算上述样品中CaCl2·2H2O的质量分数为:
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:
您最近一年使用:0次
2019-01-30更新
|
1152次组卷
|
5卷引用:2020年安徽省全省教学质量检测统一考试(练习检测一)
2020年安徽省全省教学质量检测统一考试(练习检测一)2009年普通高等学校招生统一考试化学试题(江苏卷)2009高考真题汇编-化学实验常用仪器和基本操作(已下线)2011届湖北省天门市高三模拟考试(三)(理综)化学部分河北省黄骅中学2018-2019学年高二上学期第二次月考化学试题
6 . 某铝土矿和黄铁矿的共生矿(主要成分为Al2O3、FeS2和SiO2),由此矿石制备Fe3O4和Al2O2的流程如下图所示:

回答下列问题:
(1)“步骤2焙烧过程产生的废气为___________ 。
(2)已知“步骤4隔绝空气焙烧,则化学方程式为______________________ (已知该过程产生的废气和废气1成分相同)。
(3)“滤渣2”的成分是___________ ,其重要用途为______________________ 。
(4)常温下,向“滤液2”中加入氨水,当Al3+沉淀完全时,溶液的pH约为___________ 。(若当离子浓度小于1.0×10-5mol/L时,认为沉淀完全,已知Ksp[Al(OH)3]=1.0×10-32)
(5)若原矿石质量为bkg,经过该流程获得的Fe3O4的质量为akg则原矿石中铁元素的质量分数为___________ 。
(6)该流程中存在较为明显的缺陷是_________________________________ 。

回答下列问题:
(1)“步骤2焙烧过程产生的废气为
(2)已知“步骤4隔绝空气焙烧,则化学方程式为
(3)“滤渣2”的成分是
(4)常温下,向“滤液2”中加入氨水,当Al3+沉淀完全时,溶液的pH约为
(5)若原矿石质量为bkg,经过该流程获得的Fe3O4的质量为akg则原矿石中铁元素的质量分数为
(6)该流程中存在较为明显的缺陷是
您最近一年使用:0次
真题
7 . 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O:
用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是_______________ 。
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子
(ClO2-)。2001年我国卫生部规定,饮用水中ClO2-的含量应不超过0.2mg·L-1。
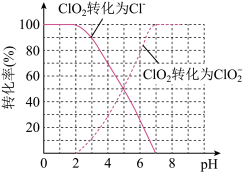
饮用水中ClO2、ClO2-的含量可用连续碘量法进行测定。ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如图所示。
当pH≤2.0时,ClO2-也能被I-还原成Cl-。
反应生成的I2用标准Na2S2O3溶液滴定: Na2S2O3+I2=Na2S4O6+2NaI
①请写出pH≤2.0时,ClO2-与I-反应的离子方程式______________________ 。
②请完成相应的实验步骤:
步骤1:准确量取VmL水样加入到锥形瓶中。
步骤2:调节水样的pH为7.0~8.0。
步骤3:加入足量的KI晶体。
步骤4:加入少量淀粉溶液,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。
步骤5:______________________ 。
步骤6:再用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。
③根据上述分析数据,测得该饮用水样中ClO2-浓度为_____________ mol·L-1用含字母的代数式表示)
④若饮用水中ClO2-的含量超标,可向其中加入适量的Fe2+将ClO2-还原成Cl-,该反应的氧化产物是___________ (填化学式)。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O:
用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子
(ClO2-)。2001年我国卫生部规定,饮用水中ClO2-的含量应不超过0.2mg·L-1。
饮用水中ClO2、ClO2-的含量可用连续碘量法进行测定。ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如图所示。

当pH≤2.0时,ClO2-也能被I-还原成Cl-。
反应生成的I2用标准Na2S2O3溶液滴定: Na2S2O3+I2=Na2S4O6+2NaI
①请写出pH≤2.0时,ClO2-与I-反应的离子方程式
②请完成相应的实验步骤:
步骤1:准确量取VmL水样加入到锥形瓶中。
步骤2:调节水样的pH为7.0~8.0。
步骤3:加入足量的KI晶体。
步骤4:加入少量淀粉溶液,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。
步骤5:
步骤6:再用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。
③根据上述分析数据,测得该饮用水样中ClO2-浓度为
④若饮用水中ClO2-的含量超标,可向其中加入适量的Fe2+将ClO2-还原成Cl-,该反应的氧化产物是
您最近一年使用:0次
2016-12-09更新
|
242次组卷
|
3卷引用:2020年安徽省全省教学质量检测统一考试(练习检测一)



