1 . 硫氰化钾( )俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
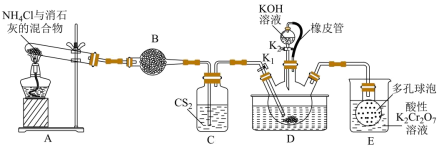
已知:① 不溶于水,密度比水的大;
不溶于水,密度比水的大;
② 不溶于
不溶于 ;
;
③三颈烧瓶内盛放有 、水和催化剂。
、水和催化剂。
回答下列问题:
(1)制备 溶液:
溶液:
①实验前,经检验装置的气密性良好。其中装置B中的试剂是___________ 。
②实验开始时,打开K,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应
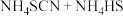 该反应比较缓慢),当看到
该反应比较缓慢),当看到___________ 现象时说明该反应接近完全。
(2)制备 溶液:
溶液:
①熄灭A处的酒精灯,关闭 ,移开水浴,将装置D继续加热至105℃,当
,移开水浴,将装置D继续加热至105℃,当 完全分解后(
完全分解后(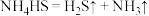 ),打开
),打开 ,继续保持液温105℃,缓缓滴入适量的
,继续保持液温105℃,缓缓滴入适量的 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为___________ 。
②装置E中多孔球泡的作用是___________ 。
(3)制备 晶体:先滤去三颈烧瓶中的固体催化剂,
晶体:先滤去三颈烧瓶中的固体催化剂,___________ 、___________ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
(4)测定晶体中 的含量:称取10.0g样品,配成
的含量:称取10.0g样品,配成 溶液。量取
溶液。量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴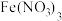 溶液作指示剂,用
溶液作指示剂,用
 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液 。
。
①滴定时发生的反应: (白色)。则判断到达滴定终点的方法是
(白色)。则判断到达滴定终点的方法是________ 。
②晶体中 的质量分数为
的质量分数为___________ (结果精确至0.1%)。
 )俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
已知:①
 不溶于水,密度比水的大;
不溶于水,密度比水的大;②
 不溶于
不溶于 ;
;③三颈烧瓶内盛放有
 、水和催化剂。
、水和催化剂。回答下列问题:
(1)制备
 溶液:
溶液:①实验前,经检验装置的气密性良好。其中装置B中的试剂是
②实验开始时,打开K,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应

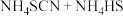 该反应比较缓慢),当看到
该反应比较缓慢),当看到(2)制备
 溶液:
溶液:①熄灭A处的酒精灯,关闭
 ,移开水浴,将装置D继续加热至105℃,当
,移开水浴,将装置D继续加热至105℃,当 完全分解后(
完全分解后(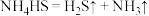 ),打开
),打开 ,继续保持液温105℃,缓缓滴入适量的
,继续保持液温105℃,缓缓滴入适量的 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为②装置E中多孔球泡的作用是
(3)制备
 晶体:先滤去三颈烧瓶中的固体催化剂,
晶体:先滤去三颈烧瓶中的固体催化剂,(4)测定晶体中
 的含量:称取10.0g样品,配成
的含量:称取10.0g样品,配成 溶液。量取
溶液。量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴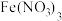 溶液作指示剂,用
溶液作指示剂,用
 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液 。
。①滴定时发生的反应:
 (白色)。则判断到达滴定终点的方法是
(白色)。则判断到达滴定终点的方法是②晶体中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 钴及其化合物在化工生产中有重要的用途。三氯化六氨合钴(Ⅲ)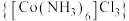 是黄色或橙黄色晶体,实验室以
是黄色或橙黄色晶体,实验室以 为原料经催化制备
为原料经催化制备 ,步骤如下:
,步骤如下:
Ⅰ. 的制备
的制备
 (易潮解)可以通过钴和氯气反应制得,实验室用下图实验装置制备纯净
(易潮解)可以通过钴和氯气反应制得,实验室用下图实验装置制备纯净 。
。
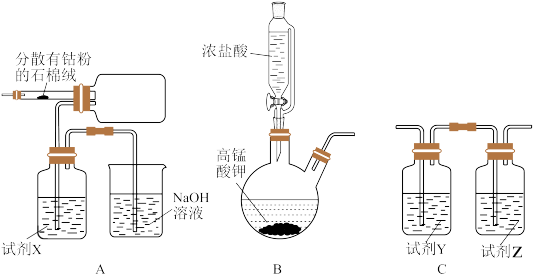
(1)装置的连接顺序为_______ (填字母),B装置用于制备氧气,其反应的化学方程式为_______ ,A装置中试剂X的名称为_______ 。
(2)组装好仪器进行实验时,要先加入浓盐酸,使B装置中开始生成氯气,待A装置内充满黄绿色气体,再加热A装置中的钴粉,目的是_______ 。
Ⅱ.三氯化六氨合钴(Ⅲ)的制备。其原理为: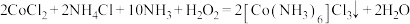 。
。

已知:三氯化六氨合钴不溶于乙醇,常温水中溶解度较小。
(3)水浴温度不超过 的原因是
的原因是_______ 。
(4)下列说法不正确的是_______(填标号)。
Ⅲ.晶体结构测定与钴含量分析。
(5)测定晶体结构最常见的仪器是_______ ,从而获取晶胞形状和大小、分子或原子在微观空间的有序排列。已知 具有正八面体的空间结构,
具有正八面体的空间结构, 中的2个
中的2个 被2个
被2个 取代,能得到
取代,能得到_______ 种产物。
(6)利用 将
将 氧化成
氧化成 ,
, 被还原后的产物为
被还原后的产物为 。然后用
。然后用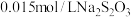 标准溶液滴定生成的
标准溶液滴定生成的 (已知:
(已知: )。若称取样品的质量为
)。若称取样品的质量为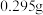 ,滴定
,滴定 时,达到终点消耗
时,达到终点消耗 标准溶液的平均体积为
标准溶液的平均体积为 。该样品中钴元素的质量分数为
。该样品中钴元素的质量分数为_______ %。
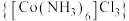 是黄色或橙黄色晶体,实验室以
是黄色或橙黄色晶体,实验室以 为原料经催化制备
为原料经催化制备 ,步骤如下:
,步骤如下:Ⅰ.
 的制备
的制备 (易潮解)可以通过钴和氯气反应制得,实验室用下图实验装置制备纯净
(易潮解)可以通过钴和氯气反应制得,实验室用下图实验装置制备纯净 。
。
(1)装置的连接顺序为
(2)组装好仪器进行实验时,要先加入浓盐酸,使B装置中开始生成氯气,待A装置内充满黄绿色气体,再加热A装置中的钴粉,目的是
Ⅱ.三氯化六氨合钴(Ⅲ)的制备。其原理为:
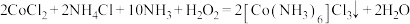 。
。
已知:三氯化六氨合钴不溶于乙醇,常温水中溶解度较小。
(3)水浴温度不超过
 的原因是
的原因是(4)下列说法不正确的是_______(填标号)。
A. 除作为反应物外,还有调节溶液的 除作为反应物外,还有调节溶液的 的作用 的作用 |
| B.活性炭是脱色剂,固体2是活性炭 |
C.加入浓盐酸,析出产品的反应方程式为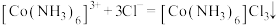 |
| D.可用乙醇水溶液洗涤产品 |
Ⅲ.晶体结构测定与钴含量分析。
(5)测定晶体结构最常见的仪器是
 具有正八面体的空间结构,
具有正八面体的空间结构, 中的2个
中的2个 被2个
被2个 取代,能得到
取代,能得到(6)利用
 将
将 氧化成
氧化成 ,
, 被还原后的产物为
被还原后的产物为 。然后用
。然后用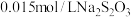 标准溶液滴定生成的
标准溶液滴定生成的 (已知:
(已知: )。若称取样品的质量为
)。若称取样品的质量为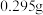 ,滴定
,滴定 时,达到终点消耗
时,达到终点消耗 标准溶液的平均体积为
标准溶液的平均体积为 。该样品中钴元素的质量分数为
。该样品中钴元素的质量分数为
您最近一年使用:0次
名校
3 . 硫酸四氨合铜晶体([Cu(NH3)4]SO4·H2O)常在工业上用途广泛。常温下该物质在空气中不稳定,受热时易发生分解。某小组拟合成硫酸四氨合铜晶体并测定其纯度。
I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)A仪器的名称为_______ ,相比用铜与浓硫酸直接反应制备硫酸铜,上述方法的优点是_______ 。
II.晶体的制备:将上述制备的CuSO4溶液按如图所示进行操作:
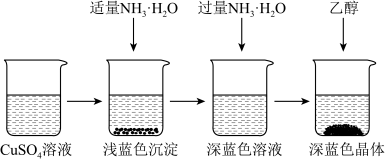
(2)已知浅蓝色沉淀的成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式_______ 。
(3)析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是_______ 。
III.氨含量的测定
精确称取wg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1mL0.5mol/L的盐酸标准溶液完全吸收。取下接收瓶,用0.5mol/LNaOH标准溶液滴定过剩的HCl(选用甲基橙作指示剂),到终点时消耗V2mLNaOH溶液。

(4)装置1中长玻璃管的作用_______ ,样品中氨的质量分数的表达式_______ 。
(5)下列实验操作可能使氨含量测定结果偏高的原因是_______。
I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)A仪器的名称为
II.晶体的制备:将上述制备的CuSO4溶液按如图所示进行操作:

(2)已知浅蓝色沉淀的成分为Cu2(OH)2SO4,试写出生成此沉淀的离子反应方程式
(3)析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是
III.氨含量的测定
精确称取wg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1mL0.5mol/L的盐酸标准溶液完全吸收。取下接收瓶,用0.5mol/LNaOH标准溶液滴定过剩的HCl(选用甲基橙作指示剂),到终点时消耗V2mLNaOH溶液。

(4)装置1中长玻璃管的作用
(5)下列实验操作可能使氨含量测定结果偏高的原因是_______。
| A.滴定时未用NaOH标准溶液润洗滴定管 |
| B.读数时,滴定前平视,滴定后俯视 |
| C.滴定过程中选用酚酞作指示剂 |
| D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁 |
您最近一年使用:0次
2023-01-20更新
|
344次组卷
|
2卷引用:重庆市西南大学附属中学校2022-2023学年高二上学期开学定时训练化学试题(广延班)
名校
解题方法
4 . 乳酸亚铁晶体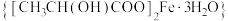 是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由
是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由 与乳酸(结构简式为:
与乳酸(结构简式为: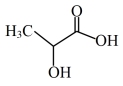 )反应制得。
)反应制得。
Ⅰ.制备

实验步骤如下:
ⅰ.检查气密性,按图示添加药品;
ⅱ.在装置B中制取硫酸亚铁,并将整个装置内的空气排净;
ⅲ.将B中溶液导入C中产生 沉淀;
沉淀;
ⅳ.将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)装置D的作用是_______ 。
(2)装置C中生成 的离子方程式是
的离子方程式是_______ 。
(3)步骤ⅱ和步骤ⅲ中应打开的开关分别是_______ (选填“ 和
和 ”或“
”或“ 和
和 ”)
”)
Ⅱ.制备乳酸亚铁晶体
将制得的 加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
(4)加入乙醇的目的是_______ 。
Ⅲ.探究乳酸亚铁晶体中铁元素的含量
乙同学称取g样品溶于水,用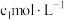 的酸性
的酸性 标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。
标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。
(5)乙同学方案是否正确?_______ (选填“是”或“否”),如填“是”,计算铁元素的质量分数(用含有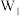 、
、 、
、 的代数式表示);如填“否”,说明偏高还是偏低,并写出理由
的代数式表示);如填“否”,说明偏高还是偏低,并写出理由_______ 。
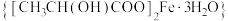 是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由
是一种很好的食品铁强化剂,吸收效果比无机铁好,易溶于水,几乎不溶于乙醇,可由 与乳酸(结构简式为:
与乳酸(结构简式为: )反应制得。
)反应制得。Ⅰ.制备


实验步骤如下:
ⅰ.检查气密性,按图示添加药品;
ⅱ.在装置B中制取硫酸亚铁,并将整个装置内的空气排净;
ⅲ.将B中溶液导入C中产生
 沉淀;
沉淀;ⅳ.将C中混合物分离提纯,获得纯净的碳酸亚铁产品。
(1)装置D的作用是
(2)装置C中生成
 的离子方程式是
的离子方程式是(3)步骤ⅱ和步骤ⅲ中应打开的开关分别是
 和
和 ”或“
”或“ 和
和 ”)
”) Ⅱ.制备乳酸亚铁晶体
将制得的
 加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。
加入到乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸。冷却,加入乙醇,过滤,再洗涤和干燥,得到产品。(4)加入乙醇的目的是
Ⅲ.探究乳酸亚铁晶体中铁元素的含量
乙同学称取g样品溶于水,用
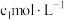 的酸性
的酸性 标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。
标准溶液滴定,当溶液恰好显浅红色,且30s内浅红色不褪去,停止滴定,测得消耗标准溶液V1mL。(5)乙同学方案是否正确?
 、
、 、
、 的代数式表示);如填“否”,说明偏高还是偏低,并写出理由
的代数式表示);如填“否”,说明偏高还是偏低,并写出理由
您最近一年使用:0次
2022-09-11更新
|
365次组卷
|
5卷引用:重庆八中2022-2023学年高三上学期入学考试化学试题
名校
5 . 现有mg含有Na2O杂质的Na2O2样品,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
(1)装置A中反应的离子方程式为_____ ;其中CaCO3属于____ (填“酸”“碱”或“盐”)。
(2)图中有一处明显错误,请指出并改正:_____ 。
(3)装置B的作用是____ ;装置D的作用是_____ ;若无装置D,样品中杂质的质量分数____ (填“偏高”“偏低”或“无影响”)。
(4)写出装置C中Na2O2和CO2反应的化学方程式:_____ 。
(5)实验结束后,装置F中水的体积为VmL,已知氧气的密度为1.43g·L-1,样品的质量分数为____ (用含m、V的代数式表示,列出计算式即可)。

(1)装置A中反应的离子方程式为
(2)图中有一处明显错误,请指出并改正:
(3)装置B的作用是
(4)写出装置C中Na2O2和CO2反应的化学方程式:
(5)实验结束后,装置F中水的体积为VmL,已知氧气的密度为1.43g·L-1,样品的质量分数为
您最近一年使用:0次
2022-09-13更新
|
556次组卷
|
3卷引用:重庆两江新区西南大学附属中学校2023-2024学年高一下学期开学检测化学试题
6 . 高纯MnCO3在电子工业中有重要的应用,工业上利用软锰矿(主要成分是MnO2,还含有Fe2O3、CaCO3、CuO等杂质)制取碳酸锰的流程如图所示:
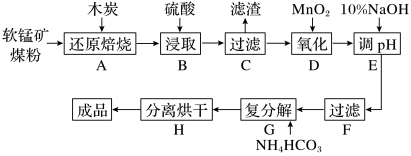
已知:还原焙烧主反应为2MnO2+C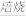 2MnO+CO2↑。
2MnO+CO2↑。
可能用到的数据如下:
根据要求回答下列问题:
(1)在实验室进行步骤A,混合物应放在__________ 中加热;步骤C中的滤渣为__________ 。
(2)步骤D中氧化剂与还原剂的物质的量之比为__________ 。
(3)步骤E中调节pH的范围为__________ ,其目的是__________ 。
(4)步骤G,温度控制在35℃以下的原因是__________ ,若Mn2+恰好沉淀完全时测得溶液中 的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=
的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=__________ 。
(5)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否干净的方法是__________ 。
(6)现用滴定法测定产品中锰元素的含量。实验步骤:称取3.300g试样,向其中加入稍过量的磷酸和硝酸,加热使产品中MnCO3完全转化为[Mn(PO4)2]3-(其中 完全转化为
完全转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应 +
+ =N2↑+2H2O以除去
=N2↑+2H2O以除去 ;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2
;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 ;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程为__________ 。
②试样中锰元素的质量分数为__________ 。

已知:还原焙烧主反应为2MnO2+C
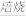 2MnO+CO2↑。
2MnO+CO2↑。可能用到的数据如下:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 1.5 | 6.5 | 4.2 | 8.1 |
| 沉淀完全pH | 3.7 | 9.7 | 7.4 | 10.1 |
(1)在实验室进行步骤A,混合物应放在
(2)步骤D中氧化剂与还原剂的物质的量之比为
(3)步骤E中调节pH的范围为
(4)步骤G,温度控制在35℃以下的原因是
 的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=
的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=(5)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否干净的方法是
(6)现用滴定法测定产品中锰元素的含量。实验步骤:称取3.300g试样,向其中加入稍过量的磷酸和硝酸,加热使产品中MnCO3完全转化为[Mn(PO4)2]3-(其中
 完全转化为
完全转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应 +
+ =N2↑+2H2O以除去
=N2↑+2H2O以除去 ;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2
;加入稀硫酸酸化,再加入60.00mL0.500mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2 ;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用5.00mL0.500mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。①酸性K2Cr2O7溶液与Fe2+反应的离子方程为
②试样中锰元素的质量分数为
您最近一年使用:0次
2020-06-24更新
|
98次组卷
|
4卷引用:重庆市乌江新高考协作体2023-2024学年高一下学期开学化学试题
重庆市乌江新高考协作体2023-2024学年高一下学期开学化学试题江西省重点中学盟校2020届高三下学期第一次联考理综化学试题安徽省泗县第一中学2019-2020学年高二下学期第四次月考化学试题(已下线)专题15 工艺流程题-2020年高考真题和模拟题化学分项汇编
名校
解题方法
7 . 硫化铋在光电、催化及储能方面有着广泛应用,还可用作新型锂离子电池的电极材料。以浮选过的辉铋矿(主要成分是Bi2S3,还含少量Fe2O3、SiO2等杂质)为原料制备高纯 Bi2S3的工艺流程如下:

已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)为了提高“浸出”的速率和效率,可以采取的措施有:___________ (请写出2条合理的措施)。
(2)滤渣1的主要成分是S和___________ 。“浸出”时加入盐酸,既可提高铋的浸出率,又可___________ ;
(3)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:___________ 。
(4)“还原”过程中过量的铁粉可用___________ 除去。
(5)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是___________ 。
(6)已知辉铋矿在转化过程中铋元素有10%的损耗,一吨某种辉铋矿可以制得高纯 Bi2S3的771kg,则该辉铋矿中铋元素的质量分数为___________ 。

已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)为了提高“浸出”的速率和效率,可以采取的措施有:
(2)滤渣1的主要成分是S和
(3)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:
(4)“还原”过程中过量的铁粉可用
(5)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是
(6)已知辉铋矿在转化过程中铋元素有10%的损耗,一吨某种辉铋矿可以制得高纯 Bi2S3的771kg,则该辉铋矿中铋元素的质量分数为
您最近一年使用:0次
2022-02-16更新
|
149次组卷
|
2卷引用:重庆市西北狼教育联盟2021–2022学年高三上学期开学质量检测化学试题
8 . 疫情防控中,含氯消毒剂发挥了重要作用。含氯消毒剂有多种,如 、
、 、
、 、
、 、
、 。某化学兴趣小组利用
。某化学兴趣小组利用 溶液来制备含氯消毒剂。
溶液来制备含氯消毒剂。
I.配制一定物质的量浓度的 溶液
溶液
(1)配制 溶液,需用托盘天平称取
溶液,需用托盘天平称取______ 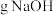 固体。
固体。
(2)配制上述溶液,除用到量筒、烧杯、玻璃棒外,还需要的玻璃仪器是__________ 。
(3)若向容量瓶加水定容时眼睛仰视液面,会造成所配溶液浓度__________ (“偏高”、“偏低”或“不变”)。
II.制备“84”消毒液

(4)仪器A的名称为__________ 。
(5)装置①中二氧化锰和浓盐酸反应制取氯气的化学方程式为__________ 。
(6)装置②中盛装的试剂为__________ ,用于除去 中的
中的 杂质。
杂质。
(7)装置③中制得“84”消毒液,其有效成分是__________ (填化学式)。
(8)清洗卫生间时,“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,用离子方程式解释其原因为__________ 。
(9)含氯消毒剂中有效氯含量,能反映含氯消毒剂消毒能力的大小,其定义是每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。则 的有效氯含量为
的有效氯含量为__________ (保留小数点后两位)。
 、
、 、
、 、
、 、
、 。某化学兴趣小组利用
。某化学兴趣小组利用 溶液来制备含氯消毒剂。
溶液来制备含氯消毒剂。I.配制一定物质的量浓度的
 溶液
溶液(1)配制
 溶液,需用托盘天平称取
溶液,需用托盘天平称取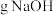 固体。
固体。(2)配制上述溶液,除用到量筒、烧杯、玻璃棒外,还需要的玻璃仪器是
(3)若向容量瓶加水定容时眼睛仰视液面,会造成所配溶液浓度
II.制备“84”消毒液

(4)仪器A的名称为
(5)装置①中二氧化锰和浓盐酸反应制取氯气的化学方程式为
(6)装置②中盛装的试剂为
 中的
中的 杂质。
杂质。(7)装置③中制得“84”消毒液,其有效成分是
(8)清洗卫生间时,“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,用离子方程式解释其原因为
(9)含氯消毒剂中有效氯含量,能反映含氯消毒剂消毒能力的大小,其定义是每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。则
 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
名校
解题方法
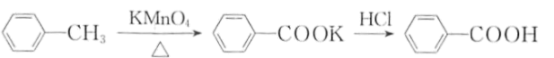
9 . 苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:

苯甲酸在水中的溶解度如表:
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在b中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取m g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶中,滴加2~3滴酚酞,然后用标准浓度的KOH溶液滴定。
请回答下列问题:
(1)装置b的名称是__________________ ,装置a的作用为_____________________________ 。
(2)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐、无色气体和黑色固体生成。加入草酸的作用是_________________________ ,请用离子方程式表示反应的原理______________________________ 。
(3)产品减压过滤时用冷水洗涤的原因是__________________________________________ 。
(4)选用下列__________ 操作,可以将粗产品进一步提纯。(选填字母)
A.溶于水后过滤 B.溶于乙醇后蒸馏 C.用甲苯萃取后分液 D.升华
(5)测定纯度步骤中,判断滴定终点的标志是________________________________________________ 。若m=1.200g,滴定时用去0.1200mol· L-1标准KOH溶液18.00mL,则所得产品中苯甲酸的质量分数为__________ (保留四位有效数字)。

| 名词 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 112.4(100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/g | 0.2 | 0.3 | 2.2 |

一、制备苯甲酸
在b中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
二、分离提纯
在反应混合物中加入一定量草酸(H2C2O4)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取m g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶中,滴加2~3滴酚酞,然后用标准浓度的KOH溶液滴定。
请回答下列问题:
(1)装置b的名称是
(2)分离提纯过程中加入的草酸是一种二元弱酸,反应过程中有酸式盐、无色气体和黑色固体生成。加入草酸的作用是
(3)产品减压过滤时用冷水洗涤的原因是
(4)选用下列
A.溶于水后过滤 B.溶于乙醇后蒸馏 C.用甲苯萃取后分液 D.升华
(5)测定纯度步骤中,判断滴定终点的标志是
您最近一年使用:0次
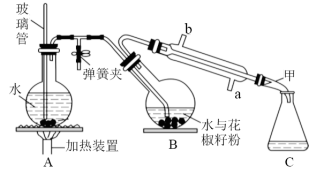
10 . 常用调味剂花椒油是一种从花椒籽中提取的挥发性香精油,高温易被氧化,易溶于乙瞇、乙 醇等有机溶剂。利用如图所示,水蒸气蒸馏装置处理花椒籽粉,经分离提纯得到花椒油。水蒸气蒸馏可以在较低的温度(略低于100度)下把沸点较高的不溶于水的液体蒸出。
实验步骤:
(一)在A装置中的圆底烧瓶中装入2/3容积的水,加1-2粒沸石。同时,在B中的圆底烧瓶中加入209g花椒籽粉和50mL水。
(二)加热A装置中的圆底烧瓶,当有大量蒸气产生时关闭弹簧夹,进行蒸馏。
(三)向馏出液中加入食盐至饱和,再用乙醚萃取,萃取后的醚层加入少量无水Na2SO4;将萃取后的有机层倾倒入蒸馏烧瓶中,蒸馏得花椒油。
(1)装置A中玻璃管的作用是_______ 。
(2)步骤(三)中,用50mL乙醚萃取的最佳方法是______ 。
A.直接用50 mL乙醚萃取分液
B.将溶液分两份,乙醚也分两份,分别萃取,萃取液合并
C.先用30 mL乙醚萃取分液,再分别用10 mL乙醚萃取两次,并将三次萃取液合并
(3)在馏出液中加入食盐的作用是___ ;加入无水Na2SO4的作用是_____ 。
(4)相比直接蒸馏,水蒸气蒸馏法的优点有______ 。
(5)为测定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加入80.00mL0.5mol/LNaOH的乙醇溶液,搅拌,充分反应,加水配成200mL溶液。取25.00mL所配溶液,加入_____ 做指示剂,用0.1mol/L盐酸进行滴定,滴定终点消耗盐酸20.00 mL。则该花椒油中含有油脂_____ g/L(以 计,式量:884)。
计,式量:884)。

实验步骤:
(一)在A装置中的圆底烧瓶中装入2/3容积的水,加1-2粒沸石。同时,在B中的圆底烧瓶中加入209g花椒籽粉和50mL水。
(二)加热A装置中的圆底烧瓶,当有大量蒸气产生时关闭弹簧夹,进行蒸馏。
(三)向馏出液中加入食盐至饱和,再用乙醚萃取,萃取后的醚层加入少量无水Na2SO4;将萃取后的有机层倾倒入蒸馏烧瓶中,蒸馏得花椒油。
(1)装置A中玻璃管的作用是
(2)步骤(三)中,用50mL乙醚萃取的最佳方法是
A.直接用50 mL乙醚萃取分液
B.将溶液分两份,乙醚也分两份,分别萃取,萃取液合并
C.先用30 mL乙醚萃取分液,再分别用10 mL乙醚萃取两次,并将三次萃取液合并
(3)在馏出液中加入食盐的作用是
(4)相比直接蒸馏,水蒸气蒸馏法的优点有
(5)为测定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加入80.00mL0.5mol/LNaOH的乙醇溶液,搅拌,充分反应,加水配成200mL溶液。取25.00mL所配溶液,加入
 计,式量:884)。
计,式量:884)。
您最近一年使用:0次
2019-09-15更新
|
228次组卷
|
2卷引用:重庆市第一中学2020届高三上学期摸底考试理科综合化学试题



