1 . 三氯化铬(CrCl3)在工业上主要用作媒染剂和催化剂,实验室模拟工业上以BaCrO4为原料制备CrCl3。
(1)制备CrCl3
取一定质量的BaCrO4和对应量的水加入到三预瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇(C2H5OH)充分反应,生成CrC13并放出CO2气体。
①上述反应的化学方程式为__________ 。
②上述反应中的乙醇与BaCrO4投料的物质的量比例大约为3:8,原因是__________ 。
(2)测定CrCl3的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为Cr2O ;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
Ⅲ.加入少量淀粉溶液,用0.0500mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次。平均消耗标准Na2S2O3溶液12.00mL。
已知反应: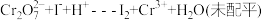 ;
;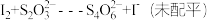
①滴定终点的现象是__________ 。
②计算CrC13的质量分数(写出计算过程,结果保留3位有效数字)__________
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有__________ (填字母)
A.碱式滴定管使用前,水洗后未用标准Na2S2O3溶液润洗
B.锥形瓶水洗后未干燥
C滴定终点读数时俯视读数
D.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(3)CrC13样品中C1-含量测定
实验室可用AgNO3标准溶液测定CrCl3样品中C1-的含量,请补充完成相应的实验步骤:准确量取25.00mL待测样品溶液于锥形瓶中,__________ ,进行数据处理。(终点反应为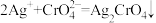 砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
(1)制备CrCl3
取一定质量的BaCrO4和对应量的水加入到三预瓶中,水浴加热并搅拌,一段时间后同时加入过量浓盐酸和无水乙醇(C2H5OH)充分反应,生成CrC13并放出CO2气体。
①上述反应的化学方程式为
②上述反应中的乙醇与BaCrO4投料的物质的量比例大约为3:8,原因是
(2)测定CrCl3的质量分数。
Ⅰ.称取样品0.3300g,加水溶解并配成250.0mL的溶液。
Ⅱ.移取25.00mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为Cr2O
 ;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。
;再加入过量KI固体,加塞揺匀。使铬元素完全以Cr3+的形式存在。Ⅲ.加入少量淀粉溶液,用0.0500mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次。平均消耗标准Na2S2O3溶液12.00mL。
已知反应:
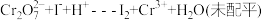 ;
;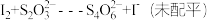
①滴定终点的现象是
②计算CrC13的质量分数(写出计算过程,结果保留3位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有
A.碱式滴定管使用前,水洗后未用标准Na2S2O3溶液润洗
B.锥形瓶水洗后未干燥
C滴定终点读数时俯视读数
D.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(3)CrC13样品中C1-含量测定
实验室可用AgNO3标准溶液测定CrCl3样品中C1-的含量,请补充完成相应的实验步骤:准确量取25.00mL待测样品溶液于锥形瓶中,
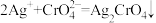 砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
砖红色)。实验中须使用的试剂有:K2CO3溶液、AgNO3标准溶液:除常用仪器外须使用的仪器有:棕色酸式滴定管)
您最近一年使用:0次
2 . Na2CO3、NaHCO3和NaCl都是重要的无机化工原料。
(1)以NaCl和NH4HCO3为原料制备Na2CO3,并测定产品中少量NaHCO3的含量,过程如下:
Ⅰ.Na2CO3的制备

Ⅱ.产品中NaHCO3含量的测定
步骤1 称取产品2.500g;溶解,配成250mL溶液。
步骤2 取25.00mL上述溶液,向其中滴入0.1000mol/L盐酸至22.45mL时,溶液中 恰好完全转化为
恰好完全转化为 。
。
步骤3 向步骤 2中溶液继续滴入0.1000mol/L盐酸,又消耗盐酸23.45mL时,溶液中 恰好完全转化为CO2。
恰好完全转化为CO2。
有关盐的溶解度曲线如图所示。
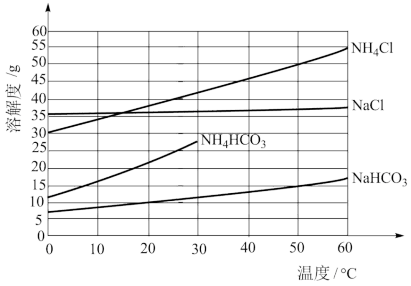
①Ⅰ中“反应”的化学方程式为_______ 。
②题图中碳酸氢铵溶解度在 后无数据的原因可能是
后无数据的原因可能是_______ 。
③“滤液”中除了Na+外,还含有一种阳离子,检验该阳离子的实验方法是_______ 。
④产品中NaHCO3的质量分数为_______ 。
(2)精制氯化钠可由海水晒制的粗盐(含有少量Ca2+、Mg2+、 等杂质离子)获得。请补充完整由粗盐获得精制氯化钠的实验方案:将粗盐加水溶解,
等杂质离子)获得。请补充完整由粗盐获得精制氯化钠的实验方案:将粗盐加水溶解,_______ ,蒸发结晶,得到精制氯化钠(实验中须用 的用品:饱和Na2CO3溶液、NaOH溶液、BaCl2溶液、盐酸、pH试纸)。
(1)以NaCl和NH4HCO3为原料制备Na2CO3,并测定产品中少量NaHCO3的含量,过程如下:
Ⅰ.Na2CO3的制备

Ⅱ.产品中NaHCO3含量的测定
步骤1 称取产品2.500g;溶解,配成250mL溶液。
步骤2 取25.00mL上述溶液,向其中滴入0.1000mol/L盐酸至22.45mL时,溶液中
 恰好完全转化为
恰好完全转化为 。
。步骤3 向步骤 2中溶液继续滴入0.1000mol/L盐酸,又消耗盐酸23.45mL时,溶液中
 恰好完全转化为CO2。
恰好完全转化为CO2。有关盐的溶解度曲线如图所示。

①Ⅰ中“反应”的化学方程式为
②题图中碳酸氢铵溶解度在
 后无数据的原因可能是
后无数据的原因可能是③“滤液”中除了Na+外,还含有一种阳离子,检验该阳离子的实验方法是
④产品中NaHCO3的质量分数为
(2)精制氯化钠可由海水晒制的粗盐(含有少量Ca2+、Mg2+、
 等杂质离子)获得。请补充完整由粗盐获得精制氯化钠的实验方案:将粗盐加水溶解,
等杂质离子)获得。请补充完整由粗盐获得精制氯化钠的实验方案:将粗盐加水溶解,
您最近一年使用:0次
名校
解题方法
3 . 透明铁黄(FeOOH)是一种分散性良好的铁系颜料。工业上采用硫铁矿熔烧去硫后烧渣(主要成分为 、FeO、
、FeO、 、
、 、不考虑其他杂质)制备透明铁黄工艺流程如下:
、不考虑其他杂质)制备透明铁黄工艺流程如下:
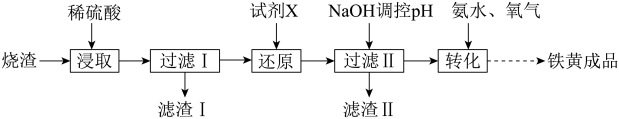
(1)浸取液中 的核外电子排布式为
的核外电子排布式为_______ 。
(2)“过滤I”后,滤液中所含金属阳离子有_______ 。
(3)“还原”时,试剂X若选用铁粉,则该反应的离子方程式为_______ 。
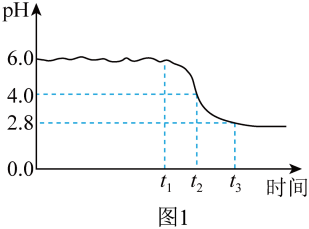
(4)制备铁黄:向一定浓度 溶液中加入氨水,当滴加氨水至pH为6.0时,停止滴加氨水,开始通氧气,生成铁黄。通入氧气过程中,记录溶液pH变化如图1所示。
溶液中加入氨水,当滴加氨水至pH为6.0时,停止滴加氨水,开始通氧气,生成铁黄。通入氧气过程中,记录溶液pH变化如图1所示。
已知:25℃时, 完全沉淀(离子浓度
完全沉淀(离子浓度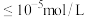 )的
)的 。
。
①滴加氨水产生沉淀,当pH为6.0时,溶液中残留 浓度为
浓度为_______ mol/L。
②请写出0~ 时段发生的化学方程式
时段发生的化学方程式_______ ; ~
~ 时段,溶液pH明显降低,请解释原因:
时段,溶液pH明显降低,请解释原因:_______ 。
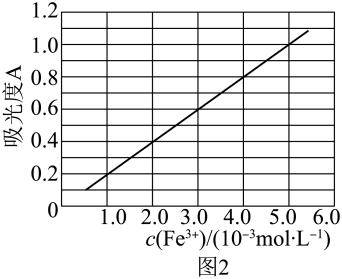
(5)制得的透明铁黄中往往混有氧化铁,可用分光光度法测定透明铁黄的含量。已知 的吸光度A(对特定波长光的吸收程度)与
的吸光度A(对特定波长光的吸收程度)与 标准溶液浓度的关系如图-2所示。称取3.47g样品,用稀硫酸溶解并定容至1L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,计算样品中FeOOH的质量分数(写出主要计算过程)。
标准溶液浓度的关系如图-2所示。称取3.47g样品,用稀硫酸溶解并定容至1L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,计算样品中FeOOH的质量分数(写出主要计算过程)。_______
 、FeO、
、FeO、 、
、 、不考虑其他杂质)制备透明铁黄工艺流程如下:
、不考虑其他杂质)制备透明铁黄工艺流程如下:
(1)浸取液中
 的核外电子排布式为
的核外电子排布式为(2)“过滤I”后,滤液中所含金属阳离子有
(3)“还原”时,试剂X若选用铁粉,则该反应的离子方程式为
(4)制备铁黄:向一定浓度
 溶液中加入氨水,当滴加氨水至pH为6.0时,停止滴加氨水,开始通氧气,生成铁黄。通入氧气过程中,记录溶液pH变化如图1所示。
溶液中加入氨水,当滴加氨水至pH为6.0时,停止滴加氨水,开始通氧气,生成铁黄。通入氧气过程中,记录溶液pH变化如图1所示。
已知:25℃时,
 完全沉淀(离子浓度
完全沉淀(离子浓度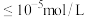 )的
)的 。
。①滴加氨水产生沉淀,当pH为6.0时,溶液中残留
 浓度为
浓度为②请写出0~
 时段发生的化学方程式
时段发生的化学方程式 ~
~ 时段,溶液pH明显降低,请解释原因:
时段,溶液pH明显降低,请解释原因:(5)制得的透明铁黄中往往混有氧化铁,可用分光光度法测定透明铁黄的含量。已知
 的吸光度A(对特定波长光的吸收程度)与
的吸光度A(对特定波长光的吸收程度)与 标准溶液浓度的关系如图-2所示。称取3.47g样品,用稀硫酸溶解并定容至1L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,计算样品中FeOOH的质量分数(写出主要计算过程)。
标准溶液浓度的关系如图-2所示。称取3.47g样品,用稀硫酸溶解并定容至1L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,计算样品中FeOOH的质量分数(写出主要计算过程)。
您最近一年使用:0次
2022-09-03更新
|
282次组卷
|
3卷引用:江苏省海安市2022-2023学年高三上学期期初学业质量监测化学试题
4 . 硫代硫酸钠晶体(Na2S2O3·5H2O)俗名“大苏打”。已知它易溶于水,难溶于乙醇,在中性或碱性环境中稳定,受热、遇酸易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:

(1)装置甲中,a仪器的名称是____________ ;a中盛有浓硫酸,b中盛有亚硫酸钠,实验中要控制SO2生成速率,可以采取的措施有_________________________ (写出一条即可)。
(2)装置乙的作用是____________________________________ 。
(3)装置丙中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2。反应的化学方程式为:________________________________________ 。
(4)本实验所用的Na2CO3中含少量NaOH,检验含有NaOH的实验方案为_________ 。(实验中供选用的试剂及仪器:CaCl2溶液、Ca(OH)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管.提示:室温时CaCO3饱和溶液的pH=9.5)
(5)反应结束后过滤丙中的混合物,滤液经蒸发、结晶、过滤、洗涤、干燥等得到产品,生成的硫代硫酸钠粗品可用_____________ 洗涤。为了测定粗产品中Na2S2O3·5H2O的含量,采用在酸性条件下用KMnO4标准液滴定的方法(假设粗产品中的杂质与酸性KMnO4溶液不反应)。称取1.50g粗产品溶于水,用0.20 mol·L-1KMnO4溶液(加适量稀硫酸酸化)滴定,当溶液中 全部被氧化为
全部被氧化为 时,消耗高锰酸钾溶液体积40.00mL。
时,消耗高锰酸钾溶液体积40.00mL。
①写出反应的离子方程式:________________________________________ 。
②产品中Na2S2O3·5H2O的质量分数为____________________ (保留小数点后一位)。

(1)装置甲中,a仪器的名称是
(2)装置乙的作用是
(3)装置丙中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2。反应的化学方程式为:
(4)本实验所用的Na2CO3中含少量NaOH,检验含有NaOH的实验方案为
(5)反应结束后过滤丙中的混合物,滤液经蒸发、结晶、过滤、洗涤、干燥等得到产品,生成的硫代硫酸钠粗品可用
 全部被氧化为
全部被氧化为 时,消耗高锰酸钾溶液体积40.00mL。
时,消耗高锰酸钾溶液体积40.00mL。①写出反应的离子方程式:
②产品中Na2S2O3·5H2O的质量分数为
您最近一年使用:0次
2020-04-02更新
|
512次组卷
|
4卷引用:江苏省昆山市周市高级中学2021-2022学年高三上学期暑期自主学习测试化学试题
10-11高三·江苏泰州·开学考试
5 . 硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%)。某同学设计了如下方案,分离样品中各种金属元素。请回答下列问题。

(1)写出溶液B的溶质是____________ 。
(2)参照以下框的形式进一步完成“溶液C”到“Al2O3”的流程(注明试剂、条件和操作)____________ 。

(3)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成 Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①判断到达滴定终点的现象是____________ 。
②某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移到25.00mL试样溶液,用0.0050mol·L-1KMnO4标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是_______________ 。

(1)写出溶液B的溶质是
(2)参照以下框的形式进一步完成“溶液C”到“Al2O3”的流程(注明试剂、条件和操作)

(3)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成 Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①判断到达滴定终点的现象是
②某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移到25.00mL试样溶液,用0.0050mol·L-1KMnO4标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是
您最近一年使用:0次
名校
6 . 氧化钴常用作超耐热合金和磁性材料及化学工业的催化剂。一种以 -萘酚钴渣(含有
-萘酚钴渣(含有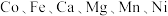 等元素的化合物及
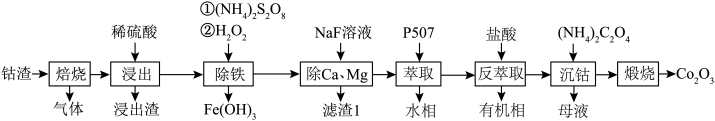
等元素的化合物及 )制备氧化钴的工艺流程如下。
)制备氧化钴的工艺流程如下。
已知:① -萘酚钴渣焙烧浸出后溶液中金属元素主要以
-萘酚钴渣焙烧浸出后溶液中金属元素主要以 价离子形式存在。
价离子形式存在。
②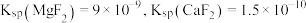 ;
;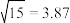 。
。
③溶液的氧化还原电势(E)为正,表示该溶液显示出一定的氧化性。氧化还原电势越高,氧化性越强;电势越低,氧化性越弱。
回答下列问题:
(1)“焙烧”过程中的主要气体产物为___________ (填化学式)。
(2)“除铁”过程中, 参与反应的离子方程式为
参与反应的离子方程式为___________ 。
(3)“除铁”后滤液中 浓度分别为
浓度分别为 和
和 ,若取
,若取 该废液,则至少需加入
该废液,则至少需加入___________ 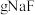 才能使该废液中
才能使该废液中 沉淀完全(当离子浓度
沉淀完全(当离子浓度 可认为沉淀完全)。
可认为沉淀完全)。
(4)用萃取剂P507“萃取”后所得水相中主要含有的金属离子为___________ (填离子符号)。“煅烧”时主要反应的化学方程式为___________ 。
(5)钴元素的存在形式的稳定区域与溶液 的关系如图(
的关系如图(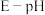 图)所示,在溶液
图)所示,在溶液 时,
时, 能将
能将 氧化,写出该反应的离子方程式:
氧化,写出该反应的离子方程式:___________ ;以1吨 -萘酚钴渣(
-萘酚钴渣( 的质量分数为
的质量分数为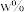 )为原料提取出
)为原料提取出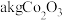 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为___________  (填含
(填含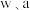 的表达式)。
的表达式)。
 -萘酚钴渣(含有
-萘酚钴渣(含有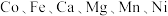 等元素的化合物及
等元素的化合物及 )制备氧化钴的工艺流程如下。
)制备氧化钴的工艺流程如下。
已知:①
 -萘酚钴渣焙烧浸出后溶液中金属元素主要以
-萘酚钴渣焙烧浸出后溶液中金属元素主要以 价离子形式存在。
价离子形式存在。②
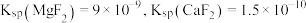 ;
;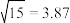 。
。③溶液的氧化还原电势(E)为正,表示该溶液显示出一定的氧化性。氧化还原电势越高,氧化性越强;电势越低,氧化性越弱。
回答下列问题:
(1)“焙烧”过程中的主要气体产物为
(2)“除铁”过程中,
 参与反应的离子方程式为
参与反应的离子方程式为(3)“除铁”后滤液中
 浓度分别为
浓度分别为 和
和 ,若取
,若取 该废液,则至少需加入
该废液,则至少需加入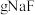 才能使该废液中
才能使该废液中 沉淀完全(当离子浓度
沉淀完全(当离子浓度 可认为沉淀完全)。
可认为沉淀完全)。(4)用萃取剂P507“萃取”后所得水相中主要含有的金属离子为
(5)钴元素的存在形式的稳定区域与溶液
 的关系如图(
的关系如图(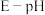 图)所示,在溶液
图)所示,在溶液 时,
时, 能将
能将 氧化,写出该反应的离子方程式:
氧化,写出该反应的离子方程式: -萘酚钴渣(
-萘酚钴渣( 的质量分数为
的质量分数为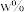 )为原料提取出
)为原料提取出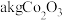 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为 (填含
(填含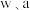 的表达式)。
的表达式)。
您最近一年使用:0次
2023-10-04更新
|
186次组卷
|
3卷引用:江苏省百师联盟2023-2024学年高三上学期开学摸底联考化学试题
7 . 纳米铁粉常用于废水处理,以草酸(H2C2O4)与FeSO4为原料可制取纳米铁粉。
I.制取草酸
用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液氧化淀粉水解液制备草酸,其装置如下图所示。
【已知:硝酸氧化淀粉水解液过程中主要反应: (未配平)】
(未配平)】

(1)仪器甲的名称为___________ 。
(2)装置B的作用___________ 。
(3)控制反应温度不超过60℃可以防止有机物脱水炭化和___________ 。
Ⅱ.制备纳米铁粉,其流程如下:

已知:H2C2O4为二元弱酸。
(4)检验酸溶后的溶液是否含Fe3+的试剂是___________ 。
(5)向酸溶后的溶液中滴加稍过量的H2C2O4,过滤得FeC2O4·H2O。
①沉淀反应的离子方程式为___________ 。
②过滤所得沉淀中FeC2O4·H2O含量的测定:准确称取5.800g沉淀,加入适量的蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol·L-1KMnO4溶液,完全反应时,消耗KMnO4溶液18.00mL。过程中发生的反应为: (假设杂质不参与反应)。计算沉淀中FeC2O4·2H2O(相对分子质量为180)的质量分数
(假设杂质不参与反应)。计算沉淀中FeC2O4·2H2O(相对分子质量为180)的质量分数___________ (写出计算过程)。
I.制取草酸
用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液氧化淀粉水解液制备草酸,其装置如下图所示。
【已知:硝酸氧化淀粉水解液过程中主要反应:
 (未配平)】
(未配平)】
(1)仪器甲的名称为
(2)装置B的作用
(3)控制反应温度不超过60℃可以防止有机物脱水炭化和
Ⅱ.制备纳米铁粉,其流程如下:

已知:H2C2O4为二元弱酸。
(4)检验酸溶后的溶液是否含Fe3+的试剂是
(5)向酸溶后的溶液中滴加稍过量的H2C2O4,过滤得FeC2O4·H2O。
①沉淀反应的离子方程式为
②过滤所得沉淀中FeC2O4·H2O含量的测定:准确称取5.800g沉淀,加入适量的蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol·L-1KMnO4溶液,完全反应时,消耗KMnO4溶液18.00mL。过程中发生的反应为:
 (假设杂质不参与反应)。计算沉淀中FeC2O4·2H2O(相对分子质量为180)的质量分数
(假设杂质不参与反应)。计算沉淀中FeC2O4·2H2O(相对分子质量为180)的质量分数
您最近一年使用:0次
名校
解题方法
8 .  和ZnO都是常用的化学添加剂,一种以含锌废液(主要含有
和ZnO都是常用的化学添加剂,一种以含锌废液(主要含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 )为原料,制备
)为原料,制备 和ZnO的工艺流程如下:
和ZnO的工艺流程如下:

已知:常温下, 、
、 ,
, 、
、 开始沉淀至完全沉淀时的pH分别为2.7~3.7、4.2~5.1、5.4~6.7、6.2~8.0。回答下列问题:
开始沉淀至完全沉淀时的pH分别为2.7~3.7、4.2~5.1、5.4~6.7、6.2~8.0。回答下列问题:
(1) 的价电子排布式为
的价电子排布式为___________ 。
(2)加入试剂 氧化的目的是
氧化的目的是___________ (用离子方程式表示)。检验滤液Ⅲ中含量最高的阳离子的实验方法为___________ 。
(3)调节pH值时,pH值至少为___________ ;物质b为___________ (用化学式表示)。
(4)已知:室温下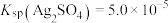 ,
, 。滤液Ⅱ中加入
。滤液Ⅱ中加入 的目的是为了除去
的目的是为了除去 ,发生的反应为
,发生的反应为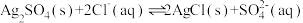 ,室温下该反应的平衡常数K=
,室温下该反应的平衡常数K=___________ 。
(5)“沉锌”在一定条件下进行,生成碱式碳酸锌[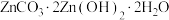 ]沉淀和一种气体,写出该反应的化学方程式:
]沉淀和一种气体,写出该反应的化学方程式:___________ 。
 和ZnO都是常用的化学添加剂,一种以含锌废液(主要含有
和ZnO都是常用的化学添加剂,一种以含锌废液(主要含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 )为原料,制备
)为原料,制备 和ZnO的工艺流程如下:
和ZnO的工艺流程如下:
已知:常温下,
 、
、 ,
, 、
、 开始沉淀至完全沉淀时的pH分别为2.7~3.7、4.2~5.1、5.4~6.7、6.2~8.0。回答下列问题:
开始沉淀至完全沉淀时的pH分别为2.7~3.7、4.2~5.1、5.4~6.7、6.2~8.0。回答下列问题:(1)
 的价电子排布式为
的价电子排布式为(2)加入试剂
 氧化的目的是
氧化的目的是(3)调节pH值时,pH值至少为
(4)已知:室温下
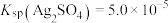 ,
, 。滤液Ⅱ中加入
。滤液Ⅱ中加入 的目的是为了除去
的目的是为了除去 ,发生的反应为
,发生的反应为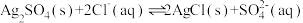 ,室温下该反应的平衡常数K=
,室温下该反应的平衡常数K=(5)“沉锌”在一定条件下进行,生成碱式碳酸锌[
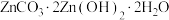 ]沉淀和一种气体,写出该反应的化学方程式:
]沉淀和一种气体,写出该反应的化学方程式:
您最近一年使用:0次
2024-02-29更新
|
208次组卷
|
2卷引用:江苏省建湖高级中学2023-2024学年高二下学期期初测试(2月)化学试题
名校
9 . 葡萄糖酸亚铁 是常用的补铁剂,一种制备流程如图:
是常用的补铁剂,一种制备流程如图: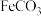 的制取。如图所示,向装置甲中滴加稀盐酸,产生气体经洗气后通入装置丙中的
的制取。如图所示,向装置甲中滴加稀盐酸,产生气体经洗气后通入装置丙中的 溶液
溶液 ,当溶液的
,当溶液的 约为7时,滴入
约为7时,滴入 溶液,生成
溶液,生成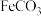 沉淀。
沉淀。_______ 溶液(填化学式)。
②写出装置丙中生成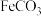 的主要离子方程式:
的主要离子方程式:_______ 。
(2)葡萄糖氧化为葡萄糖酸。
取一定量葡萄糖,加入蒸馏水至完全溶解,加入少量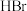 和稍过量
和稍过量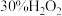 ,充分反应,加热煮沸,将产生的气体用
,充分反应,加热煮沸,将产生的气体用 溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。
溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。
①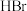 催化
催化 氧化法分两步进行,过程如下:
氧化法分两步进行,过程如下:
第一步:_______
第二步:
写出第一步反应的化学方程式:_______ 。
②加热煮沸的作用是_______ 。
(3)用酸性 溶液测定葡萄糖酸亚铁晶体中
溶液测定葡萄糖酸亚铁晶体中 含量,进而计算出晶体的纯度。
含量,进而计算出晶体的纯度。
①请补充完整测定葡萄糖酸亚铁晶体中 含量的实验方案:准确称取一定质量的葡萄糖酸亚铁晶体样品,用稀硫酸溶解,配制成
含量的实验方案:准确称取一定质量的葡萄糖酸亚铁晶体样品,用稀硫酸溶解,配制成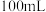 溶液,
溶液,_______ 。【须使用的仪器和药品:酸式滴定管(规格 ),锥形瓶,
),锥形瓶, 的
的 标准溶液】
标准溶液】
②发现纯度总是大于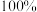 。若实验操作和计算均正确,其可能原因是
。若实验操作和计算均正确,其可能原因是_______ 。
 是常用的补铁剂,一种制备流程如图:
是常用的补铁剂,一种制备流程如图:
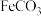 的制取。如图所示,向装置甲中滴加稀盐酸,产生气体经洗气后通入装置丙中的
的制取。如图所示,向装置甲中滴加稀盐酸,产生气体经洗气后通入装置丙中的 溶液
溶液 ,当溶液的
,当溶液的 约为7时,滴入
约为7时,滴入 溶液,生成
溶液,生成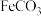 沉淀。
沉淀。
②写出装置丙中生成
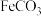 的主要离子方程式:
的主要离子方程式:(2)葡萄糖氧化为葡萄糖酸。
取一定量葡萄糖,加入蒸馏水至完全溶解,加入少量
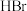 和稍过量
和稍过量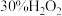 ,充分反应,加热煮沸,将产生的气体用
,充分反应,加热煮沸,将产生的气体用 溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。
溶液吸收,加入无水乙醇,静置,过滤,干燥,得纯净葡萄糖酸晶体。①
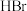 催化
催化 氧化法分两步进行,过程如下:
氧化法分两步进行,过程如下:第一步:_______
第二步:

写出第一步反应的化学方程式:
②加热煮沸的作用是
(3)用酸性
 溶液测定葡萄糖酸亚铁晶体中
溶液测定葡萄糖酸亚铁晶体中 含量,进而计算出晶体的纯度。
含量,进而计算出晶体的纯度。①请补充完整测定葡萄糖酸亚铁晶体中
 含量的实验方案:准确称取一定质量的葡萄糖酸亚铁晶体样品,用稀硫酸溶解,配制成
含量的实验方案:准确称取一定质量的葡萄糖酸亚铁晶体样品,用稀硫酸溶解,配制成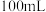 溶液,
溶液, ),锥形瓶,
),锥形瓶, 的
的 标准溶液】
标准溶液】②发现纯度总是大于
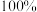 。若实验操作和计算均正确,其可能原因是
。若实验操作和计算均正确,其可能原因是
您最近一年使用:0次
10 . 在不同温度下, 可与
可与 、
、 或
或 以配位键形成多种配合物。
以配位键形成多种配合物。 是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下:
是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下: 溶液为指示剂,用
溶液为指示剂,用 溶液滴定可测定
溶液滴定可测定 溶液中氯离子的含量。
溶液中氯离子的含量。
① 中含有的
中含有的 键的数目为
键的数目为_______ 。
②反应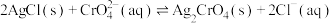 的平衡常数
的平衡常数
_______ 。(已知: ,
,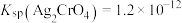 )
)
(2)“混合”反应物需降温到 以下,原因是
以下,原因是_______ 。
(3)制备 装置如图所示。加入催化剂活性炭加热至
装置如图所示。加入催化剂活性炭加热至 反应20min。
反应20min。_______ 。
②“转化”的化学方程式为_______ 。
(4)保持其它条件不变,改变反应温度, 的产率与温度变化如图所示。温度高于
的产率与温度变化如图所示。温度高于 时,
时, 产率下降的原因可能为
产率下降的原因可能为_______ 。 的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,
的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,_______ 。(实验中必须 使用的药品:浓盐酸、乙醇和水)
 可与
可与 、
、 或
或 以配位键形成多种配合物。
以配位键形成多种配合物。 是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下:
是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下: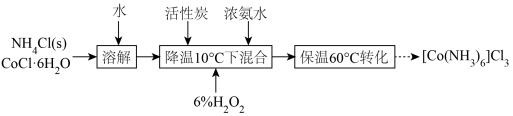
 溶液为指示剂,用
溶液为指示剂,用 溶液滴定可测定
溶液滴定可测定 溶液中氯离子的含量。
溶液中氯离子的含量。①
 中含有的
中含有的 键的数目为
键的数目为②反应
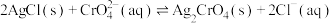 的平衡常数
的平衡常数
 ,
,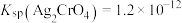 )
)(2)“混合”反应物需降温到
 以下,原因是
以下,原因是(3)制备
 装置如图所示。加入催化剂活性炭加热至
装置如图所示。加入催化剂活性炭加热至 反应20min。
反应20min。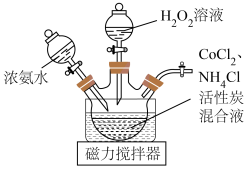
②“转化”的化学方程式为
(4)保持其它条件不变,改变反应温度,
 的产率与温度变化如图所示。温度高于
的产率与温度变化如图所示。温度高于 时,
时, 产率下降的原因可能为
产率下降的原因可能为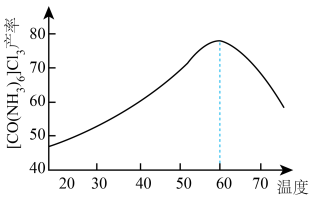
 的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,
的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,
您最近一年使用:0次



