名校
解题方法
1 . 亚硝酰氯NOCl常用于合成洗涤剂、触媒及用作中间体,其熔点为-64.5℃,沸点-5.5℃,遇水易水解为两种酸。某学习小组在实验室用Cl2与NO制备NOCl并测定其纯度,进行如图实验(部分夹持装置已略去)。

(1)实验室制取Cl2的离子方程式为____ 。
(2)仪器a的名称为____ ,装置C中长颈漏斗的作用是____ 。
(3)若不用装置D中的干燥管,对实验有何影响____ (用化学方程式表示)。
(4)N、O、Cl的简单氢化物的熔沸点由高到低的顺序是____ (用化学式表示)。
(5)通过以下实验测定NOCl样品的纯度。取D中所得液体100g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL于锥形瓶中,用cmol·L-1AgNO3标准溶液滴定,滴定终点时(只生成AgCl沉淀)消耗标准溶液的体积为20.00mL。则亚硝酰氯(NOCl)样品的纯度为____ 。

(1)实验室制取Cl2的离子方程式为
(2)仪器a的名称为
(3)若不用装置D中的干燥管,对实验有何影响
(4)N、O、Cl的简单氢化物的熔沸点由高到低的顺序是
(5)通过以下实验测定NOCl样品的纯度。取D中所得液体100g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL于锥形瓶中,用cmol·L-1AgNO3标准溶液滴定,滴定终点时(只生成AgCl沉淀)消耗标准溶液的体积为20.00mL。则亚硝酰氯(NOCl)样品的纯度为
您最近一年使用:0次
2022-07-29更新
|
69次组卷
|
2卷引用:甘肃省张掖市高台县第一中学2022-2023学年高二上学期开校检测化学试题
名校
解题方法
2 . 镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:

回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是_______ 。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入盛有_______ 溶液的烧杯中,充分搅拌后经_______ 、_______ (填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:

其中装置A的作用是_______ 。
(4)写出过程④中发生反应的化学方程式:_______ 。
(5)工业制造镁粉是将镁蒸气在气体中冷却,下列①Ar,②空气,③CO2,④N2,可作为冷却气的是_______ 。

回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入盛有
(3)下图是该兴趣小组设计进行过程③的实验装置图:

其中装置A的作用是
(4)写出过程④中发生反应的化学方程式:
(5)工业制造镁粉是将镁蒸气在气体中冷却,下列①Ar,②空气,③CO2,④N2,可作为冷却气的是
您最近一年使用:0次
2022-04-11更新
|
252次组卷
|
2卷引用:甘肃省临洮中学2023-2024学年上学期高二下学期开学考试化学试题
名校
3 . 碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。
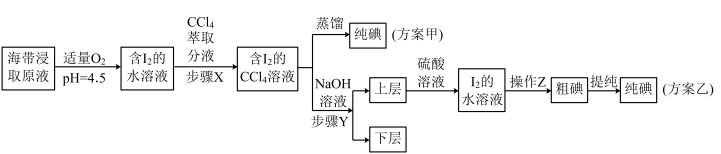
已知:3I2+6NaOH===5NaI+NaIO3+3H2O。
请回答下列问题:
(1)分液漏斗使用前需要检漏,检漏方法为__________ 。
(2)步骤X中,萃取后分液漏斗内观察到的现象是_____________ 。
(3)下列有关步骤Y的说法中正确的是_____ (填字母)。
A.应控制NaOH溶液的浓度和体积
B.将碘单质转化成碘离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以用乙醇代替
(4)向“上层”中加入H2SO4溶液,发生反应的化学方程式为____ ,操作Z的名称为________ 。
(5)方案甲中采用蒸馏不合理,理由是________ 。

已知:3I2+6NaOH===5NaI+NaIO3+3H2O。
请回答下列问题:
(1)分液漏斗使用前需要检漏,检漏方法为
(2)步骤X中,萃取后分液漏斗内观察到的现象是
(3)下列有关步骤Y的说法中正确的是
A.应控制NaOH溶液的浓度和体积
B.将碘单质转化成碘离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以用乙醇代替
(4)向“上层”中加入H2SO4溶液,发生反应的化学方程式为
(5)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次
2019-09-16更新
|
631次组卷
|
9卷引用:甘肃省武威市民勤县第一中学2023-2024学年高二上学期开学考试化学试题
甘肃省武威市民勤县第一中学2023-2024学年高二上学期开学考试化学试题云南省玉溪元江民中2019-2020学年高二开学考试化学试题云南省元阳县第一中学2019-2020学年高二上学期开学考试化学试题云南省南华县一中2019-2020学年高二上学期开学考试化学试题人教版高中化学必修二第四章《化学与自然资源的开发利用》测试卷2020年春季人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷第八章 化学与可持续发展 综合拓展——B拓展区 夯实基础(人教版(2019)第二册)第四章 化学与自然资源的开发利用 综合拓展——B拓展区 夯实基础(人教版必修2)必修第二册RJ第八章 B拓展区 综合拓展
4 . 实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
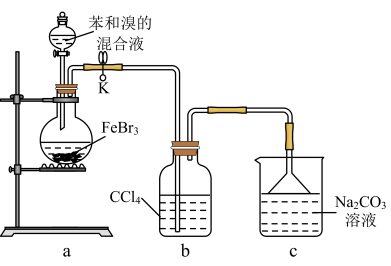
| A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K |
| B.实验中装置b中的液体逐渐变为浅红色 |
| C.装置c中的碳酸钠溶液的作用是吸收溴化氢 |
| D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯 |
您最近一年使用:0次
2019-06-09更新
|
28054次组卷
|
126卷引用:甘肃省天水一中2020-2021学年高二上学期开学考试化学(理科)试题
甘肃省天水一中2020-2021学年高二上学期开学考试化学(理科)试题安徽省黄山市屯溪第一中学2019-2020学年高二上学期入学摸底考试化学试题河北省沧州市盐山县盐山中学2019-2020学年高二下学期开学考试化学试题湖南省株洲市茶陵县第一中学2020-2021学年高二年上学期入学考试化学试题甘肃省武威市民勤县第一中学2019-2020学年高二下学期第二次月考化学(理)试题湖南省长沙市第一中学2020-2021学年高二下学期开学考化学试题天津市第一中学2018-2019学年高二下学期期末考试化学试题河北省张家口市第四中学2018-2019学年高二下学期6月月考理科综合化学试题 广西桂林市第十八中学2019-2020学年高二上学期期中考试化学(理)试题(已下线)【新东方】2020-63江西省宜春市奉新县第一中学2019-2020学年高二下学期第一次月考化学试题河北省邯郸市永年区第二中学2019-2020学年高二下学期6月考试化学试题广东省佛山市三水区三水中学2019-2020学年高二下学期第二次统考化学试题陕西省渭南市大荔县2019-2020学年高二下学期转段(期末)考试化学试题浙江省嘉兴市2019-2020学年高二下学期期末考试化学试题天津市耀华中学2019-2020学年高三上学期开学化学试卷河北省唐山市玉田县第一中学2019-2020学年高二第二次阶段性考试化学试题吉林省松原市油田第十一中学2020-2021学年高二上学期月考化学试题宁夏银川一中2020-2021学年高二上学期期中考试化学试题四川省蓬安县第二中学2020-2021学年高二12月月考化学试题江西省南昌市新建区第二中学2019-2020学年高二下学期期终考试化学试题江西省南昌市新建区第二中学2020-2021学年高二上学期“新星计划”体验营12月月考化学试题四川省南充市2020-2021学年高二上期期末考试化学试题高二选择性必修3(人教版2019)第二章 烃 第二章素养检测江西省南昌县莲塘第一中学2020-2021学年高二上学期期末检测化学试题(已下线)【浙江新东方】高中化学20210304-005广西南宁市第十中学2020-2021学年高二下学期3月月考化学试题新疆新源县第二中学2018-2019学年高二下学期期末考试化学试题山东省枣庄滕州市2020-2021学年高二下学期期中质量检测化学试题(已下线)【浙江新东方】【2021.4.27】【温州】【高二上】【高中化学】【00197】安徽省亳州市第二中学2020-2021学年高二下学期期中考试化学试题辽宁省六校协作体2020-2021学年高二下学期第三次联考化学试题陕西省咸阳百灵学校2020-2021学年高二下学期第二次月考化学试题陕西省黄陵中学2020-2021学年高二下学期期末考试化学试题广东省清远市凤霞中学2020-2021学年高二下学期期中质量检测化学试题吉林省白城市2020-2021学年高二下学期期末考试化学试题云南省曲靖市罗平县第二中学2019-2020学年高二上学期期末考试化学试题广州市培正中学2020-2021学年高二下学期期中考试化学试题陕西省长安区第一中学2021-2022学年高二上学期期中考试化学试题吉林省长春市实验中学2021-2022学年高二下学期4月月考化学试题黑龙江省黑河市嫩江市高级中学等部分学校2021-2022学年高二4月月考化学试题浙江省台州市三门启超中学等两校2021-2022学年高二下学期期中联考化学试题山西省长治市第二中学校2021-2022学年高二下学期期中考试化学试题河南省南阳市六校2021-2022学年高二下学期5月份联考化学试题山东省东营市河口区第一中学2021-2022学年高二下学期期中考试化学试题专题3 石油化工的基础物质——烃 第一~二单元综合拔高练第一~三节综合拔高练吉林省延边第二中学2022-2023学年高三上学期开学调研考试化学试题山东省临沂市沂南第一中学2021-2022学年高二下学期第三次检测化学试题四川省自贡市富顺县城关中学2021-2022学年高二下学期期中考试化学试题云南省弥勒市第一中学2022-2023学年高二上学期10月月考化学试题(已下线)【知识图鉴】单元讲练测选择性必修3第2单元03巩固练湖南省邵阳市第二中学2022-2023学年高二下学期期中考试化学试题第二章 烃(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修3)江西省上饶市民校考试联盟2022-2023学年高二下学期阶段测试(四)化学试题陕西省榆林市绥德中学2022-2023学年高二下学期第一次月考化学试题广东省汕头市金山中学2022-2023学年高二下学期期中考试化学试题湖北省沙市中学2022-2023学年高二下学期5月月考化学试题安徽省亳州市第二完全中学2022-2023学年高二下学期期末考试化学(A卷)试题云南省马关县第一中学校2022-2023学年高二下学期期末考试化学试题河南省开封高级中学2023-2024学年高三上学期第一次质量检测化学试题江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题河南省博爱县第一中学2023-2024学年高二上学期9月月考化学试题江苏省无锡市市北高级中学2023-2024学年高二上学期期中检测化学试题云南省大理州实验中学2021-2022学年高二上学期化学期中考试题安徽省阜阳一中2023-2024学年高二下学期4月月考化学试卷安徽省定远县育才学校2023-2024学年高二下学期期中化学试卷2019年全国统一考试化学试题(新课标Ⅰ)【全国百强校】河南省南阳市第一中学2018-2019学年高一下学期第五次月考化学试题(已下线)专题10.1 常见仪器使用和实验基本操作(讲)-《2020年高考一轮复习讲练测》(已下线)专题10.1 常见仪器使用和实验基本操作(练)-《2020年高考一轮复习讲练测》2020届高考化学小题狂练(全国通用版)专练19 化学实验基础江西省上饶市上饶中学2019-2020学年高一上学期第二次月考化学(特零班)试题河北省隆化县存瑞中学2020届高三上学期第二次质检化学试题福建省永春第一中学2018-2019学年高一下学期期末考试化学试题浙江大学附属中学2020届高三1月选考模拟考试化学试题专题4.1 常见的有机物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升专题5.2 化学实验的设计与评价(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升天津市海河中学2020届高三第二学期化学测试(二)试卷第三章 有机化合物 模拟高考——C挑战区 夯实基础(人教版必修2)黑龙江省哈尔滨市第六中学校2019-2020学年高一下学期返校适应训练化学试题黑龙江省牡丹江市第一高级中学2019-2020学年高一下学期6月月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第六次综合测试化学试题吉林省长春市实验中学2019-2020学年高一下学期期末考试化学试题江西省宜春市上高县第二中学2019-2020学年高一下学期期末考试化学试题黑龙江省肇州县第二中学2019-2020学年高一下学期6月月考化学试题(已下线)第28讲 物质的制备-2021年高考化学一轮复习名师精讲练广东省深圳市龙岗区三校2019-2020学年高一下学期期末联考化学试题(已下线)第01讲 化学实验基础知识和技能(精讲)——2021年高考化学一轮复习讲练测新疆哈密市第十五中学2021届高三上学期第一次质量检测化学试题第29讲 重要的烃 同分异构体(精讲)-2021年高考化学一轮复习讲练测(鲁科版2019)必修第二册 第3章 简单的有机化合物 学科素养提升(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)小题11 简单代表物的组成、结构与性质 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第9题 化学实验基础-备战2021年高考化学临考题号押题(课标全国卷)四川省雅安中学2020-2021学年高一下学期期中考试化学试题(人教2019)选择性必修3第二章 C高考挑战区四川省成都外国语学校2020-2021学年高一下学期第三次(6月)月考化学试题山东省菏泽市(一中系列)2020-2021学年高一下学期期末考试化学(A)试题(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点34 物质的制备与合成-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第27讲 常见仪器使用和实验基本操作(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第25讲 烃 有机高分子材料(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第九单元 有机化学基础(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-测试(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)押全国卷理综第9题 化学实验基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题11化学实验基础-五年(2018~2022)高考真题汇编(全国卷)山东省德州市第一中学2021-2022学年高一下学期6月月考化学试题(已下线)第25讲 常见仪器使用和实验基本操作(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第27讲 物质的制备与性质实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题25 化学实验综合性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析(已下线)专题06 突破常见有机化合物(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)题型36 微型成套装置实验流程型(已下线)素养卷07 微型物质制备方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题13 化学实验基础广东省深圳市龙华中学2021-2022学年高三下学期(二月第一次)半周测化学试题(已下线)考点巩固卷10 有机化学基础(一)(3大考点60题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)T9-实验方案的设计与评价河南省焦作市博爱县第一中学2022-2023学年高三下学期5月月考化学试题



