名校
解题方法
1 . 某矿渣中含MgO、Al2O3,、Fe2O3,和SiO2等,通过下列工艺流程可回收其中的Mg、Fe、Al等。

已知:i.溶液中的目标离子浓度小于或等于10-5mol·L-1时,该离子已经完全沉淀。
ii.室温下部分金属离子转化为氢氧化物沉淀的相关pH如下表:
回答下列问题:
(1)“酸浸”时,可以提高浸取反应速率的措施有_______ (任写一条)。
(2)调 ①调整
①调整 合适的范围是
合适的范围是_______ ,若室温下调节 ,则溶液中
,则溶液中
_____  。
。
(3)“调 ②”的目的是
②”的目的是_______ ,“滤液”中溶质的主要成分是_______ (填化学式)。
(4) “加热”制备
“加热”制备 时,必须在
时,必须在 氛围中进行,其目的是
氛围中进行,其目的是_______ 。
(5)“电解”制金属 时:
时:
① 的状态为
的状态为____ (填标号)。
A.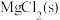 B.
B.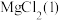 C.
C. (aq)
(aq)
②阳极的电极反应式为____ 。

已知:i.溶液中的目标离子浓度小于或等于10-5mol·L-1时,该离子已经完全沉淀。
ii.室温下部分金属离子转化为氢氧化物沉淀的相关pH如下表:
| 金属离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 2.2 | 3.5 | 9.5 |
| 沉淀完全的pH | 3.2 | 4.7 | 11.1 |
(1)“酸浸”时,可以提高浸取反应速率的措施有
(2)调
 ①调整
①调整 合适的范围是
合适的范围是 ,则溶液中
,则溶液中
 。
。(3)“调
 ②”的目的是
②”的目的是(4)
 “加热”制备
“加热”制备 时,必须在
时,必须在 氛围中进行,其目的是
氛围中进行,其目的是(5)“电解”制金属
 时:
时:①
 的状态为
的状态为A.
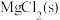 B.
B.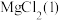 C.
C. (aq)
(aq)②阳极的电极反应式为
您最近一年使用:0次
2024-02-29更新
|
129次组卷
|
2卷引用:四川省眉山市彭山区第一中学2023-2024学年高二下学期开学考试化学试题
2 . 据公安部统计,截至2023年6月底,成都汽车保有量超过600万辆,仅次于北京,居全国第二、高密度的车辆行驶,容易引发交通事故,若车辆受到相对较大撞击,就会引起安全气囊弹出,从而保护车内乘客。叠氮化钠是汽车安全气囊内的重要填充物质。某化学兴趣小组根据工业制备叠氮化钠(NaN3)的方法在实验室设计出制备该物质的装置如下:
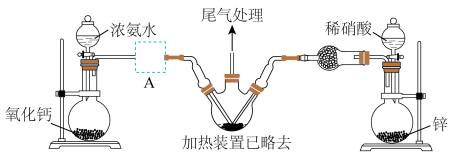
已知:ⅰ.工业上制备 的原理分两步进行:
的原理分两步进行:
①将 通入熔融状态的Na中先制得
通入熔融状态的Na中先制得 ,
,
②将 与
与 加热至
加热至 左右合成
左右合成 ,在合成过程中,易发生副反应:
,在合成过程中,易发生副反应: ;
;
ⅱ. 和
和 的性质如下表:
的性质如下表:
ⅲ. 属于危险化学药品,工业上一般用NaClO销毁剩余
属于危险化学药品,工业上一般用NaClO销毁剩余 ;
;
ⅳ. 与
与 离子反应产生鲜明的血红色,此反应非常灵敏。
离子反应产生鲜明的血红色,此反应非常灵敏。
回答下列问题:
(1)盛装浓氨水的仪器的名称是___________ 。
(2)连接好装置之后,应进行的操作是___________ 。
(3)实验室用 和稀硝酸反应制备
和稀硝酸反应制备 ,其离子方程式为
,其离子方程式为___________ 。
(4)图中虚线框处应选用的装置是___________ (填标号)。

(5)安全气囊中填充 的理由是
的理由是___________ 。
(6)在销毁多余 时会有
时会有 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为___________ ;如何检测销毁是否彻底,请提供一种检测方法:___________ 。

已知:ⅰ.工业上制备
 的原理分两步进行:
的原理分两步进行:①将
 通入熔融状态的Na中先制得
通入熔融状态的Na中先制得 ,
,②将
 与
与 加热至
加热至 左右合成
左右合成 ,在合成过程中,易发生副反应:
,在合成过程中,易发生副反应: ;
;ⅱ.
 和
和 的性质如下表:
的性质如下表:| 物质 |  |  |
| 性质 | 白色固体,易溶于水,有一定危险性,受撞击易快速分解出一种无色、无味、无毒的气体,且有固体Na生成。 | 无色、有甜味的气体,有轻微麻醉作用,常用于医疗,有一定氧化性。 |
 属于危险化学药品,工业上一般用NaClO销毁剩余
属于危险化学药品,工业上一般用NaClO销毁剩余 ;
;ⅳ.
 与
与 离子反应产生鲜明的血红色,此反应非常灵敏。
离子反应产生鲜明的血红色,此反应非常灵敏。回答下列问题:
(1)盛装浓氨水的仪器的名称是
(2)连接好装置之后,应进行的操作是
(3)实验室用
 和稀硝酸反应制备
和稀硝酸反应制备 ,其离子方程式为
,其离子方程式为(4)图中虚线框处应选用的装置是

(5)安全气囊中填充
 的理由是
的理由是(6)在销毁多余
 时会有
时会有 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为
您最近一年使用:0次
名校
3 . 肼( )是我国导弹和运载火箭中广泛使用的液体燃料之一,具有较强的还原性。某实验小组拟用
)是我国导弹和运载火箭中广泛使用的液体燃料之一,具有较强的还原性。某实验小组拟用 和NaClO溶液反应制备肼,装置如图所示(夹持装置未画出)。
和NaClO溶液反应制备肼,装置如图所示(夹持装置未画出)。

(1)装置A中制备 的化学方程式为
的化学方程式为___________________________________ 。
(2)装置B中长颈漏斗的作用是_______________ ;仪器C中盛放的试剂为___________ 。
(3) 的电子式为
的电子式为__________________ ,装置B中制备 的化学方程式为
的化学方程式为___________________ ;
(4)由于反应放热,通常把B装置放于温度较低的水浴中,目的是______________ ;实验时,先打开A中的分液漏斗活塞得到饱和氨水后,再打开D中的漏斗活塞的原因是_____________________ 。
(5)测定产品中 的质量分数
的质量分数
取装置B中的溶液4.00g,并调节为弱酸性,加水配成500mL溶液,从中取25.00mL溶液与0.2000mol/L的 溶液反应(只有
溶液反应(只有 参与反应,其他物质不反应),反应过程中有无污染性的气体生成,消耗
参与反应,其他物质不反应),反应过程中有无污染性的气体生成,消耗 溶液的体积为20.00mL,则该产品中
溶液的体积为20.00mL,则该产品中 的质量分数为
的质量分数为___________ %。
 )是我国导弹和运载火箭中广泛使用的液体燃料之一,具有较强的还原性。某实验小组拟用
)是我国导弹和运载火箭中广泛使用的液体燃料之一,具有较强的还原性。某实验小组拟用 和NaClO溶液反应制备肼,装置如图所示(夹持装置未画出)。
和NaClO溶液反应制备肼,装置如图所示(夹持装置未画出)。
(1)装置A中制备
 的化学方程式为
的化学方程式为(2)装置B中长颈漏斗的作用是
(3)
 的电子式为
的电子式为 的化学方程式为
的化学方程式为(4)由于反应放热,通常把B装置放于温度较低的水浴中,目的是
(5)测定产品中
 的质量分数
的质量分数取装置B中的溶液4.00g,并调节为弱酸性,加水配成500mL溶液,从中取25.00mL溶液与0.2000mol/L的
 溶液反应(只有
溶液反应(只有 参与反应,其他物质不反应),反应过程中有无污染性的气体生成,消耗
参与反应,其他物质不反应),反应过程中有无污染性的气体生成,消耗 溶液的体积为20.00mL,则该产品中
溶液的体积为20.00mL,则该产品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
4 . 氨基甲酸铵(NH2COONH4)是一种重要的医用氨化剂,有关该物质的信息如下表所示:
某实验小组在实验室中利用下列装置合成少量的氨基甲酸铵。回答下列问题:
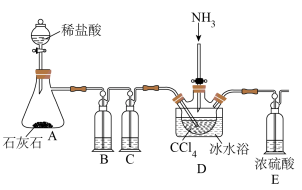
(1)盛放稀盐酸的仪器的名称是___________ 。
(2)装置B和C中试剂的名称分别是___________ 、___________ 。
(3)实验室制取氨气的化学方程式为___________ 。
(4)反应结束后,从三颈烧瓶中分离出产品,进行的实验操作是___________ 。
(5)装置E的作用有___________ (写出两点)。若观察到E中出现大量气泡(浓硫酸足量),则可能的原因是___________ 。
(6)设计实验:检验制得的产品中是否混有 ?
?___________ 。
| 制备原理 | 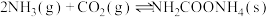 放热反应 放热反应 |
| 主要性质 | ①在潮湿的空气中转变为 ②温度较高时容易分解生成  、 、 ③不溶于  |

(1)盛放稀盐酸的仪器的名称是
(2)装置B和C中试剂的名称分别是
(3)实验室制取氨气的化学方程式为
(4)反应结束后,从三颈烧瓶中分离出产品,进行的实验操作是
(5)装置E的作用有
(6)设计实验:检验制得的产品中是否混有
 ?
?
您最近一年使用:0次
2023-07-14更新
|
78次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高二上学期开学化学试题
名校
5 . 过氧化钙晶体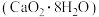 为白色固体,难溶于水,可做分析试剂、消毒剂等。制备
为白色固体,难溶于水,可做分析试剂、消毒剂等。制备 晶体的装置如下图所示。回答相关问题:
晶体的装置如下图所示。回答相关问题:___________ 。
(2)B中反应需在0℃~3℃的温度下进行,B可采用的降温方式为___________ 。B中发生的离子反应方程式为___________ 。
(3)C管起到平衡气压的作用,加水液封的目的是___________ 。
(4)该实验装置还需要在AB之间增加一个装置,其作用是___________ 。
(5)碘量法测定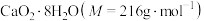 的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用
的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用 的
的 溶液滴定至终点,终点溶液颜色变化为
溶液滴定至终点,终点溶液颜色变化为___________ ,重复操作2次,三次平均消耗 溶液体积为15.00mL,则
溶液体积为15.00mL,则 的质量分数为
的质量分数为___________ %。
已知: ;
; 。
。
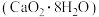 为白色固体,难溶于水,可做分析试剂、消毒剂等。制备
为白色固体,难溶于水,可做分析试剂、消毒剂等。制备 晶体的装置如下图所示。回答相关问题:
晶体的装置如下图所示。回答相关问题: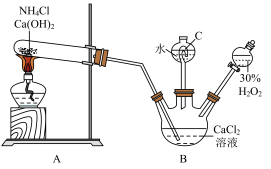
(2)B中反应需在0℃~3℃的温度下进行,B可采用的降温方式为
(3)C管起到平衡气压的作用,加水液封的目的是
(4)该实验装置还需要在AB之间增加一个装置,其作用是
(5)碘量法测定
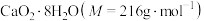 的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用
的纯度:准确称取2.0g产品放入锥形瓶中,加入适量蒸馏水和过量KI固体,再酸化,充分反应。滴加淀粉作指示剂,用 的
的 溶液滴定至终点,终点溶液颜色变化为
溶液滴定至终点,终点溶液颜色变化为 溶液体积为15.00mL,则
溶液体积为15.00mL,则 的质量分数为
的质量分数为已知:
 ;
; 。
。
您最近一年使用:0次
2023-04-22更新
|
95次组卷
|
2卷引用:四川省德阳外国语学校2023-2024学年高二下学期入学考试化学试题
6 . 工业上用饱和食盐水吸收尾气 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):

已知:浓硫酸的沸点为338℃。回答下列问题:
(1)仪器a的名称_______ ,导气管b的作用_______ 。
(2)装置A中发生的化学反应的化学方程式为_______ 。
(3)固、固加热制取氨气的发生装置可以选择下图中的_______ (填编号),反应的化学方程式为_______ 。

(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得_______ ,然后将滤液_______ 、过滤、洗涤、干燥可得另一产物。

(5)产品中可能混有少量 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是_______ ,检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,_______ 。
【可选试剂:稀硝酸、 溶液、酸性
溶液、酸性 溶液、
溶液、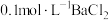 溶液、
溶液、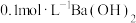 溶液、
溶液、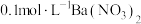 溶液】
溶液】
 和
和 制备无水
制备无水 。同时得到副产物
。同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
已知:浓硫酸的沸点为338℃。回答下列问题:
(1)仪器a的名称
(2)装置A中发生的化学反应的化学方程式为
(3)固、固加热制取氨气的发生装置可以选择下图中的

(4)利用各物质的溶解度曲线图(见图)分离产品,取出装置B中的溶液,蒸发浓缩,趁热过滤可得

(5)产品中可能混有少量
 和
和 杂质,混有
杂质,混有 杂质的原因可能是
杂质的原因可能是 的的实验方法:取少量样品于试管中,加入适量水溶解,
的的实验方法:取少量样品于试管中,加入适量水溶解,【可选试剂:稀硝酸、
 溶液、酸性
溶液、酸性 溶液、
溶液、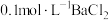 溶液、
溶液、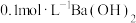 溶液、
溶液、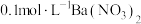 溶液】
溶液】
您最近一年使用:0次
2023-02-25更新
|
990次组卷
|
4卷引用:四川省内江市第六中学2023-2024学年高二上学期入学考试化学试题
名校
解题方法
7 . 黄铜矿( )是一种较常见的铜矿物,可形成于不同的环境下,产地遍布世界各地。在工业上,它是炼铜的主要原料,其流程如图。
)是一种较常见的铜矿物,可形成于不同的环境下,产地遍布世界各地。在工业上,它是炼铜的主要原料,其流程如图。

根据所学知识,回答下列问题:
(1)在“浸取”前,应先对黄铜矿进行粉碎处理,其目的是_______ 。
(2)实验室利用 配制澄清的
配制澄清的 溶液的方法是
溶液的方法是_______ 。
(3)写出“浸取”时 和
和 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)为提高废物利用率,可向黄铜矿“浸取”后的滤液中通入(或滴加)_______ 。
(5)工业上也通过黄铜矿进行火法炼铜,其主要反应有:
步骤I: (炉渣);
(炉渣);
步骤II: ;
;
步骤III:……
步骤I的反应中每生成 时,反应中转移的电子的物质的星为
时,反应中转移的电子的物质的星为_______ mol;
步骤I、II两步反应生成的铜产物( 、
、 )在1200℃条件下继续反应生成单质铜,请写出步骤Ⅲ反应的化学方程式:
)在1200℃条件下继续反应生成单质铜,请写出步骤Ⅲ反应的化学方程式:_______ 。
 )是一种较常见的铜矿物,可形成于不同的环境下,产地遍布世界各地。在工业上,它是炼铜的主要原料,其流程如图。
)是一种较常见的铜矿物,可形成于不同的环境下,产地遍布世界各地。在工业上,它是炼铜的主要原料,其流程如图。
根据所学知识,回答下列问题:
(1)在“浸取”前,应先对黄铜矿进行粉碎处理,其目的是
(2)实验室利用
 配制澄清的
配制澄清的 溶液的方法是
溶液的方法是(3)写出“浸取”时
 和
和 溶液反应的离子方程式:
溶液反应的离子方程式:(4)为提高废物利用率,可向黄铜矿“浸取”后的滤液中通入(或滴加)
(5)工业上也通过黄铜矿进行火法炼铜,其主要反应有:
步骤I:
 (炉渣);
(炉渣);步骤II:
 ;
;步骤III:……
步骤I的反应中每生成
 时,反应中转移的电子的物质的星为
时,反应中转移的电子的物质的星为步骤I、II两步反应生成的铜产物(
 、
、 )在1200℃条件下继续反应生成单质铜,请写出步骤Ⅲ反应的化学方程式:
)在1200℃条件下继续反应生成单质铜,请写出步骤Ⅲ反应的化学方程式:
您最近一年使用:0次
2022-12-20更新
|
52次组卷
|
2卷引用:四川省泸州市泸县第五中学2023-2024学年高二下学期开学化学试题
名校
解题方法
8 . 碘化钾可用于有机合成、制药等,它是一种白色立方晶体或粉末,易溶于水。实验室制备KI的实验装置如下:

已知:Ⅰ.N2H4是非电解质,沸点为113.5℃,具有强还原性,其氧化产物为N2。
Ⅱ.装置B是单向阀,作用是使装置A中生成的NH3进入装置C,而装置C中生成的N2H4不会进入装置A。
回答下列问题:
(1)装置A中生成NH3的化学反应方程式为_______ 。
(2)盛放NaClO溶液的仪器名称是_______ 。
(3)实验时,装置A处的大试管与装置C处的三颈烧瓶均需加热,应先加热装置_______ 处(填“A”或“C”)。
(4)装置C中NaClO溶液不能加入过多,其原因是_______ 。
(5)装置E中KOH、 与N2H4发生反应生成KI,反应的离子方程式为
与N2H4发生反应生成KI,反应的离子方程式为_______ 。
(6)反应过程中需用热源间歇性微热D处连接管,目的是_______ 。
(7)装置F中稀硫酸的作用是_______ 。

已知:Ⅰ.N2H4是非电解质,沸点为113.5℃,具有强还原性,其氧化产物为N2。
Ⅱ.装置B是单向阀,作用是使装置A中生成的NH3进入装置C,而装置C中生成的N2H4不会进入装置A。
回答下列问题:
(1)装置A中生成NH3的化学反应方程式为
(2)盛放NaClO溶液的仪器名称是
(3)实验时,装置A处的大试管与装置C处的三颈烧瓶均需加热,应先加热装置
(4)装置C中NaClO溶液不能加入过多,其原因是
(5)装置E中KOH、
 与N2H4发生反应生成KI,反应的离子方程式为
与N2H4发生反应生成KI,反应的离子方程式为(6)反应过程中需用热源间歇性微热D处连接管,目的是
(7)装置F中稀硫酸的作用是
您最近一年使用:0次
名校
9 . 肼(N2H4) 是一种重要的工业产品,实验室用NH3与Cl2合成肼(N2H4) 并探究肼的性质。实验装置如图所示:
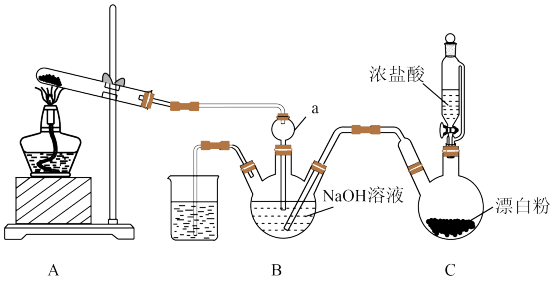
相关物质的性质如下:
回答下列问题:
(1)装置A试管中的试剂为_______ (填化学式)。仪器a的名称是_______ 。
(2)N2H4是_______ 分子(填“极性”或“非极性”)。
(3)装置B中制备肼的离子方程式为_______ ,该装置中通入NH3必须过量的原因是_______ 。
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究N2H4的性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元弱碱,肼与硫酸反应除能生成N2H6SO4外,还可能生成的盐为_______ 。(填化学式)。
②测定肼的质量分数。取装置B中的溶液3.2g,调节溶液pH为6.5左右,加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用c mol·L-1的碘溶液滴定(杂质不参与反应),滴定过程中有无色、无味、无毒气体产生。滴定终点平均消耗标准溶液20.00mL,产品中肼的质量分数为_______ %。

相关物质的性质如下:
| 性状 | 熔点/℃ | 沸点/℃ | 性质 | |
| N2H4 | 无色液体 | 1.4 | 113 | 与水混溶、强还原性 |
| N2H6SO4 | 无色晶体 | 254 | / | 微溶于冷水,易溶于热水 |
(1)装置A试管中的试剂为
(2)N2H4是
(3)装置B中制备肼的离子方程式为
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究N2H4的性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到无色晶体。肼是一种二元弱碱,肼与硫酸反应除能生成N2H6SO4外,还可能生成的盐为
②测定肼的质量分数。取装置B中的溶液3.2g,调节溶液pH为6.5左右,加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用c mol·L-1的碘溶液滴定(杂质不参与反应),滴定过程中有无色、无味、无毒气体产生。滴定终点平均消耗标准溶液20.00mL,产品中肼的质量分数为
您最近一年使用:0次
2022-09-17更新
|
842次组卷
|
7卷引用:四川省泸州市泸县第五中学2023-2024学年高二下学期开学化学试题
名校
10 . ClO2作为一种广泛的消毒剂,它是一种易溶于水而难溶于有机溶剂的黄绿色气体,实验室用NaClO2与Cl2反应制得ClO2。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去ClO2中的未反应的Cl2)。
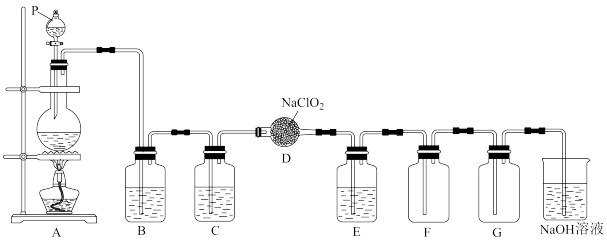
(1)仪器P的名称为____ 。
(2)请写出装置A圆底烧瓶内发生反应的化学方程式____ 。
(3)C装置中所盛试剂为____ ,G装置的作用____ 。
(4)装置D中发生反应的化学方程式为____ ,每生成1molClO2,转移的电子数目为____ 。

(1)仪器P的名称为
(2)请写出装置A圆底烧瓶内发生反应的化学方程式
(3)C装置中所盛试剂为
(4)装置D中发生反应的化学方程式为
您最近一年使用:0次



