19. 实验室制备Cl
2通常采用如图所示装置:
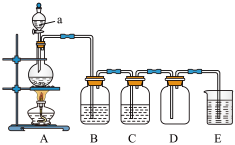
(1)A装置中发生反应的化学方程式是
________;每生成0.5 mol Cl
2,被氧化的物质的物质的量是
_____mol。
(2)仪器a的名称是
_________;
(3)B装置中所盛的试剂是
________________;
(4)实验时,通常采用密度为1.19 g/cm
3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为
________;
(5)将如图装置代替装置D和E,可进行“氯气与金属钠反应”的实验,以下叙述正确的是
________。
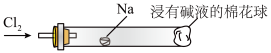
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气
C. 玻璃管中,钠燃烧时会产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
(6)E装置中发生反应的化学方程式是
________________;为验证E装置反应后的溶液中存在Cl
-,正确的操作是
_____________。