上海市奉贤区曙光中学2017-2018学年高三上学期期中考试化学试题
上海
高三
期中
2020-03-25
210次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.水 | B.氯化钠 | C.乙醇 | D.脂肪 |
【知识点】 无机物质的分类
| A.CH2=CH-CH=CH2 1,3-二丁烯 | B.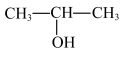 2-羟基丙烷 2-羟基丙烷 |
C.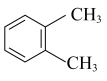 1,2-二甲苯 1,2-二甲苯 | D.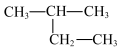 2-乙基丙烷 2-乙基丙烷 |
【知识点】 烯烃、炔烃的命名 烷烃系统命名法解读 含有苯环的化合物的命名解读
A.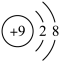 | B. | C.I- | D.1s22s22p63s23p6 |
【知识点】 盐类水解的应用 元素性质与原子结构的关系解读
| A.Ar | B.Na2O2 | C.MgO | D.金刚石 |
【知识点】 离子键 共价键 化学键与分子间作用力解读 化学键类别与晶体类别间的关系解读
| A.浓硫酸的氧化性强于稀硫酸 |
| B.与冷水反应的速率:Na>Mg |
| C.向淀粉KI溶液中滴入氯水,溶液变蓝 |
| D.原子半径:Al>Si>P |
| A.反应的速率:反应物的本性 | B.KNO3的溶解度:温度 |
| C.分子间作用力:分子的质量 | D.气体摩尔体积:气体的物质的量 |
| A.1:3 | B.3:1 | C.1:1 | D.3:8 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
 cZ(g)达到平衡时平衡常数为K1;在温度不变的条件下向容器中通入一定量的X和Y气体,达到新的平衡后Z的浓度为原来的1.2倍,平衡常数为K2,则K1与K2的大小关系是( )
cZ(g)达到平衡时平衡常数为K1;在温度不变的条件下向容器中通入一定量的X和Y气体,达到新的平衡后Z的浓度为原来的1.2倍,平衡常数为K2,则K1与K2的大小关系是( )| A.K1<K2 | B.K1=K2 | C.K1>K2 | D.无法确定 |
【知识点】 化学平衡常数
| A.KHSO4 | B.CH3COOH | C.FeCl3 | D.NaHSO3 |
【知识点】 溶液的酸碱性与pH 盐类水解规律理解及应用解读
| 所含离子 | NO3- | SO42- | H+ | M |
| 物质的量浓度(mol∙L-1) | 2 | 1 | 3 | 1 |
| A.Ba2+ | B.Mg2+ | C.F- | D.Na+ |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
| A.该气体中肯定含有H2S和SO2 | B.该气体不能肯定是否含有SO2 |
| C.该气体中肯定含有CO2和SO2 | D.该气体中肯定不含有H2S和HI |
A.氯气的收集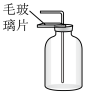 | B.氯气的吸收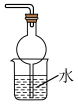 |
C.氯化氢的吸收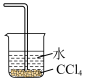 | D.食盐水的蒸发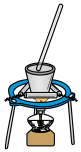 |
【知识点】 氯气的制法 物质分离、提纯综合应用解读
| 物质 | 杂质 | 试剂 | 提纯方法 | |
A | 乙炔 | 硫化氢 | 酸性高锰酸钾溶液 | 分液 |
B | 二氧化碳 | 二氧化硫 | 饱和碳酸钠溶液 | 洗气 |
C | 甲烷 | 乙烯 | 溴水 | 洗气 |
D | 乙醛 | 乙酸 | 稀氢氧化钠溶液 | 分液 |
| A.A | B.B | C.C | D.D |
 H++OH--Q的平衡,下列叙述一定正确的是( )
H++OH--Q的平衡,下列叙述一定正确的是( )| A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小 |
| B.将水加热,Kw增大,pH减小 |
| C.向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低 |
| D.向水中加入少量固体硫酸钠,c(H+)=10-7mol/L,Kw不变 |
| A.氢氧化钡溶液与稀硫酸混合:Ba2++SO42-→BaSO4↓ |
| B.铁片放入稀盐酸溶液中:2Fe+6H+→2Fe3++3H2↑ |
| C.向Ca(ClO)2溶液中通入过量CO2:ClO-+H2O+CO2→HClO+HCO3– |
| D.Na2CO3溶液中CO32-的水解:CO32-+2H2O→H2CO3+2OH- |
【知识点】 离子方程式的正误判断解读

| A.负极反应式为:2H++2e-→H2↑ |
| B.此过程中铁做负极,被氧化 |
| C.此过程中铜会被腐蚀,发生氧化反应 |
| D.此过程中电子从Fe移向Cu,铁铆钉发生还原反应 |
【知识点】 金属的电化学腐蚀与防护 原电池原理 吸氧腐蚀解读
 2NH3(g)过程的能量变化如图所示。下列说法正确的是
2NH3(g)过程的能量变化如图所示。下列说法正确的是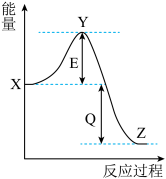
| A.加入催化剂,Z点位置降低 | B.反应热=E+Q |
| C.加入催化剂,Y点位置降低 | D.加入催化剂,反应热减少 |
【知识点】 化学反应中能量变化的原因 能量的相互转化
| A.显碱性 | B.显中性 | C.显酸性 | D.可能中性、碱性、酸性 |
【知识点】 溶液的酸碱性与pH 酸碱混合时的定性判断及计算解读
| A.6g | B.5g | C.4g | D.3g |
【知识点】 二氧化硫的化学性质
二、填空题 添加题型下试题
(1)饱和食盐水所用的原料粗盐主要来自于海洋,从海水中得到粗盐我们通常用的方法是
(2)所得的粗盐(含Ca2+、Mg2+、SO42-)需要提纯,需要加入足量NaOH、BaCl2、Na2CO3溶液将杂质离子除去,随后过滤并加入盐酸调pH至7。其中先用BaCl2,再用Na2CO3的原因是
(3)饱和食盐水除用于制纯碱,也是氯碱工业的原料。氯碱工业中电解饱和食盐水的方程式为
(4)测试纯碱产品中NaHCO3含量的方法是:用
(5)若上述过程中共消耗氢氧化钠58.00mL,纯碱样品中NaHCO3质量分数为
(6)如果装氢氧化钠的滴定管滴定结束读数时有漏液情况,会导致测定结果
【知识点】 酸碱中和滴定原理的应用解读 氯碱工业解读 物质的分离、提纯
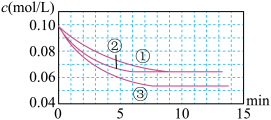
(1)工业制硫酸的接触室中用二氧化硫与氧气制三氧化硫的生产条件为
(2)实验②,0~4min 平均反应速率v(O2)=
(3)实验③可能改变的条件是什么:
(4)二氧化硫尾气可以用氨水吸收,最终的产物可能有(NH4)2SO4、(NH4)2SO3、NH4HSO3。若三者的物质的量浓度相同时,铵根离子浓度由大到小的顺序为
(5)浓硫酸是常见的干燥剂,请解释不能干燥硫化氢与氨气的原因
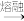 2Na2SiO3+CaSiO3+CO2↑
2Na2SiO3+CaSiO3+CO2↑(1)某反应物在熔融状态下不导电,它属于
(2)上述反应里所涉及的短周期元素原子半径由大到小的顺序为
(3)碳和硅属于同族元素,该族元素的原子最外层轨道表示式为
(4)写一个能比较碳元素和氧元素非金属性强弱的化学反应方程式:
(5)CO2的电子式为
(6)反应物Na2CO3和CaCO3均能制备二氧化碳,但是往往不是都能使用稀硫酸,请说明理由:
三、解答题 添加题型下试题
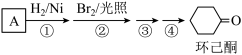
回答下列问题:
(1)反应①的反应类型为
(2)反应④所用的试剂为
(3)A的同系物(C8H10)所有可能的结构简式为
(4)环己酮的还原产物能与乙酸产生乙酸乙酯,请写出产生酯的条件:
(5)写出A的相邻同系物合成
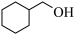 的合成路线
的合成路线合成路线的常用表示方式为:A
 B……
B…… 目标产物。
目标产物。
【知识点】 有机反应类型 同分异构体书写 有机物的合成 根据题给物质选择合适合成路线解读
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 常见能量转化形式 | |
| 2 | 0.94 | 无机物质的分类 | |
| 3 | 0.65 | 烯烃、炔烃的命名 烷烃系统命名法 含有苯环的化合物的命名 | |
| 4 | 0.65 | 盐类水解的应用 元素性质与原子结构的关系 | |
| 5 | 0.65 | 离子键 共价键 化学键与分子间作用力 化学键类别与晶体类别间的关系 | |
| 6 | 0.85 | 同周期元素性质递变规律探究实验 元素非金属性强弱的比较方法 | |
| 7 | 0.65 | 决定物质体积大小的微观因素 影响化学反应速率的内因 化学键与分子间作用力 | |
| 8 | 0.65 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 9 | 0.94 | 化学平衡常数 | |
| 10 | 0.65 | 溶液的酸碱性与pH 盐类水解规律理解及应用 | |
| 11 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 | |
| 12 | 0.65 | 氯水 二氧化硫的化学性质 硫化氢 常见气体的检验 | |
| 13 | 0.65 | 氯气的制法 物质分离、提纯综合应用 | |
| 14 | 0.65 | 有机物分离提纯的几种常见操作 物质分离、提纯的常见化学方法 | |
| 15 | 0.85 | 水的电离 影响水电离的因素 | |
| 16 | 0.65 | 离子方程式的正误判断 | |
| 17 | 0.85 | 金属的电化学腐蚀与防护 原电池原理 吸氧腐蚀 | |
| 18 | 0.65 | 化学反应中能量变化的原因 能量的相互转化 | |
| 19 | 0.65 | 溶液的酸碱性与pH 酸碱混合时的定性判断及计算 | |
| 20 | 0.65 | 二氧化硫的化学性质 | |
| 二、填空题 | |||
| 21 | 0.65 | 酸碱中和滴定原理的应用 氯碱工业 物质的分离、提纯 | |
| 22 | 0.65 | 二氧化硫与氧气的反应 化学反应速率计算 温度对化学平衡移动的影响 盐类水解的应用 | |
| 23 | 0.85 | 元素金属性与非金属性递变规律的理解及应用 微粒半径大小的比较方法 轨道表示式 常见原子晶体的结构 | |
| 三、解答题 | |||
| 24 | 0.65 | 有机反应类型 同分异构体书写 有机物的合成 根据题给物质选择合适合成路线 | 有机推断题 |



