29. I、为了模拟汽车尾气在催化转化器内的工作情况:
(1)控制条件,让反应在恒容密闭容器中进行如下反应:2NO(g)+2CO(g)⇌ N
2(g)+2CO
2(g),用传感器测得不同时间NO和CO的浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(NO)(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
前2s内的平均反应速率v(N
2)=
____,从表格看,达到化学平衡的时间段为:
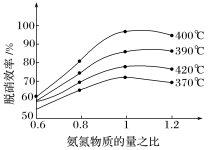
____(2)用氨气催化氧化还原法脱硝(NOx):根据如图(纵坐标是脱硝效率、横坐标为氨氮物质的量之比),判断提高脱硝效率的最佳条件是:
____。
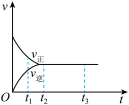
(3)如图是在一定温度下,某固定容积的密闭容器中充入一定量的NO
2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是
____。
a.t
1时,反应未达到平衡,NO
2浓度在减小
b.t
2时,反应达到平衡,反应不再进行
c.t
2~t
3,各物质浓度不再变化
d.t
2~t
3,各物质的浓度相等
e.0~t
2,N
2O
4浓度增大
f.反应过程中气体的颜色不变
g.建立平衡过程中,混合气体平均相对分子质量增大
Ⅱ、甲醇是一种很好的燃料
(1)在压强为0.1MPa条件下,amolCO与3amolH
2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H
2(g)
⇌CH
3OH(l)放热。为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在了面的实验设计表中.
| 实验编号 | T(℃) | n(CO)/n(H2) | P(MPa) |
| ① | 180 | 2:3 | 0.1 |
| ② | n | 2:3 | 5 |
| ③ | 350 | m | 5 |
表中剩余的实验数据:n=
____,m=
____.
(2)CH
3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。下列说法不正确的是
____(填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH
3OH转移1.2mol电子
④负极反应式为CH
3OH+8OH
--6e
-=CO
32-+6H
2O
(3)某反应2A⇌B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L
-1)随反应时间(min)的变化情况如表所示。

①在实验2中,A的初始浓度c
2=
____mol·L
-1。
②设实验3的反应速率为v
3,实验1的反应速率为v
1,则v
3____v
l(填“>”、“="或“<”)。