19. 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:
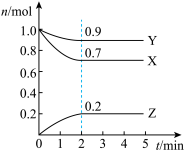
(1)由图中所给数据进行分析,该反应的化学方程式为
_________。
(2)若上述反应中X、Y、Z分别为H
2、N
2、NH
3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN
2和2.0mol H
2,一段时间后反应达平衡状态,实验数据如表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.36 | 0.48 | 0.50 | 0.50 |
0~50s内的平均反应速率
v(N
2)=
__________。
(3)已知:键能指在标准状况下,将lmol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号
E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成lmol NH
3过程中放出46kJ的热量。则N≡N的键能为
_________kJ/mol。
(4)CO与H
2反应可制备CH
3OH,由CH
3OH和O
2构成的质子交换膜燃料电池的结构示意图如下。
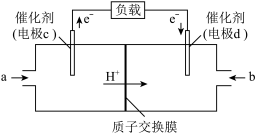
电池总反应为2CH
3OH+3O
2=2CO
2+4H
2O,则c电极是
________(填“正极”或“负极”),c电极的电极反应式为
___________。若外电路中转移2 mol电子,则上述燃料电池所消耗的O
2在标准状况下的体积为
______ L。
(5)下列反应中,属于吸热反应的是
__________(填序号)
①物质燃烧
②炸药爆炸
③酸碱中和反应
④二氧化碳通过炽热的碳
⑤食物因氧化而腐败
⑥Ba(OH)
2·8H
2O与NH
4Cl反应
⑦铁粉与稀盐酸反应