9. Li
2S(硫化锂)是一种潜在的锂电池的电解质材料。某小组选择下列装置(装置B使用两次)利用氢气还原硫酸锂制备硫化锂,原理是Li
2SO
4+4H
2
Li
2S+4H
2O。已知:Li
2S易潮解,在加热条件下易被空气中的O
2氧化。实验室用粗锌(含少量铜、FeS)和稀硫酸反应制备H
2。
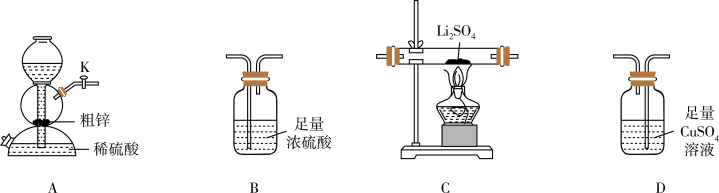
请回答下列问题:
(1)按气流从左至右,装置的连接顺序是A→
____(填字母)。
(2)其他条件相同,粗锌与稀硫酸反应比纯锌
____(填“快”或“慢”)。实验中观察到装置D中产生黑色沉淀,其离子方程式为
____。
(3)还可利用装置A制备的下列气体是
____(填字母)。
A.SO
2:70%硫酸、亚硫酸钠粉末
B.CO
2:稀盐酸、大理石
C.Cl
2:浓盐酸、二氧化锰
(4)实验完毕后,采用图1、图2(夹持装置已略去)装置对装置A中混合物进行分离可得到副产物皓矾(ZnSO
4·7H
2O)晶体。先选择图1装置进行过滤,并将滤液进行蒸发浓缩、降温结晶,再选择图2装置过滤,得到粗皓矾晶体。
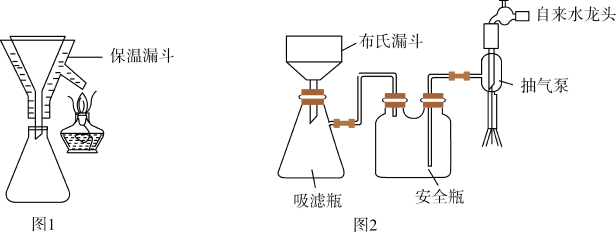
下列有关说法正确的是
____(填字母)。
| A.采用图1装置过滤的优点是避免析出ZnSO4·7H2O |
| B.采用图1装置过滤主要是分离FeSO4·7H2O和ZnSO4溶液 |
| C.粗皓矾晶体中可能含少量CuSO4·5H2O杂质 |
| D.采用图2装置过滤的优点是过滤速度快 |
(5)欲探究Li
2S产品的成分,现进行如表实验:
| 实验 | 操作与现象 | 结论 |
| I | 取少量Li2S样品,滴加足量的稀盐酸,将气体通入品红溶液中,溶液褪色 | 样品含Li2SO3 |
| II | 在实验I的溶液中滴加BaCl2溶液,产生白色沉淀 | 样品含 |
①由上述实验II可知,Li
2S样品中含有
____杂质(填化学式),产生该杂质的原因可能是
____。
②测定产品纯度的方法:取wgLi
2S样品加入V
1mLc
1mol·L
-1稀硫酸(过量)中,充分反应后,煮沸溶液以除去残留的酸性气体;滴加酚酞溶液作指示剂,用c
2mol·L
-1标准NaOH溶液滴定过量的硫酸,消耗NaOH溶液V
2mL。若该Li
2S样品中杂质不参加反应,用上述方法测得的Li
2S样品的纯度为
____%(用含V
1、V
2、c
1、c
2、w的代数式表示)。