河南省部分学校2023届高三下学期模拟预测理科综合化学试题
河南
高三
模拟预测
2023-07-13
294次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学与STSE、化学反应原理、化学实验基础、有机化学基础
河南省部分学校2023届高三下学期模拟预测理科综合化学试题
河南
高三
模拟预测
2023-07-13
294次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学与STSE、化学反应原理、化学实验基础、有机化学基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 科技进步促进社会发展。 下列有关最新科技成果的解读错误的是
| 选项 | 最新成果 | 化学解读 |
| A | 首次实现CO2和NH3协同催化合成甘氨酸 | 发生了化学变化 |
| B | 首次合成石墨炔、聚C60材料 | 石墨炔和C60互为同素异形体 |
| C | 首次检测月壤富含Cr、Be、Ni、Co元素 | 它们都是长周期元素 |
| D | 光学观测有助于构建纯硅量子互联网 | 硅是半导体材料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难(0.4)
2. 为了探究CdS、Ag2S的溶解度相对大小,利用如图装置进行实验。
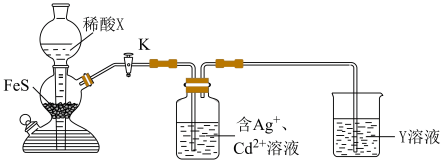
已知:Ag2S呈黑色,难溶;CdS呈黄色,难溶;FeS呈块状黑色,难溶。下列叙述正确的是

已知:Ag2S呈黑色,难溶;CdS呈黄色,难溶;FeS呈块状黑色,难溶。下列叙述正确的是
| A.X为硝酸,Y溶液为硫酸铜溶液 |
| B.若装置B中先生成黑色沉淀,则Ag2S的溶解度小于CdS |
| C.停止反应的操作是关闭活塞K |
| D.用浓盐酸和MnO2制备氯气时可以用装置A |
您最近一年使用:0次
2023-06-06更新
|
1645次组卷
|
3卷引用:河南省部分学校2023届高三下学期模拟预测理科综合化学试题
单选题
|
较难(0.4)
3. 最近,科学家开发了一种用二氧化碳淡化海水的技术,其循环图如下:
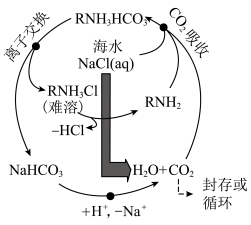
下列有关叙述错误的是

下列有关叙述错误的是
| A.上述转化中包括氧化还原反应 |
| B.该技术中发生离子交换的实质是产物溶解度较小 |
| C.加热RNH3Cl并用水吸收HCl可制盐酸 |
| D.淡化后的海水导电性减弱; |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 中南民族大学张泽会教授课题组开发催化剂高效催化碳水化合物转化为有机酸和呋喃化学品,如图所示。已知:碳原子上连有4个不同的原子或基团时,该碳称为手性碳。下列叙述正确的是
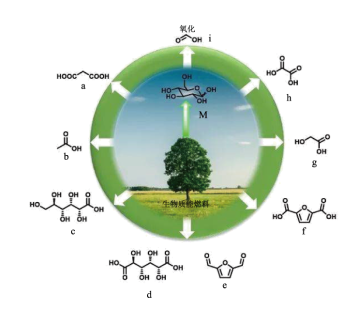

| A.a和h互为同分异构体 |
| B.M和c分子所含手性碳原子数相等 |
| C.可用NaHCO3溶液区别d和f |
| D.等物质的量的c和d,d消耗NaOH的量是c的2倍 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 短周期主族元素W、Y、Z、X的原子半径依次减小,锂离子电池的一种溶剂的结构式如图1所示。已知,X、Y、Z的原子序数之和等于15。在W的硝酸盐溶液中滴加烧碱溶液,生成沉淀的物质的量与烧碱溶液体积的关系如图2所示。下列叙述正确的是


| A.原子序数:W>Y >Z>X |
| B.工业上电解熔融W2Z3制备W的单质 |
| C.最高价氧化物对应水化物的酸性:W> Y |
| D.简单氢化物的稳定性:Y >Z |
您最近一年使用:0次
单选题
|
适中(0.65)
6. 南开大学教授罗景山课题组基于中性水分解反应体系对CaCO3进行处理转化,此过程利用中性水分解反应中析氧反应过程产生的H+与CaCO3反应生成Ca2+及CO,Ca2+与体系中生成的OH -结合形成Ca( OH)2,可直接用于水泥生产,工作原理如图所示。

下列叙述正确的是

下列叙述正确的是
| A.电极电势:c>d |
| B.气体1为O2,气体2为H2 |
| C.通过交换膜M和交换膜N的OH-、H+总数一定相等 |
| D.制备C2H4的电极反应为2CO2 +8H2O + 12e-= C2H4 + 12OH- |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
7. 常温下,三种金属硫化物XS、YS、ZS的饱和溶液中pM[pM= -lgc(M2+)]与pS[pS= -lgc(S2-)]的关系如图所示。已知:Ksp(XS) > Ksp(YS) > Ksp (ZS)。

| A.直线③代表ZS |
| B.Ksp (XS) =1 ×10-36 |
| C.向c点饱和溶液中加少量Na2S,c点向b点迁移 |
D.YS(s) +Z2+(aq)  ZS(s) +Y2+ (aq) K=1 ×108 ZS(s) +Y2+ (aq) K=1 ×108 |
您最近一年使用:0次
2023-06-06更新
|
185次组卷
|
3卷引用:河南省部分学校2023届高三下学期模拟预测理科综合化学试题
二、解答题 添加题型下试题
8. 羟基氧化镍( NiOOH)可作镍镉电池正极材料[放电时产物之一是Ni( OH)2];高纯度一氧化锰(MnO)可用于医药、冶炼、焊接、干电池的制造。某化工厂以含有MnS、NiS的工业料渣为原料制备NiOOH、MnO的流程如下:

请回答下列问题:
(1)写出一种能提高料渣利用率的方法:___________ ,操作X的名称是___________ 。
(2)NiOOH中Ni元素的化合价为___________ , 溶剂A必须具有的两种物理性质:一是不溶于水;二是___________ ;写出生成NiOOH的离子方程式:___________ 。
(3)热氧化过程中MnS发生反应时氧化剂与还原剂的物质的量之比为___________ 。214℃时MnC2O4分解(隔绝空气)的化学方程式为___________ 。
(4)镍镉碱性电池放电时发生还原反应的电极上的反应式为。___________ 。
(5)若10 kg料渣经过上述处理后得到a kg NiOOH,则料渣中Ni的质量分数为___________ (设转化过程中镍的损失率为2% ,列出计算式即可)。

请回答下列问题:
(1)写出一种能提高料渣利用率的方法:
(2)NiOOH中Ni元素的化合价为
(3)热氧化过程中MnS发生反应时氧化剂与还原剂的物质的量之比为
(4)镍镉碱性电池放电时发生还原反应的电极上的反应式为。
(5)若10 kg料渣经过上述处理后得到a kg NiOOH,则料渣中Ni的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
解题方法
9. 稳定的[Co(NH3)6]Cl3常用于制备钴的高效催化剂,制备条件(催化剂、温度等)不同,其组成不同,如[Co(NH3)6]Cl3 (橙黄色)、[Co(NH3)5H2O]Cl3 (紫红色)等。某小组拟制备三氯六氨合钴[Co(NH3)6]Cl3并测定其纯度。回答下列问题:
实验(一)制备[Co(NH3)6]Cl3产品。

(1)步骤②中活性炭的作用是___________ 。
(2)步骤③中发生反应的离子方程式为___________ 。
(3)步骤⑦中趁热过滤的目的是___________ 。步骤⑧中浓盐酸的作用是___________ 。
(4)产品的收率等于实际产量与理论产量之比,本实验的收率为___________ (保留三位有效数字)。
实验(二)测定[Co(NH3)6]Cl3产品的纯度。
用沉淀滴定法(又称莫尔法)测定产品中Cl-含量。实验原理如下:以K2CrO4为指示剂,用AgNO3标准溶液滴定Cl-。已知:Ksp ( AgCl)≈2.0× 10 -10,Ksp ( Ag2CrO4)≈9.0×10-12 ,Ag2CrO4为砖红色。
实验步骤:
①准确称取mg样品于锥形瓶中,加入去离子水完全溶解并配制成100mL溶液。
②准确量取25. 00 mL所配溶液于锥形瓶中,滴入2滴K2CrO4溶液,用c mol · L-1AgNO3溶液滴定至终点,消耗滴定液V mL。
(5)滴定终点的现象是___________ 。
(6)该样品纯度为___________ 。 若滴加指示剂过多,导致测得结果___________ (填“偏高” “偏低”或“无影响”)。
实验(一)制备[Co(NH3)6]Cl3产品。

(1)步骤②中活性炭的作用是
(2)步骤③中发生反应的离子方程式为
(3)步骤⑦中趁热过滤的目的是
(4)产品的收率等于实际产量与理论产量之比,本实验的收率为
实验(二)测定[Co(NH3)6]Cl3产品的纯度。
用沉淀滴定法(又称莫尔法)测定产品中Cl-含量。实验原理如下:以K2CrO4为指示剂,用AgNO3标准溶液滴定Cl-。已知:Ksp ( AgCl)≈2.0× 10 -10,Ksp ( Ag2CrO4)≈9.0×10-12 ,Ag2CrO4为砖红色。
实验步骤:
①准确称取mg样品于锥形瓶中,加入去离子水完全溶解并配制成100mL溶液。
②准确量取25. 00 mL所配溶液于锥形瓶中,滴入2滴K2CrO4溶液,用c mol · L-1AgNO3溶液滴定至终点,消耗滴定液V mL。
(5)滴定终点的现象是
(6)该样品纯度为
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
解题方法
10. 近日,中国科学技术大学的江海龙教授调控催化剂中钴的价态,高选择性进行光催化还原CO2制备HCOOH。
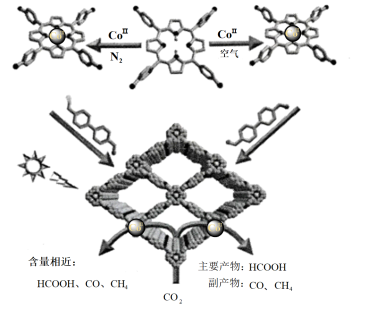
回答下列问题:
(1)根据图示可知,Co(II) →Co( III)中氧化剂是___________ ( 填化学式)。含Co(II)的催化剂对HCOOH的选择性___________ (填“ 高于”“低于”或“等于”)含Co( III)的催化剂。
(2)COF -367 – CoII和COF - 367 – CoIII催化CO2还原生成HCOOH的能垒图分别为a和b.注明: *代表吸附在催化剂表面,TS代表过渡态,能量单位为eV。

①CO2* +2H* =HCOOH * ΔH___________ 0(填“>”“<”或“=”)。
②在生成上述过渡态(TS)中,能垒最大为___________ eV。 COF - 367 – CoII和COF - 367 – CoIII中催化效能较高的是___________ (填“前者”或“后者”)。
(3)某催化剂作用下,CO2(g) + H2(g) HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。
HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。
 =
=___________ ,α___________ 50%(填“>”“<”或“=”)。
(4)在某催化剂作用下,向2 L恒容密闭反应器中充入1 mol CO2和2 mol H2发生如下反应:
主反应:CO2(g) +H2(g) HCOOH(g) ΔH >0
HCOOH(g) ΔH >0
副反应:CO2(g) +4H2(g) CH4(g) +2H2O(g) ΔH <0
CH4(g) +2H2O(g) ΔH <0
测得CO2的平衡转化率、HCOOH的选择性与温度关系如图所示。
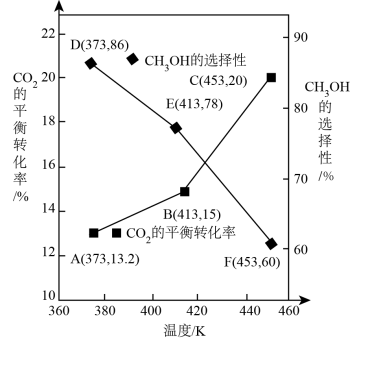
①已知:选择性等于HCOOH的物质的量与CO2转化的物质的量之比。其他条件不变,升高温度, CO2的平衡转化率增大的原因是___________ 。
②已知F点压强为27.2 kPa,主反应在F点对应的温度下,压强平衡常数Kp=___________ kPa-1(结果保留两位有效数字)。

回答下列问题:
(1)根据图示可知,Co(II) →Co( III)中氧化剂是
(2)COF -367 – CoII和COF - 367 – CoIII催化CO2还原生成HCOOH的能垒图分别为a和b.注明: *代表吸附在催化剂表面,TS代表过渡态,能量单位为eV。

①CO2* +2H* =HCOOH * ΔH
②在生成上述过渡态(TS)中,能垒最大为
(3)某催化剂作用下,CO2(g) + H2(g)
 HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。
HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。| 容器 | 起始投料/ mol | CO2的平衡转化率 | ||
| CO2 | H2 | HCOOH | ||
| 甲 | 1.0 | 1.0 | 0 | 50% |
| 乙 | 2.0 | 2.0 | 0 | α |
 =
=(4)在某催化剂作用下,向2 L恒容密闭反应器中充入1 mol CO2和2 mol H2发生如下反应:
主反应:CO2(g) +H2(g)
 HCOOH(g) ΔH >0
HCOOH(g) ΔH >0副反应:CO2(g) +4H2(g)
 CH4(g) +2H2O(g) ΔH <0
CH4(g) +2H2O(g) ΔH <0 测得CO2的平衡转化率、HCOOH的选择性与温度关系如图所示。

①已知:选择性等于HCOOH的物质的量与CO2转化的物质的量之比。其他条件不变,升高温度, CO2的平衡转化率增大的原因是
②已知F点压强为27.2 kPa,主反应在F点对应的温度下,压强平衡常数Kp=
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
解题方法
11. 近日,济南大学原长洲教授制备了一种高性能的钾离子电池负极材料( Bi - MOF),反应可简单表示为Bi( NO3)3·5H2O + BTC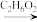 Bi – MOF。回答下列问题:
Bi – MOF。回答下列问题:
(1)铋(Bi)位于元素周期表中第6周期VA族,基态Bi原子的价层电子排布式为___________ 。
Bi(NO3)3中阴离子的立体构型为___________ 。基态O原子核外成对电子数与未成对电子数之比为___________ 。
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为___________ 。C2H5OH的沸点高于CH3OCH3,原因是___________ 。
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。
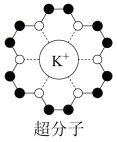
已知:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。超分子定义中的分子是广义的,包括离子。
①冠醚分子中C原子的杂化类型为___________ 。
②下列叙述正确的是___________ (填字母)。
A.含该超分子的物质属于分子晶体
B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变
D.冠醚与碱金属离子之间形成离子键
(4)铋的相关晶胞如图所示。
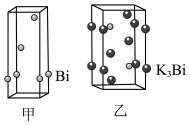
①等晶胞数的甲、乙中含铋原子数之比为___________ 。
②已知乙晶胞底边长为acm,高为bcm,NA为阿伏伽德罗常数的值。该晶体密度___________ g·cm-3(只列计算式)。
 Bi – MOF。回答下列问题:
Bi – MOF。回答下列问题:(1)铋(Bi)位于元素周期表中第6周期VA族,基态Bi原子的价层电子排布式为
Bi(NO3)3中阴离子的立体构型为
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。

已知:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。超分子定义中的分子是广义的,包括离子。
①冠醚分子中C原子的杂化类型为
②下列叙述正确的是
A.含该超分子的物质属于分子晶体
B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变
D.冠醚与碱金属离子之间形成离子键
(4)铋的相关晶胞如图所示。

①等晶胞数的甲、乙中含铋原子数之比为
②已知乙晶胞底边长为acm,高为bcm,NA为阿伏伽德罗常数的值。该晶体密度
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
解题方法
12. 某药物中间体H的合成路线如下(已知:D遇FeCl3溶液发生显色反应):
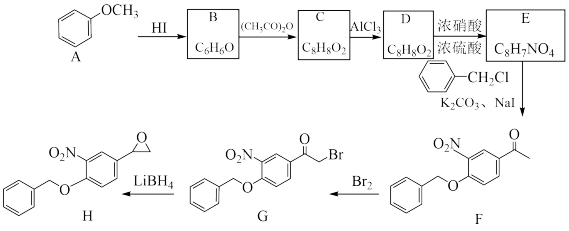
回答下列问题:
(1)H中所含官能团有___________ (填名称),B的名称为___________ 。
(2)F→G的反应类型是___________ 。A→B的副产物为___________ (填化学式)。
(3)B→C的化学方程式为___________ 。
(4)E→F中,K2CO3的作用是___________ 。
(5)T是C的芳香族同分异构体,能发生银镜反应且苯环上只有2个取代基的T的结构有___________ 种,其中在核磁共振氢谱上有4组峰且峰面积比为1:2:2:3的结构简式为___________ (写出一种即可)。
(6)设计以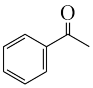 为原料制备
为原料制备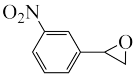 的合成路线
的合成路线___________ (无机试剂任选)。

回答下列问题:
(1)H中所含官能团有
(2)F→G的反应类型是
(3)B→C的化学方程式为
(4)E→F中,K2CO3的作用是
(5)T是C的芳香族同分异构体,能发生银镜反应且苯环上只有2个取代基的T的结构有
(6)设计以
 为原料制备
为原料制备 的合成路线
的合成路线
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、物质结构与性质、化学与STSE、化学反应原理、化学实验基础、有机化学基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 物理变化与化学变化 硅的物理性质与用途 几组常见同素异形体 化学科学对人类文明发展的意义 | |
| 2 | 0.4 | 氯气的实验室制法 难溶电解质的溶解平衡 沉淀溶解平衡的应用 物质性质实验方案的设计 | |
| 3 | 0.4 | 物质水溶液的导电性 氧化还原反应定义、本质及特征 化学科学对人类文明发展的意义 海水淡化 | |
| 4 | 0.65 | 有机官能团的性质及结构 同分异构现象、同分异构体的概念 分子的手性 | |
| 5 | 0.65 | 元素非金属性强弱的比较方法 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 常见金属的冶炼 | |
| 6 | 0.65 | 电解原理的理解及判断 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.65 | 同离子效应对难溶电解质溶解平衡的影响 沉淀的溶解与生成 溶度积常数相关计算 | |
| 二、解答题 | |||
| 8 | 0.4 | 氧化还原反应方程式的配平 原电池电极反应式书写 物质分离、提纯综合应用 探究物质组成或测量物质的含量 | 工业流程题 |
| 9 | 0.4 | 氧化还原反应方程式的配平 酸碱中和滴定原理的应用 物质分离、提纯综合应用 探究物质组成或测量物质的含量 | 工业流程题 |
| 10 | 0.4 | 碰撞理论及活化能 等效平衡理论的综合应用 化学平衡常数的有关计算 与转化率变化有关图像的分析 | 原理综合题 |
| 11 | 0.4 | 元素性质与电负性的关系 利用杂化轨道理论判断分子的空间构型 配合物的结构与性质 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 有机合成综合考查 | 有机推断题 |



