2. 油气开采、石油化工、煤化工等行业废气中普遍含有硫化氢,需要回收处理并加以利用。
I.已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ∆H1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ∆H2
③2H2(g)+O2(g)=2H2O(g) ∆H3
④2H2S(g)=S2(g)+2H2(g) ∆H4
(1)∆H
4=
___________(用∆H
1、∆H
2、∆H
3表示)。
(2)已知∆H
4>0,
___________有利于反应④正向自发进行。
A.低温 B.高温
(3)处理H
2S普遍采用的方法是克劳斯工艺,即利用反应①和②生成S
2;另一种方法是利用反应④分解H
2S。相比克劳斯工艺,分解法的优点是
___________,缺点是
___________。
II.在1373K、100 kPa下,分别将n(H2S):n(Ar)为4:1、1:1、1:4、1:9的H2S-Ar混合气体置于密闭容器中发生反应④,反应过程中H2S转化率随时间的变化如下图所示:
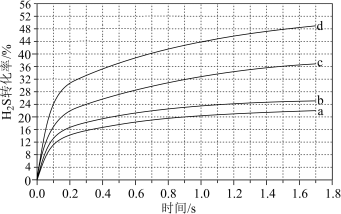
(4)n(H
2S):n(Ar)=1:9对应图中曲线
___________,理由是
___________。
A.a B.b C.c D.d
(5)n(H
2S):n(Ar)=1:4的混合气体投料后,若将温度升高至1473K,达到平衡时混合气体中H
2S与H
2的分压相等,H
2S平衡转化率为
___________。
III.在真空克劳斯法脱硫中,用K2CO3溶液吸收H2S。
电离平衡常数 | H2CO3 | H2S |
K1 | 4.2×10-7 | 5.6×10-8 |
K2 | 5.6×10-11 | 1.2×10-15 |
(6)下列关于K
2CO
3溶液中微粒关系正确的是___________。
A.c(OH-)>c(HCO ) ) | B.c(H+)>c(HCO ) ) |
C.c(OH-)=c(H+)+c(HCO )+2c(H2CO3) )+2c(H2CO3) | D.2c(K+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
(7)K
2CO
3溶液吸收少量H
2S的离子方程式为
___________。计算该反应的平衡常数K=
___________。