油气开采、石油化工、煤化工等行业废气中普遍含有硫化氢,需要回收处理并加以利用。
I.已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ∆H1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ∆H2
③2H2(g)+O2(g)=2H2O(g) ∆H3
④2H2S(g)=S2(g)+2H2(g) ∆H4
(1)∆H4=
(2)已知∆H4>0,
A.低温 B.高温
(3)处理H2S普遍采用的方法是克劳斯工艺,即利用反应①和②生成S2;另一种方法是利用反应④分解H2S。相比克劳斯工艺,分解法的优点是
II.在1373K、100 kPa下,分别将n(H2S):n(Ar)为4:1、1:1、1:4、1:9的H2S-Ar混合气体置于密闭容器中发生反应④,反应过程中H2S转化率随时间的变化如下图所示:
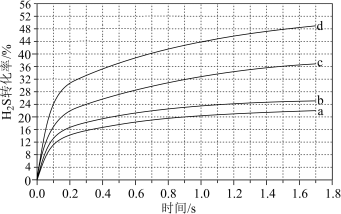
(4)n(H2S):n(Ar)=1:9对应图中曲线
A.a B.b C.c D.d
(5)n(H2S):n(Ar)=1:4的混合气体投料后,若将温度升高至1473K,达到平衡时混合气体中H2S与H2的分压相等,H2S平衡转化率为
III.在真空克劳斯法脱硫中,用K2CO3溶液吸收H2S。
电离平衡常数 | H2CO3 | H2S |
K1 | 4.2×10-7 | 5.6×10-8 |
K2 | 5.6×10-11 | 1.2×10-15 |
(6)下列关于K2CO3溶液中微粒关系正确的是___________。
A.c(OH-)>c(HCO ) ) | B.c(H+)>c(HCO ) ) |
C.c(OH-)=c(H+)+c(HCO )+2c(H2CO3) )+2c(H2CO3) | D.2c(K+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
(7)K2CO3溶液吸收少量H2S的离子方程式为
更新时间:2024-03-28 18:02:59
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】利用天然气及化工废气中的硫化氢,不仅可制取氢气并回收单质硫,还可减少对环境的污染。
回答下列问题:
(1)在一定的条件下,天然气脱硫工艺中会发生以下反应:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1
4H2S(g)+SO2(g)=3S2(g)+4H2O(g) ΔH2
2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH3
则相同条件下反应2S(g)=S2(g)的△H=_______ (用含△H1、△H2和△H3的代数式表示)。
(2)硫化氢分解反应2H2S(g) 2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:
2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:

①该反应的△H______ 0(填“>”、“<”)。
②为提高H2S的平衡分解率,除改变温度外,还可采取的措施是______________________________ 。
③图中A点时反应的平衡常数Kp=______ (用平衡分压代替浓度,平衡分压=总压×物质的量分数)。
(3)我国学者发明的一种分解硫化氢制氢并回收硫的装置如下图所示:
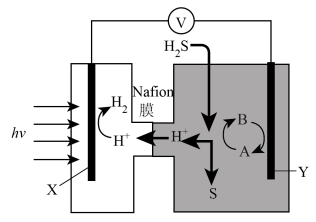
①该装置中能量转化的方式为____________________________________________________ 。
②若Y极液中的电对(A/B)选用I3-/I-,装置工作时Y极上的电极反应式为__________________________ ,Y极溶液中发生的离子反应为________________________________ ;再列举一种可作为Y极循环液常见的电对:_______________ 。
③该分解H2S制氢的方法主要优点是_____________________________________________________ 。
回答下列问题:
(1)在一定的条件下,天然气脱硫工艺中会发生以下反应:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1
4H2S(g)+SO2(g)=3S2(g)+4H2O(g) ΔH2
2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH3
则相同条件下反应2S(g)=S2(g)的△H=
(2)硫化氢分解反应2H2S(g)
 2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:
2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示: 
①该反应的△H
②为提高H2S的平衡分解率,除改变温度外,还可采取的措施是
③图中A点时反应的平衡常数Kp=
(3)我国学者发明的一种分解硫化氢制氢并回收硫的装置如下图所示:

①该装置中能量转化的方式为
②若Y极液中的电对(A/B)选用I3-/I-,装置工作时Y极上的电极反应式为
③该分解H2S制氢的方法主要优点是
您最近半年使用:0次
【推荐2】氨氮(NH3、NH4+等)是一种重要污染物,可利用合适的氧化剂氧化去除。
(1)氯气与水反应产生的HClO可去除废水中含有的NH3。
已知:NH3(aq)+HClO(aq)=NH2Cl(aq)+H2O(l) ΔH=a kJ·mol-1
2NH2Cl(aq)+HClO(aq)=N2(g)+H2O(l)+3H+(aq)+3Cl-(aq) ΔH=b kJ·mol-1
则反应2NH3(aq)+3HClO(aq)=N2(g)+3H2O(l)+3H+(aq)+3Cl-(aq)的ΔH=________ kJ·mol-1。
(2)在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响如图所示。
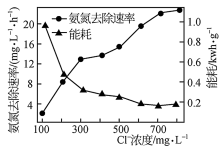
①写出电解时阳极的电极反应式:________________ 。
②当Cl-浓度减小时,氨氮去除速率下降,能耗却增加的原因是____________________________ 。
③保持加入NaCl的量不变,当废水的pH低于4时,氨氮去除速率也会降低的原因是____________________________ 。
(3)高铁酸钾(K2FeO4)是一种高效氧化剂,可用于氨氮处理。K2FeO4在干燥空气中和强碱性溶液中能稳定存在。氧化剂的氧化性受溶液中的H+浓度影响较大。
①碱性条件下K2FeO4可将水中的NH3转化为N2除去,该反应的离子方程式为________________________________ 。
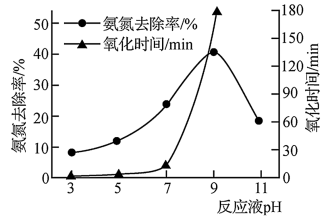
②用K2FeO4氧化含氨氮废水,其他条件相同时,废水pH对氧化氨氮去除率及氧化时间的影响如图所示。当pH小于9时,随着pH的增大,氨氮去除率增大、氧化时间明显增长的原因是_________________ 。
(1)氯气与水反应产生的HClO可去除废水中含有的NH3。
已知:NH3(aq)+HClO(aq)=NH2Cl(aq)+H2O(l) ΔH=a kJ·mol-1
2NH2Cl(aq)+HClO(aq)=N2(g)+H2O(l)+3H+(aq)+3Cl-(aq) ΔH=b kJ·mol-1
则反应2NH3(aq)+3HClO(aq)=N2(g)+3H2O(l)+3H+(aq)+3Cl-(aq)的ΔH=
(2)在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响如图所示。

①写出电解时阳极的电极反应式:
②当Cl-浓度减小时,氨氮去除速率下降,能耗却增加的原因是
③保持加入NaCl的量不变,当废水的pH低于4时,氨氮去除速率也会降低的原因是
(3)高铁酸钾(K2FeO4)是一种高效氧化剂,可用于氨氮处理。K2FeO4在干燥空气中和强碱性溶液中能稳定存在。氧化剂的氧化性受溶液中的H+浓度影响较大。
①碱性条件下K2FeO4可将水中的NH3转化为N2除去,该反应的离子方程式为
②用K2FeO4氧化含氨氮废水,其他条件相同时,废水pH对氧化氨氮去除率及氧化时间的影响如图所示。当pH小于9时,随着pH的增大,氨氮去除率增大、氧化时间明显增长的原因是

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】气态含氮化合物是把双刃剑,既是固氮的主要途径,也是大气污染物。气态含氮化合物及相关反应是新型科研热点。回答下列问题:
(1)用NH3催化还原NOx可以消除氮氧化物的污染。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-akJ/mol
②N2(g)+O2(g)=2NO(g) △H=-bkJ/mol
写出NH3还原NO至N2和水蒸气的热化学方程式___________ 。
(2)东南大学王金兰课题组提出合成氨的“表面氢化机理”如图所示,在较低的电压下实现氮气的还原合成氨。

已知:第一步:*H++e-=*H(快)(吸附在催化剂表而的物种用*表示)
第二步:N2+2*H=中间体(吸附在催化剂表面)(慢)
第三步:___________ (快)
第三步的方程式为,上述三步中的决速步为第二步,原因是___________ 。该法较传统工业合成氨法,具有能耗小、环境友好的优点。
(3)向一恒定温度的刚性密闭容器中充入物质的量之比为1:1的N2和H2混合气体,初始压强为30MPa,在不同催化剂作用下反应,相同时间内H2的转化率随温度的变化如图所示,b点v正___________ v逆(填“>”、“<”或“=”)。图中a点混合气体平均相对分子质量为18.75,a点对应温度下反应的平衡常数Kp=___________ (保留两位有效数字,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)

(1)用NH3催化还原NOx可以消除氮氧化物的污染。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-akJ/mol
②N2(g)+O2(g)=2NO(g) △H=-bkJ/mol
写出NH3还原NO至N2和水蒸气的热化学方程式
(2)东南大学王金兰课题组提出合成氨的“表面氢化机理”如图所示,在较低的电压下实现氮气的还原合成氨。

已知:第一步:*H++e-=*H(快)(吸附在催化剂表而的物种用*表示)
第二步:N2+2*H=中间体(吸附在催化剂表面)(慢)
第三步:
第三步的方程式为,上述三步中的决速步为第二步,原因是
(3)向一恒定温度的刚性密闭容器中充入物质的量之比为1:1的N2和H2混合气体,初始压强为30MPa,在不同催化剂作用下反应,相同时间内H2的转化率随温度的变化如图所示,b点v正

您最近半年使用:0次
【推荐1】碳的化合物在生产、生活中有着重要的作用。
(1)已知:2CO(g)+O2 (g)=2CO2 (g) △H1=-566kJ⋅mol-1
H2O(g)+CO(g)=H2 (g)+CO2 (g) △H2=-41kJ⋅mol-1
CO(g)+2H2 (g)=CH3 OH(g) △H3=-107kJ⋅mol-1
则2CO2 (g)+4H2 O(g)=2CH3 OH(g)+3O2 (g) △H=___________ kJ⋅mol-1
(2)T℃时,向容积为2L的恒容密闭容器中通入4.0molCO2和6.8molH2,发生反应:CO2 (g)+3H2 (g)⇌CH3 OH(g)+H2 O(g) △H=50kJ ⋅mol -1,5分钟时反应达到平衡,CO2的转化率为50%,回答下列问题:
①在0~5min内容器中v(H2)=___________ 。
②反应过程中,下列各项指标能表明A容器中反应的v正<v逆的是___________ (填标号)。
a.体系内的压强增大
b.气体的平均相对分子质量减小
c.H2 O(g)的物质的量增加
d.v正 (CO2)=v逆 (H2)
(3)T℃时,通入1.0 mol CO和3.0 mol H2于恒压密闭容器中,起始容积为2L,发生反应:CO(g)+2H2 (g)⇌CH3 OH(g)。5分钟时反应达到平衡,CO的转化率为50%,回答下列问题:
①该温度下上述反应的平衡常数K=___________ ;
②若达平衡后,再充入1.0 mol CO、4.0 mol H2、1.0 mol CH3 OH,平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(1)已知:2CO(g)+O2 (g)=2CO2 (g) △H1=-566kJ⋅mol-1
H2O(g)+CO(g)=H2 (g)+CO2 (g) △H2=-41kJ⋅mol-1
CO(g)+2H2 (g)=CH3 OH(g) △H3=-107kJ⋅mol-1
则2CO2 (g)+4H2 O(g)=2CH3 OH(g)+3O2 (g) △H=
(2)T℃时,向容积为2L的恒容密闭容器中通入4.0molCO2和6.8molH2,发生反应:CO2 (g)+3H2 (g)⇌CH3 OH(g)+H2 O(g) △H=50kJ ⋅mol -1,5分钟时反应达到平衡,CO2的转化率为50%,回答下列问题:
①在0~5min内容器中v(H2)=
②反应过程中,下列各项指标能表明A容器中反应的v正<v逆的是
a.体系内的压强增大
b.气体的平均相对分子质量减小
c.H2 O(g)的物质的量增加
d.v正 (CO2)=v逆 (H2)
(3)T℃时,通入1.0 mol CO和3.0 mol H2于恒压密闭容器中,起始容积为2L,发生反应:CO(g)+2H2 (g)⇌CH3 OH(g)。5分钟时反应达到平衡,CO的转化率为50%,回答下列问题:
①该温度下上述反应的平衡常数K=
②若达平衡后,再充入1.0 mol CO、4.0 mol H2、1.0 mol CH3 OH,平衡
您最近半年使用:0次
【推荐2】“一带一路”为中国化工企业开辟了新的国际市场,而能源、资源整合及环境治理是保驾护航的基础。
Ⅰ.在能源领域,科学家提出“绿色自由“”构想: 把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如下图所示:

(1)在合成塔中,若有4400gCO2与足量H2完企反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式__________ 。
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如下图所示:
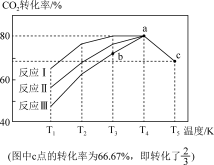
①催化剂效果最佳的反应是__________ (填“反应I”,“反应II”,“反应III”)。
②b点v (正)______ v (逆)(填 “>”, “<”, “=”)。
③c点时该反应的平衡常数K =_________ 。(写单位)
Ⅱ.环境治理中,安装汽车尾气催化转化器的反应是:2NO(g)+2CO(g)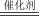 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0
(3)温度升高K值_______ (填“增大”或“减小”)
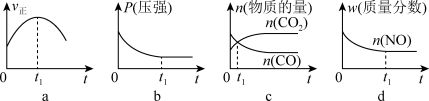
(4)若反应在恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____________ 。
(5)下列所示装置可以在吸收SO2的同时,用阴极排出的溶液吸收NO2,(电极均为惰性电极)
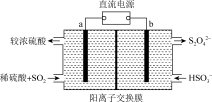
a极为______ 极(填“阴”、“阳”),b极的电极反应式为_________ ,结合电极反应式简述该装置能吸收SO2的原理:__________ 。
Ⅰ.在能源领域,科学家提出“绿色自由“”构想: 把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如下图所示:

(1)在合成塔中,若有4400gCO2与足量H2完企反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如下图所示:

①催化剂效果最佳的反应是
②b点v (正)
③c点时该反应的平衡常数K =
Ⅱ.环境治理中,安装汽车尾气催化转化器的反应是:2NO(g)+2CO(g)
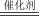 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0(3)温度升高K值
(4)若反应在恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是

(5)下列所示装置可以在吸收SO2的同时,用阴极排出的溶液吸收NO2,(电极均为惰性电极)

a极为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】还原法处理氮的氧化物是环境科学研究的热点课题。
I.氢气还原法。
H2还原NO发生的反应为:2NO(g)+2H2(g) N2(g)+2H2O(g)
N2(g)+2H2O(g)
(1)该反应速率表达式为v=kc2(NO)·c(H2)(k是速率常数,只与温度有关)。上述反应分两步进行:
反应1:2NO(g)+H2(g) N2(g)+H2O2(g)
N2(g)+H2O2(g)
反应2:H2O2(g)+H2(g) 2H2O(g)
2H2O(g)
总反应速率由反应较慢的一步决定,由此推知上述两步反应中,活化能较大的是反应___________ (填“1”或“2”)。c(NO)对总反应速率的影响程度___________ c(H2)(填“大于”“小于”或“等于”)。
II.NH3还原法。
在恒容密闭容器中充入NH3和NO2,在一定温度下发生反应:8NH3(g)+6NO2(g) N2(g)+12H2O(g)。
N2(g)+12H2O(g)。
(2)下列表明该反应达到平衡状态的是___________(填字母)。
III.CO还原法。
利用高效催化剂处理汽车尾气中的NO和CO,发生反应:2CO(g)+2NO(g) N2(g)+2CO2(g) ΔH。在2L恒容密闭容器中充入2molCO和2molNO,测得NO的转化率与温度、时间的关系如图:
N2(g)+2CO2(g) ΔH。在2L恒容密闭容器中充入2molCO和2molNO,测得NO的转化率与温度、时间的关系如图:
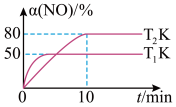
(3)下列说法正确的是___________(填字母)
(4)已知2NO2(g) N2O4(g),用分压p(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数
N2O4(g),用分压p(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数 。298K时,在体积固定的密闭容器中充入一定量的NO2,平衡时NO2的分压为100kPa。已知Kp=2.7×10-3kPa-1,则NO2的转化率为
。298K时,在体积固定的密闭容器中充入一定量的NO2,平衡时NO2的分压为100kPa。已知Kp=2.7×10-3kPa-1,则NO2的转化率为___________ 。
I.氢气还原法。
H2还原NO发生的反应为:2NO(g)+2H2(g)
 N2(g)+2H2O(g)
N2(g)+2H2O(g)(1)该反应速率表达式为v=kc2(NO)·c(H2)(k是速率常数,只与温度有关)。上述反应分两步进行:
反应1:2NO(g)+H2(g)
 N2(g)+H2O2(g)
N2(g)+H2O2(g)反应2:H2O2(g)+H2(g)
 2H2O(g)
2H2O(g)总反应速率由反应较慢的一步决定,由此推知上述两步反应中,活化能较大的是反应
II.NH3还原法。
在恒容密闭容器中充入NH3和NO2,在一定温度下发生反应:8NH3(g)+6NO2(g)
 N2(g)+12H2O(g)。
N2(g)+12H2O(g)。(2)下列表明该反应达到平衡状态的是___________(填字母)。
| A.混合气体密度保持不变 |
| B.NO2和N2的消耗速率之比为6:7 |
| C.混合气体中c(N2)=c(NO2) |
| D.混合气体压强保持不变 |
III.CO还原法。
利用高效催化剂处理汽车尾气中的NO和CO,发生反应:2CO(g)+2NO(g)
 N2(g)+2CO2(g) ΔH。在2L恒容密闭容器中充入2molCO和2molNO,测得NO的转化率与温度、时间的关系如图:
N2(g)+2CO2(g) ΔH。在2L恒容密闭容器中充入2molCO和2molNO,测得NO的转化率与温度、时间的关系如图:
(3)下列说法正确的是___________(填字母)
| A.图像中,T1>T2 |
| B.上述反应在高温下能自发进行 |
| C.增大NO的浓度,反应物的转化率增大 |
| D.10min时,T1K下平衡常数K=1 |
 N2O4(g),用分压p(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数
N2O4(g),用分压p(某组分的分压等于总压与其物质的量分数的积)表示的平衡常数 。298K时,在体积固定的密闭容器中充入一定量的NO2,平衡时NO2的分压为100kPa。已知Kp=2.7×10-3kPa-1,则NO2的转化率为
。298K时,在体积固定的密闭容器中充入一定量的NO2,平衡时NO2的分压为100kPa。已知Kp=2.7×10-3kPa-1,则NO2的转化率为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】Ⅰ:现有以下几种物质①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸钠、⑥亚硫酸氢钠、⑦氨水。请回答下列问题:
(1)以上物质属于弱电解质的是______ (填序号);
(2)常温下④的溶液pH______ 7(填>“<”或“=”),原因______ (用离子方程式表示);
(3)⑥的水溶液中呈酸性,原因是______ 。
(4)常温下,将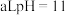 的
的 溶液与
溶液与 的
的 溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
______ 。
(5)已知:
a.常温下,醋酸和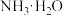 的电离平衡常数均为
的电离平衡常数均为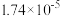 ;
;
b.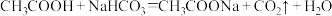
则 溶液呈
溶液呈______ 性(填“酸”、“碱”或“中”,下同), 溶液呈
溶液呈______ 性。
(6)对于醋酸溶液和醋酸钠溶液的下列说法正确的是______;
(1)以上物质属于弱电解质的是
(2)常温下④的溶液pH
(3)⑥的水溶液中呈酸性,原因是
(4)常温下,将
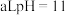 的
的 溶液与
溶液与 的
的 溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
(5)已知:
a.常温下,醋酸和
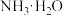 的电离平衡常数均为
的电离平衡常数均为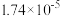 ;
;b.
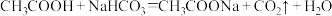
则
 溶液呈
溶液呈 溶液呈
溶液呈(6)对于醋酸溶液和醋酸钠溶液的下列说法正确的是______;
| A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小。 |
| B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解。 |
| C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离。 |
| D.常温下,醋酸和醋酸钠等体积等浓度混合,溶液呈碱性。 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】I. 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,
___________ (填“增大”“减小”或“不变”)。
(2)下列能使醋酸溶液中 的电离程度增大,而电离平衡常数不变的是___________。
的电离程度增大,而电离平衡常数不变的是___________。
(3)依上表数据写出向NaClO溶液中通少量 的离子方程式:
的离子方程式:___________ 。
(4)pH相同的NaClO和 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
____ NaClO(填“ ”“
”“ ”或“
”或“ ”,下同),两溶液中:c(Na+)−c(ClO-)
”,下同),两溶液中:c(Na+)−c(ClO-)____ c(K+)−c(CH3COO-)。
II.常温下,用0.2000mol•L-1盐酸滴定25mL0.2000mol•L-1Na2CO3溶液(溶液均为新配制),其滴定曲线如图所示(忽略溶液混合时体积和温度的变化)。回答下列问题:
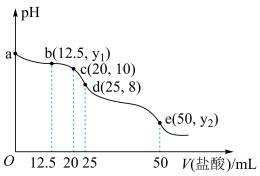
(5)往0.2000mol•L-1Na2CO3溶液中滴入2~3滴无色酚酞,溶液颜色会由无色变为________ ,判断的依据___________ (用离子方程式表示)。
(6)b点混合溶液中主要的溶质有Na2CO3、NaCl和___________ (填化学式),此时 =
=___________ 。
(7)c点混合溶液中,c(Na+)、c(CO )、(HCO
)、(HCO )、c(OH-)、c(H+)由大到小的顺序为
)、c(OH-)、c(H+)由大到小的顺序为___________ 。
(8)d点混合溶液中,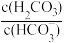 的数值是
的数值是___________ 。
 时,三种酸的电离平衡常数如下:
时,三种酸的电离平衡常数如下:| 化学式 | HClO |  |  |
| 电离平衡常数 |  |  | Ka1=4×10-7,Ka2=5×10-11 |
(1)一般情况下,当温度升高时,

(2)下列能使醋酸溶液中
 的电离程度增大,而电离平衡常数不变的是___________。
的电离程度增大,而电离平衡常数不变的是___________。| A.升高温度 | B.加水稀释 |
C.加少量的 固体 固体 | D.加少量氢氧化钠浓溶液 |
(3)依上表数据写出向NaClO溶液中通少量
 的离子方程式:
的离子方程式:(4)pH相同的NaClO和
 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
 ”“
”“ ”或“
”或“ ”,下同),两溶液中:c(Na+)−c(ClO-)
”,下同),两溶液中:c(Na+)−c(ClO-)II.常温下,用0.2000mol•L-1盐酸滴定25mL0.2000mol•L-1Na2CO3溶液(溶液均为新配制),其滴定曲线如图所示(忽略溶液混合时体积和温度的变化)。回答下列问题:

(5)往0.2000mol•L-1Na2CO3溶液中滴入2~3滴无色酚酞,溶液颜色会由无色变为
(6)b点混合溶液中主要的溶质有Na2CO3、NaCl和
 =
=(7)c点混合溶液中,c(Na+)、c(CO
 )、(HCO
)、(HCO )、c(OH-)、c(H+)由大到小的顺序为
)、c(OH-)、c(H+)由大到小的顺序为(8)d点混合溶液中,
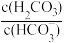 的数值是
的数值是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中
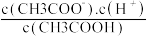
_______ (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式_______________________________ 。
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因_______________________ 。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为_______________________________ 。
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分 数随溶液pH变化的情况如下:
数随溶液pH变化的情况如下:
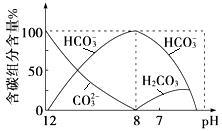
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-________ (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒有__________ 、_________ ,溶液中含量最多的三种微粒的物质的量浓度的大小关系为_______________________ ;
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中
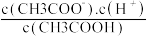
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分
 数随溶液pH变化的情况如下:
数随溶液pH变化的情况如下:
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-
②当pH=7时,溶液中含碳元素的主要微粒有
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】将锌铜合金溶解后与足量KI溶液反应(Zn2+不与I-反应),生成的I2用Na2S2O3标准溶液滴定,根据消耗的Na2S2O3溶液体积可测算合金中铜的含量。实验过程如下图所示:
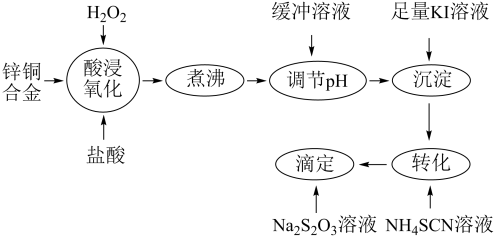
回答下列问题:
(1)H2O2的电子式为___________ ;“酸浸氧化”后铜元素的主要存在形式是___________ (填离子符号)。
(2)“煮沸”的目的是____________________________________________ 。
(3)用缓冲溶液“调pH”是为了避免溶液的酸性太强,否则“滴定”时发生反应的离子方程式:_______________________________________________________ ;
①若100mLNa2S2O3溶液发生上述反应时,20s后生成的SO2比S多6.4g,则v(Na2S2O3)=___________ mol/(L·s)(忽略溶液体积变化的影响)。
②该缓冲溶液是浓度均为0.10mol/L的CH3COOH和 CH3 COONH4的混合溶液。25℃时,溶液中各种离子浓度由大到小的顺序为_________________________________ 。(已知:25℃时,Ka(CH3COOH)=Kb(NH3·H2O)=1.8×10-5)
(4)“沉淀”步骤中有CuI沉淀产生,反应的离子方程式为______________________ 。
(5)“转化”步骤中,CuI转化为 CuSCN, CuSCN吸附I2的倾向比CuI更小,使“滴定”误差减小。沉淀完全转化后,溶液中c(SCN-):c(I-)≥___________ 。(已知:Ksp(CuI)=1.0×10-12;Ksp( CuSCN)=4.4×10-15)
(6)下列情况可能造成测得的铜含量偏高的是___________ (填标号)。
A.铜锌合金中含少量铁
B.“沉淀”时,I2与I-结合生成I3-:I2+ I-= I3-
C.“转化后的溶液在空气中放置太久,没有及时滴定
D.“滴定”过程中,往锥形瓶内加入少量蒸馏水

回答下列问题:
(1)H2O2的电子式为
(2)“煮沸”的目的是
(3)用缓冲溶液“调pH”是为了避免溶液的酸性太强,否则“滴定”时发生反应的离子方程式:
①若100mLNa2S2O3溶液发生上述反应时,20s后生成的SO2比S多6.4g,则v(Na2S2O3)=
②该缓冲溶液是浓度均为0.10mol/L的CH3COOH和 CH3 COONH4的混合溶液。25℃时,溶液中各种离子浓度由大到小的顺序为
(4)“沉淀”步骤中有CuI沉淀产生,反应的离子方程式为
(5)“转化”步骤中,CuI转化为 CuSCN, CuSCN吸附I2的倾向比CuI更小,使“滴定”误差减小。沉淀完全转化后,溶液中c(SCN-):c(I-)≥
(6)下列情况可能造成测得的铜含量偏高的是
A.铜锌合金中含少量铁
B.“沉淀”时,I2与I-结合生成I3-:I2+ I-= I3-
C.“转化后的溶液在空气中放置太久,没有及时滴定
D.“滴定”过程中,往锥形瓶内加入少量蒸馏水
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】通常用Ka表示弱酸的电离平衡常数,请回答下列问题:
(1)已知亚磷酸(H3PO3)为二元弱酸,常温下Ka1=1.6×10-2,Ka2=7×10-7。
①Na2HPO3属于___________ (填“正盐”或“酸式盐”)。
②已知常温下Ka(CH3COOH)=1.8×10-5,写出亚磷酸溶液与醋酸钠溶液反应的离子方程式___________ 。
(2)常温下,取0.3mol∙L-1HY溶液与0.3mol∙L-1NaOH溶液等体积混合 不计混合后溶液体积变化
不计混合后溶液体积变化 ,测得混合溶液pH=9
,测得混合溶液pH=9
①c(OH-)-c(HY)=____________ mol∙L-1
②常温下HY的电离平衡常数Ka=___________ 。
(3)电解法制取有广泛用途的Na2FeO4,工作原理如图所示。
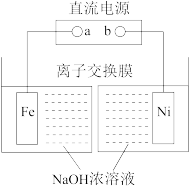
①a极为___________ 极。
②Ni极为___________ 极。
③左侧的电极反应式为___________ 。
④右侧的电极反应式为___________ 。
(1)已知亚磷酸(H3PO3)为二元弱酸,常温下Ka1=1.6×10-2,Ka2=7×10-7。
①Na2HPO3属于
②已知常温下Ka(CH3COOH)=1.8×10-5,写出亚磷酸溶液与醋酸钠溶液反应的离子方程式
(2)常温下,取0.3mol∙L-1HY溶液与0.3mol∙L-1NaOH溶液等体积混合
 不计混合后溶液体积变化
不计混合后溶液体积变化 ,测得混合溶液pH=9
,测得混合溶液pH=9 ①c(OH-)-c(HY)=
②常温下HY的电离平衡常数Ka=
(3)电解法制取有广泛用途的Na2FeO4,工作原理如图所示。

①a极为
②Ni极为
③左侧的电极反应式为
④右侧的电极反应式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题
(1)已知常温常压下,空气中的 溶于水达到平衡时,溶液的
溶于水达到平衡时,溶液的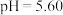 ,
,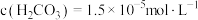 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的第一级电离的平衡常数
的第二级电离,则碳酸的第一级电离的平衡常数
_______ (已知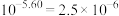 ,结果保留1位小数)。
,结果保留1位小数)。
(2)常温下0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。
(3)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10-7),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液的浓度为2×10-3 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为_______ 。
(4)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:
①若所得混合溶液为中性,则a:b=_______
②若所得混合溶液pH=3,则a:b=_______
(5)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为_______
(1)已知常温常压下,空气中的
 溶于水达到平衡时,溶液的
溶于水达到平衡时,溶液的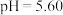 ,
,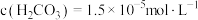 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的第一级电离的平衡常数
的第二级电离,则碳酸的第一级电离的平衡常数
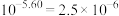 ,结果保留1位小数)。
,结果保留1位小数)。(2)常温下0.1mol/L的
 溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。A. | B. | C. | D. |
(4)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:
①若所得混合溶液为中性,则a:b=
②若所得混合溶液pH=3,则a:b=
(5)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为
您最近半年使用:0次



