2017届河北省张家口市蔚县一中高三第一学期期末教学质量监测化学试卷
河北
高三
期末
2017-04-01
380次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、有机化学基础、化学实验基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
| 选项 | 化学性质 | 实际应用 |
| A | 碳元素的非金属性比硅强 | 石英和碳粉的混合物高温下反应制备粗硅 |
| B | 乙醇能使蛋白质变性 | 无水乙醇作医用消毒剂 |
| C | 明矾溶液显酸性 | 明矾作净水剂 |
| D | 油脂在碱性条件下水解 | 热的NaOH溶液鉴别植物油和矿物油 |
| A.A | B.B | C.C | D.D |
| A.溶液和胶体的本质区别为是否能产生丁达尔效应 |
| B.K2Cr2O7溶液和氢溴酸能存放于同一药品橱内 |
| C.用带玻璃塞的细口试剂瓶保存氢氟酸 |
| D.CH4和C2H4均属于常用危险品中的易燃气体 |
| A.4.0g氦气中含有的最外层电子数为4NA |
| B.3.9g2H37Cl中含有的中子数为2.1NA |
| C.标准状况下,11.2L丙烷中含有的非极性键数目为NA |
| D.100mL1mol·L-1CH3COOH溶液中含有的分子数目大于0.1NA |
【知识点】 阿伏加德罗常数的求算解读
A.溶液中的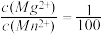 |
| B.若加入少量NaOH,Ksp[Mg(OH)2]和Ksp[Mn(OH)2]均减小 |
| C.若加入少量MgCl2,溶液中的c(Mg2+)和c(Mn2+)均增大 |
| D.若升高温度,Mg(OH)2和Mn(OH)2两种固体的质量均不变 |
A.加热TiCl4浓溶液制备TiO2·xH2O:Ti4++(x+2)H2O TiO2·xH2O+4H+ TiO2·xH2O+4H+ |
B.(NH4)2Fe(SO4)2溶液中加入少量KOH溶液: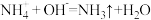 |
| C.钢铁发生吸氧腐蚀时的正极反应:O2+4H++4e-=2H2O |
| D.酸性KI溶液中通入O2:4H++2I-+O2=2H2O+I2 |
【知识点】 离子方程式的正误判断解读
| A.化学反应中,化学能全部转化为热能 |
B.已知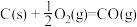 ΔH=-110.5kJ·mol-1,则碳的燃烧热为-110.5kJ·mol-1 ΔH=-110.5kJ·mol-1,则碳的燃烧热为-110.5kJ·mol-1 |
| C.测定中和热时,用铜制搅拌棒代替环形玻璃搅拌棒不影响测定结果 |
| D.反应C(s)+CO2(g)=2CO(g) ΔH>0在较高温度下能自发进行 |
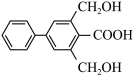 )的说法不正确的是
)的说法不正确的是| A.分子式为C15H14O4 |
| B.苯环上的一氯代物有7种 |
| C.能发生氧化反应和取代反应 |
| D.1molM与足量的Na反应,最多消耗3molNa |
【知识点】 多官能团有机物的结构与性质解读
| A.pH=4的CH3COOH溶液中,由水电离出来的c(H+)=1.0×10-4mol·L-1 |
B.物质的量浓度相等的①(NH4)2SO3溶液和②NH4HSO4溶液中的c( ):①<② ):①<② |
C.pH=3的0.1mol·L-1NaHC2O4溶液中: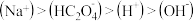 |
D.0.1mol·L-1的Na2CO3溶液中: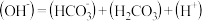 |
| 选项 | 操作 | 现象 | 结论 |
| A | 向等物质的量浓度的NaNO3溶液和Na2SiO3溶液中分别滴加3滴酚酞溶液 | NaNO3溶液为无色,Na2SiO3溶液变成红色 | 非金属性:N>Si |
| B | 将湿润的KI—淀粉试纸置于集满某气体的集气瓶口 | 试纸变蓝 | 该气体为Cl2 |
| C | 将浓盐酸滴入NaHSO3溶液,所得气体依次通过浓硫酸和CuSO4,收集气体 | CuSO4颜色未发生改变 | 收集到纯净的SO2 |
| D | 向含有少量FeCl3的FeCl2溶液中加入铜粉 | 铜粉有剩余 | 所得溶液中的溶质只有FeCl2 |
| A.A | B.B | C.C | D.D |
【知识点】 氯气 元素非金属性强弱的比较方法解读
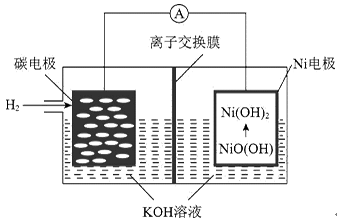
| A.离子交换膜选用阳离子交换膜(只允许阳离子通过) | B.正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
| C.导线中通过1mol电子时,理论上负极区溶液质量增加1g | D.充电时,碳电极与电源的正极相连 |
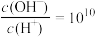 ;Z与W同周期,且W的最高正价与最低负价的代数和为4。下列说法中正确的是
;Z与W同周期,且W的最高正价与最低负价的代数和为4。下列说法中正确的是| A.原子半径:X<Y<Z<W |
| B.最简单氢化物的稳定性:Y>W |
| C.Z分别与Y、W组成的化合物中化学键类型均相同 |
| D.粘有W的单质的试管可用酒精洗涤 |
【知识点】 结合物质计算的元素周期律、元素周期表相关推断解读
 CO2(g)+2NH3(g) ΔH>0。5min达到平衡时,测得容器中NH2COONH4(s)的物质的量为0.2mol。下列说法正确的是
CO2(g)+2NH3(g) ΔH>0。5min达到平衡时,测得容器中NH2COONH4(s)的物质的量为0.2mol。下列说法正确的是| A.0~5min内,v(CO2)=0.16mol·L-1·min-1 |
| B.氨气体积分数不变时,该反应一定达到平衡状态 |
| C.平衡后,缩小容器容积,重新建立平衡时,c(CO2)增大 |
| D.其他条件不变,若将原容器改为绝热容器,则达到平衡时,NH2COONH4的转化率小于80% |
| A.2 | B.1 | C.0.5 | D.0.25 |
【知识点】 基于氧化还原反应守恒规律的计算解读

A.A点溶液中加少量水, 减小 减小 |
| B.原氨水的物质的量浓度约为1.006×10-2mol·L-1 |
| C.A、B、C三点溶液中水电离出来的c(OH-):A>B>C |
| D.C点时,盐酸和氨水恰好完全反应 |
【知识点】 酸碱中和滴定原理的应用解读
二、解答题 添加题型下试题
Ⅰ.制备AlN
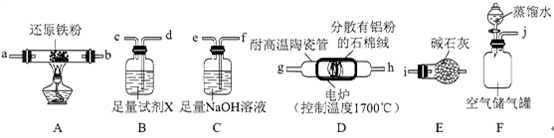
(1)实验时,以空气为原料制备AlN。按气流由左向右的方向,上述装置的正确连接顺序为j→
(2)上述装置中,需要检漏的仪器名称为
(3)试剂X的作用为
(4)装置D中发生反应的化学方程式为
Ⅱ.测定产品纯度
(5)设计实验证明:装置D的产品中含有Al单质
(6)测定产品纯度:取装置D中产品4.37g,加入足量NaOH浓溶液;通入水蒸气,将生成的气体全部蒸出,用V1mLc1mol·L-1的盐酸吸收;以酚酞作指示剂,用c2mol·L-1的NaOH标准溶液滴定过量的盐酸,达到滴定终点时,消耗V2mLNaOH标准溶液。则:
①达到滴定终点的现象为
②产品中A1N的质量分数为
【知识点】 探究物质组成或测量物质的含量解读 综合实验设计与评价解读

已知:
ⅰ.溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
ⅱ.相关试剂成分和价格如表1所示。
ⅲ.25℃时,该流程中金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表2所示。
表1
试剂 | 成分 | 价格/(元·吨-1) |
漂白液 | 含25.2%NaClO | 450 |
双氧水 | 含30%H2O2 | 2400 |
浓硝酸 | 含98%HNO3 | 1500 |
表2
氢氧化物 | 开始沉淀的pH | 沉淀完全的pH |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 4.0 | 6.5 |
请回答:
(1)FeCu4SiO5(OH)4用氧化物的形式可表示为
(2)结合题中信息,所选用的试剂1的名称为
(3)加入试剂2,需调节溶液的pH的合理范围为
A.Cu B.CuO
C.Cu(OH)2 D.Fe
(4)25℃时,Cu(OH)2的溶度积常数Ksp[Cu(OH)2]=
(5)CuSO4·5H2O溶液可用于电解精炼铜。电解精炼铜时,导线中通过9.632×104C的电量时,理论上阴极质量增加
三、填空题 添加题型下试题
 )在有机合成中占有重要的地位,有着广泛的用途。
)在有机合成中占有重要的地位,有着广泛的用途。已知:
①
 ΔH1=-54kJ·mol-1。
ΔH1=-54kJ·mol-1。②
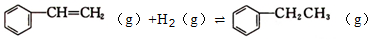 ΔH2=-121kJ·mol-1。
ΔH2=-121kJ·mol-1。③H2(g)+Cl2(g)=2HCl(g) ΔH3=-185kJ·mol-1。
④相关化学键的键能数据如表所示。
| 化学键 | C—H | C—C | C=C | C—Cl | H—Cl |
| 键能/(kJ·mol-1) | 412 | 348 | x | 341 | 432 |
请回答:
(1)根据化学反应原理,缩小容器容积对反应②的影响为
(2)根据反应①和表中数据计算,x=
(3)

①ΔH4=
②该反应正、逆反应平衡常数与温度的关系如图所示,其中表示正反应平衡常数K正的曲线为

④T1℃时,该反应的平衡常数K=
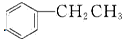 (g)、2molCl2(g)、1mol
(g)、2molCl2(g)、1mol (g)、2molHCl(g),则开始时,v正
(g)、2molHCl(g),则开始时,v正四、解答题 添加题型下试题
(1)基态Cu+的价层电子排布图为
(2)铁单质能形成Fe(CO)5,其熔点为-21℃,沸点为102.8℃。则Fe(CO)5晶体的类型为
(3)铜元素的焰色反应呈绿色,很多金属元素能发生焰色反应的微观原因为
(4)[Cu(NH3)4]SO4中,所含基态非金属原子的第一电离能由小到大的顺序为
(5)铁单质的一种晶体的堆积模型为体心立方堆积,晶胞参数为a pm;铜单质的一种晶体的堆积模型为面心立方最密堆积,晶胞参数为b pm。则两种晶体中,铁原子和铜原子的配位数之比为

已知:
①A是芳香烃的含氧衍生物,其蒸气密度是相同条件下氢气密度的54倍。
②有机物分子中,同一个碳原子上连接两个—OH不稳定,会自动失水。
③
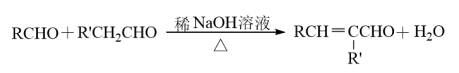 (R、R′表示烃基或氢原子)。
(R、R′表示烃基或氢原子)。请回答:
(1)A的化学名称为
(2)D中含氧官能团的名称为
(3)B→C时,第一步转化的反应类型为
(4)E→M的化学方程式为
(5)L是D的一种同系物,比D少1个碳原子且存在顺反异构;核磁共振氢谱中有6种吸收峰。则L的顺式结构简式为
(6)同时满足下列条件的E的同分异构体有
①苯环连有两个取代基
②能发生银镜反应
③能与NaHCO3反应生成CO2
试卷分析
试卷题型(共 19题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氧化还原反应的几组概念 明矾的净水作用及原理 油脂在碱性条件下水解 蛋白质的变性 | |
| 2 | 0.65 | 胶体的性质和应用 二氧化硅的化学性质 实验安全 | |
| 3 | 0.65 | 阿伏加德罗常数的求算 | |
| 4 | 0.4 | 溶度积规则及其应用 | |
| 5 | 0.65 | 离子方程式的正误判断 | |
| 6 | 0.65 | 反应焓变与热化学方程式的关系 中和热的测定与误差分析 | |
| 7 | 0.65 | 多官能团有机物的结构与性质 | |
| 8 | 0.4 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 9 | 0.4 | 氯气 元素非金属性强弱的比较方法 | |
| 10 | 0.4 | 电解原理的应用实验 | |
| 11 | 0.65 | 结合物质计算的元素周期律、元素周期表相关推断 | |
| 12 | 0.4 | 化学平衡状态的判断方法 温度对化学平衡移动的影响 压强对化学平衡移动的影响 | |
| 13 | 0.4 | 基于氧化还原反应守恒规律的计算 | |
| 14 | 0.4 | 酸碱中和滴定原理的应用 | |
| 二、解答题 | |||
| 15 | 0.65 | 探究物质组成或测量物质的含量 综合实验设计与评价 | 实验探究题 |
| 16 | 0.4 | 硅酸盐组成的表示方法 溶度积常数相关计算 铜的电解精炼 电解池有关计算 | 工业流程题 |
| 18 | 0.4 | 等电子原理的应用 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 19 | 0.4 | 有机反应类型 根据要求书写同分异构体 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 17 | 0.4 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡常数的影响因素及应用 化学平衡常数的有关计算 | |



