18. 研究化学反应原理对于生产生活是很有意义的:
(1)25℃时,醋酸溶液中CH
3COOH

CH
3COO
-+H
+;
Ka=1.75×10
-5,若向0.10 mol·L
-1CH
3COOH溶液中加入一定量的固体CH
3COONa(假设溶液体积不变),溶液中
c(CH
3COO
-)为1.0mol·L
-1,则溶液中
c(H
+)=
________mol·L
-1(计算结果保留小数点后两位数字)。溶液中各种离子浓度关系是
____________________________。
(2)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K
2SO
4溶液。
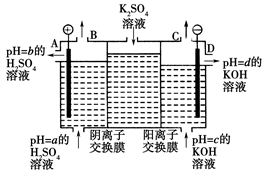
①该电解槽的阳极反应式为
____________,通过阴离子交换膜的离子数
____(填“>”“<”或“=”)通过阳离子交换膜的离子数;
②图中
a、
b、
c、
d分别表示有关溶液的pH,则
a、
b、
c、
d由小到大的顺序为
______;③电解一段时间后,B口与C口产生气体的质量比为
________。
(3)将CH
4设计成燃料电池,其利用率高,装置示意如图(A、B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。
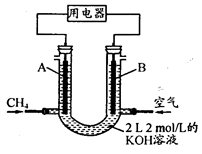
① O<V≤44.8 L时,电池总反应的化学方程式为
_____________ ;
② 44.8 L<V≤89.6 L时,负极的电极反应式为
_________________ ;
③ V=67.2 L时,溶液中各离子浓度的大小关系为
_____________________________。