【全国县级联考】甘肃省靖远县2018届高三第四次联考理科综合化学试题
甘肃
高三
模拟预测
2018-06-14
390次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学反应原理、常见无机物及其应用、化学实验基础
【全国县级联考】甘肃省靖远县2018届高三第四次联考理科综合化学试题
甘肃
高三
模拟预测
2018-06-14
390次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学反应原理、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 化学与生活密切相关。下列说法正确的是
| A.用活性炭去除冰箱中异味的过程属于化学变化 |
| B.食用花生油、葡萄糖和鸡蛋清均能发生水解反应 |
| C.古代造纸工艺中使用的明矾易导致纸张发生酸性腐蚀 |
| D.天然气、液化石油气和煤是我国目前推广使用的清洁燃料 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 设NA为阿伏伽德罗常数的数値,下列说法正确的是
| A.常温常压下,7.0g由丁烯与丙烯组成的混合气体中含有的氢原子数目为NA |
| B.向1L的密闭容器中充入46gNO2气体,容器中气体的分子数为NA |
| C.6.4g铜与足量的硫单质混合加热,转移电子的数目为0.2NA |
| D.标准状况下,2.24LSO3中含有0.1NA个SO3分子 |
您最近一年使用:0次
2018-06-06更新
|
172次组卷
|
7卷引用:【全国县级联考】甘肃省靖远县2018届高三第四次联考理科综合化学试题
单选题
|
适中(0.65)
4. 短周期主族元素a、b、c、d的原子序数依次增大,已知a、c同主族且c的原子序数是a的2倍,b元素的单质既能溶于稀硫酸、又能溶于氢氧化钠溶液。下列有关说法正确的是
| A.a的简单氢化物的沸点比c的高,且原子半径:a>c |
| B.b的简单离子与c的简单离子具有相同的电子层结构 |
| C.工业上通过电解b2a3或bd3均可得到b单质 |
| D.a与c形成的化合物的水溶液可使紫色石蕊试液变红 |
您最近一年使用:0次
2018-06-06更新
|
258次组卷
|
2卷引用:【全国县级联考】甘肃省靖远县2018届高三第四次联考理科综合化学试题
单选题
|
适中(0.65)
解题方法
5. 利用电化学原理还原CO2制取ZnC2O4的装置如图所示(电解液不参加反应),下列说法正确的是


| A.可用H2SO4溶液作电解液 |
| B.阳离子交换膜的主要作用是增强导电性 |
C.Pb电极的电极反应式是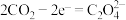 |
| D.工作电路中每流过0.02 mol电子,Zn电极质量减重0.65g |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. 25℃时,改变0.1mol/LRCOOH溶液的pH,溶液中RCOOH、RCOO-的微粒分布分数a(X)= c(X)/[c(RCOOH) + c(RCOO-)];甲酸(HCOOH)与丙酸(CH3CH2COOH)中酸分子的分布分数与pH 的关系如图所示。

下列说法正确的是

下列说法正确的是
| A.丙酸的酸性比甲酸强 |
B.CH3CH2COOH CH3CH2COO-+ H+ 的lgK=-4.88 CH3CH2COO-+ H+ 的lgK=-4.88 |
| C.若0.1mol/L 甲酸溶液的pH=2.33,则0.01mol/L 甲酸溶液的pH=3.33 |
| D.将0.1mol/L 的HCOOH溶液与0.1mol/L 的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c (HCOO-)>c(OH-)>c(H+) |
您最近一年使用:0次
2018-06-06更新
|
697次组卷
|
7卷引用:【全国省级联考】广东省2018届高三4月模拟考试(二模)理综化学试题
【全国省级联考】广东省2018届高三4月模拟考试(二模)理综化学试题【全国县级联考】甘肃省靖远县2018届高三第四次联考理科综合化学试题(已下线)高考母题题源08 电解质溶液【全国校级联考】湖南湖北八市十二校2019届高三第一次调研联考化学试题(已下线)专题8.1 弱电解质的电离平衡(练)-《2020年高考一轮复习讲练测》沪科版化学高二拓展性课程3《化学中的平衡》测试题安徽省滁州市定远县育才学校2022届高三5月教学质量检测理科综合化学试题
7. 下列实验操作、实验现象以及所得出的结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该溶液中可能含有 |
| B | 向NH3·H2O溶液中滴加少量AgNO3溶液 | 无明显现象 | NH3·H2O和AgNO3不反应 |
| C | 将木炭和浓硫酸共热生成的气体通入澄清石灰水中 | 澄清石灰水变浑浊 | 该气体只含CO2 |
| D | 向1mL.2mol/LNaOH溶液中先滴加2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/L FeCl3溶液 | 先生成白色沉淀,后生成红褐色沉淀 | Ksp[Fe(OH)3] <Ksp[ Mg(OH)2 ] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
解题方法
8. “分子筛”是一种具有多孔结构的铝硅酸盐(NaAlSiO4·nH2O),其中有许多笼状孔穴和通道,能让直径比孔穴小的分子通过而将大的分子留在外面,故此得名。利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备“分子筛”的一种工艺流程如下:

(1) “分子筛”的化学式用氧化物形式可表示为_______________ 。
(2)铝灰水解产生的气体为________ (填化学式),该气体分子中极性键的数目为___________ ;“水解”在加热条件下而不在室温下进行的原因是________________________ 。
(3) “酸溶”时,发生氧化还原反应的离子方程式为_________________________________ 。
(4)该工艺中滤渣的颜色为________________________ 。
(5)某学习小组设计实验模拟从浓缩海水(含Ca2+、Mg2+、SO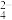 )中提取试剂级NaCl:
)中提取试剂级NaCl:

①实验中若向浓缩海水中加入的是Na2CO3浓溶液,则有难溶的Mg2(OH)2CO3生成,同时有气体逸出。该反应的离子方程式为__________________________________ 。
②该学习小组发现上述实验即使BaCl2用量不足,第Ⅲ步沉淀中依然含有少量BaCO3。从平衡角度分析其原因:_____________________________________________ 。

(1) “分子筛”的化学式用氧化物形式可表示为
(2)铝灰水解产生的气体为
(3) “酸溶”时,发生氧化还原反应的离子方程式为
(4)该工艺中滤渣的颜色为
(5)某学习小组设计实验模拟从浓缩海水(含Ca2+、Mg2+、SO
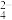 )中提取试剂级NaCl:
)中提取试剂级NaCl:
①实验中若向浓缩海水中加入的是Na2CO3浓溶液,则有难溶的Mg2(OH)2CO3生成,同时有气体逸出。该反应的离子方程式为
②该学习小组发现上述实验即使BaCl2用量不足,第Ⅲ步沉淀中依然含有少量BaCO3。从平衡角度分析其原因:
您最近一年使用:0次
2018-05-01更新
|
268次组卷
|
2卷引用:【全国市级联考】河南省新乡市2018届高三第三次模拟测试理综化学试题
9. 碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+ 15C+5N2=2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为_______ 。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3 (s)+ 3C(s)=Al2OC(s)+2CO(g) △H1
2Al2OC(s) + 3C(s)=Al4C3(s) + 2CO(g) △H2
2Al2O3 (s)+ 9C(s)= Al4C3 (s) + 6CO(g) △H3
①△H3=_______ (用△H1、△H2表示)。
②Al4C3可与足量盐酸反应制备一种最简单的烃,该反应的化学方程式为_______ 。
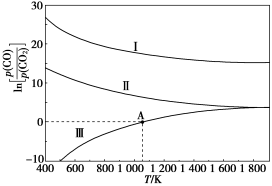
(3)下列是碳热还原制锰合金的三个反应,CO 与CO2平衡分压比的自然对数值(1nK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数。分压=总压× 气体的物质的量分数)。
I.Mn3C(s)+4CO2(g) 3MnO(s)+5CO(g) Kp(I)
3MnO(s)+5CO(g) Kp(I)
II.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(II)
MnO(s)+CO(g) Kp(II)
III.Mn3C(s) + CO2(g) 3Mn(s)+2CO(g) Kp(III)
3Mn(s)+2CO(g) Kp(III)
①△H>0 的反应是_______ (填“I”“II”或“III”)。
②1200 K时,在一体积为2L的恒容密闭容器中有17.7 gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min 内v (CO2)=_______ 。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应II,下列能说明反应II达到平衡的是_______ (填字母 )。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C 并充入0.1molCO2,若只发生反应III,则在A点反应达到平衡。当容器的总压为a kPa时,CO2的转化率为_______ ;A点对应温度下的Kp(III)=_______ 。
(1)一种制备氮氧化铝的反应原理为23Al2O3+ 15C+5N2=2Al23O27N5+15CO,产物Al23O27N5中氮的化合价为
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3 (s)+ 3C(s)=Al2OC(s)+2CO(g) △H1
2Al2OC(s) + 3C(s)=Al4C3(s) + 2CO(g) △H2
2Al2O3 (s)+ 9C(s)= Al4C3 (s) + 6CO(g) △H3
①△H3=
②Al4C3可与足量盐酸反应制备一种最简单的烃,该反应的化学方程式为
(3)下列是碳热还原制锰合金的三个反应,CO 与CO2平衡分压比的自然对数值(1nK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数。分压=总压× 气体的物质的量分数)。

I.Mn3C(s)+4CO2(g)
 3MnO(s)+5CO(g) Kp(I)
3MnO(s)+5CO(g) Kp(I)II.Mn(s)+CO2(g)
 MnO(s)+CO(g) Kp(II)
MnO(s)+CO(g) Kp(II)III.Mn3C(s) + CO2(g)
 3Mn(s)+2CO(g) Kp(III)
3Mn(s)+2CO(g) Kp(III)①△H>0 的反应是
②1200 K时,在一体积为2L的恒容密闭容器中有17.7 gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min 内v (CO2)=
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应II,下列能说明反应II达到平衡的是
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C 并充入0.1molCO2,若只发生反应III,则在A点反应达到平衡。当容器的总压为a kPa时,CO2的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
10. NiCl2是化工合成中最重要的镍源。实验室常用下列装置(夹持装置已略去)制备无水NiCl2。

实验步骤如下 :
I.按图示连接好装置,检查装置气密性后,先向装置中通入干燥的CO2。
II.约20 min后,停止通入CO2,改为通儒Cl2 并使装置中充满Cl2。
III.将电炉升温至750℃,在氯气流中加热约lh。
IV.在氯气流中冷却至室温后,再继续通入CO 2约10 min。
回答下列问题:
(1)仪器A的名称为_____________________________ 。
(2)步骤I中通入CO2 的目的是___________________________ 。
(3)A中生成Cl2 的离子方程式为______________________________________ 。
(4)判断步骤II中氧气已充满装置的现象是______________________________________ 。
(5)步骤IV中通入CO 2的目的是______________ ,水槽中NaOH 溶液的作用是_____________________ 。
(6)反应前石英管及瓷舟的总质量为m1、放入镍粉后石英管及瓷舟的总质量为m2,氧化反应后石英管及瓷舟的总质量为m3,则产品中n(Ni)/n(Cl)=________ (填计算表达式)。
(7)实验室也可用NiCl2·6H2O 与液态SOCl2 混合加热制取无水NiCl2,其反应的化学方程式为______________________ 。

实验步骤如下 :
I.按图示连接好装置,检查装置气密性后,先向装置中通入干燥的CO2。
II.约20 min后,停止通入CO2,改为通儒Cl2 并使装置中充满Cl2。
III.将电炉升温至750℃,在氯气流中加热约lh。
IV.在氯气流中冷却至室温后,再继续通入CO 2约10 min。
回答下列问题:
(1)仪器A的名称为
(2)步骤I中通入CO2 的目的是
(3)A中生成Cl2 的离子方程式为
(4)判断步骤II中氧气已充满装置的现象是
(5)步骤IV中通入CO 2的目的是
(6)反应前石英管及瓷舟的总质量为m1、放入镍粉后石英管及瓷舟的总质量为m2,氧化反应后石英管及瓷舟的总质量为m3,则产品中n(Ni)/n(Cl)=
(7)实验室也可用NiCl2·6H2O 与液态SOCl2 混合加热制取无水NiCl2,其反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. 世上万物,神奇可测。其性质与变化是物质的组成与结构发生了变化的结果。回答下列问题。
(1)根据杂化轨道理论判断,下列分子的空间构型是V形的是_________ (填字母)。
A.BeCl2 B.H2O C.HCHO D.CS2
(2)原子序数小于36的元素Q和T,在周期表中既位于同一周期又位于同一族,且T的原子序数比Q多2。T的基态原子的外围电子(价电子)排布式为_________________ ,Q2+的未成对电子数是______ 。
(3)铜及其合金是人类最早使用的金属材料,Cu2+能与NH3形成配位数为4的配合物[Cu(NH3)4]SO4
①铜元素在周期表中的位置是________________ ,[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能由大到小的顺序为_____________________ 。
②[Cu(NH3)4]SO4中,存在的化学键的类型有_______ (填字母)。
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
③NH3中N原子的杂化轨道类型是________ ,写出一种与SO42- 互为等电子体的分子的化学式:__________ 。
④[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个C1-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________________ 。
(4)氧与铜形成的某种离子晶体的晶胞如图所示,则该化合物的化学式为_________ 。若该晶体的密度为 ρ g·cm-3,则该晶体内铜离子与氧离子间的最近距离为_____________ (用含 ρ 的代数式表示,其中阿伏伽德罗常数用NA表示)cm。

(1)根据杂化轨道理论判断,下列分子的空间构型是V形的是
A.BeCl2 B.H2O C.HCHO D.CS2
(2)原子序数小于36的元素Q和T,在周期表中既位于同一周期又位于同一族,且T的原子序数比Q多2。T的基态原子的外围电子(价电子)排布式为
(3)铜及其合金是人类最早使用的金属材料,Cu2+能与NH3形成配位数为4的配合物[Cu(NH3)4]SO4
①铜元素在周期表中的位置是
②[Cu(NH3)4]SO4中,存在的化学键的类型有
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
③NH3中N原子的杂化轨道类型是
④[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个C1-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
(4)氧与铜形成的某种离子晶体的晶胞如图所示,则该化合物的化学式为

您最近一年使用:0次
2019-01-07更新
|
259次组卷
|
7卷引用:河北省邯郸市2018届高三第一次模拟考试理综-化学试题
解答题-有机推断题
|
适中(0.65)
名校
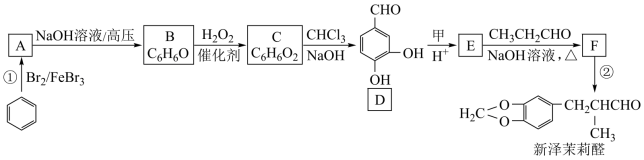
12. 新泽茉莉醛是一种名贵的香料。其合成路线如下:
已知:①RCHO+R'CH2CHO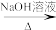
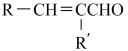 +H2O
+H2O
②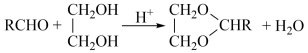
(1)已知甲的相对分子质量为30,甲的结构简式为___________ 。E中含氧官能团的名称是___________ 。
(2)反应②的反应类型是___________ 。
(3)写出反应①的化学方程式:___________ 。
(4)芳香族化合物G与E互为同分异构体,1molG能与足量NaHCO3溶液反应产生1mol气体,且G能发生银镜反应。则G的结构有___________ 种。其中一种结构苯环上的一氯代物有两种,且被氧化后能与C反应生成高分子化合物,写出该高分子化合物的结构简式:___________ 。
(5)结合已知①,设计以乙醇和苯甲醛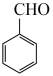 为原料(无机试剂任选)制备
为原料(无机试剂任选)制备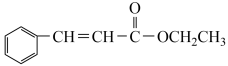 的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):___________ 。

已知:①RCHO+R'CH2CHO
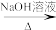
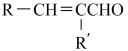 +H2O
+H2O②
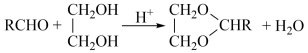
(1)已知甲的相对分子质量为30,甲的结构简式为
(2)反应②的反应类型是
(3)写出反应①的化学方程式:
(4)芳香族化合物G与E互为同分异构体,1molG能与足量NaHCO3溶液反应产生1mol气体,且G能发生银镜反应。则G的结构有
(5)结合已知①,设计以乙醇和苯甲醛
 为原料(无机试剂任选)制备
为原料(无机试剂任选)制备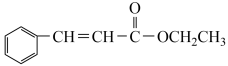 的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
您最近一年使用:0次
2018-03-24更新
|
435次组卷
|
6卷引用:河北省邯郸市2018届高三第一次模拟考试理综-化学试题
河北省邯郸市2018届高三第一次模拟考试理综-化学试题河北省武邑中学2018届高三下学期第二次质量检测化学试题2018届河南省新乡市高三第二次模拟测试化学试题河北省邢台市第二中学2018届高三下学期第二次月考理科综合化学试题【全国县级联考】甘肃省靖远县2018届高三第四次联考理科综合化学试题(已下线)易错31 官能团的性质和有机反应类型-备战2021年高考化学一轮复习易错题
试卷分析
整体难度:适中
考查范围:有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学反应原理、常见无机物及其应用、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 油脂 蛋白质 化学科学对人类文明发展的意义 煤的综合利用 | |
| 2 | 0.85 | 烷烃 烯烃 单烯烃的加成反应 | |
| 3 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合氧化还原反应知识与NA相关推算 | |
| 4 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 结合物质计算的元素周期律、元素周期表相关推断 | |
| 5 | 0.65 | 电解原理的应用 电解池电极反应式及化学方程式的书写与判断 | |
| 6 | 0.65 | 弱电解质的电离平衡 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 7 | 0.65 | 氨水 浓硫酸的强氧化性 硫酸根离子的检验 沉淀转化 | |
| 二、解答题 | |||
| 8 | 0.4 | 常见无机物的制备 | 工业流程题 |
| 9 | 0.65 | 化学反应原理综合考查 盖斯定律的应用 化学平衡状态的判断方法 化学平衡常数的概念及表达方式 | 原理综合题 |
| 10 | 0.65 | 氯气的实验室制法 氯气与金属单质的反应 物质制备的探究 | 实验探究题 |
| 11 | 0.65 | 电子排布式 利用杂化轨道理论判断分子的空间构型 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 根据题给物质选择合适合成路线 有机合成综合考查 有机推断综合考查 | 有机推断题 |



