弱电解质在水溶液中的电离状况可以进行定量计算和推测。
(1)25℃时两种酸的电离平衡常数如表所示。
①25℃时,0.100mol·L-1的NaA溶液中H+、OH-、Na+、A-、HA的物质的量浓度由大到小的顺序是:___ 。pH=8的NaA溶液中由水电离出的c(OH-)=___ mol·L-1。
②25℃时,0.100mol·L-1的NaHB溶液pH___ 7,理由是___ 。
③25℃时,向0.100mol·L-1的Na2B溶液中滴加足量0.100mol·L-1的HA溶液,反应的离子方程式为___ 。
(2)已知25℃时,向0.100mol·L-1的H3PO4溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。
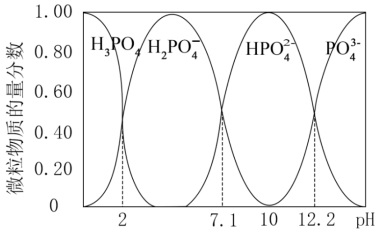
①当溶液pH由11到14时,所发生反应的离子方程式为:___ 。
(1)25℃时两种酸的电离平衡常数如表所示。
| Ka1 | Ka2 | |
| HA | 1×10-4 | |
| H2B | 1×10-2 | 5×10-6 |
①25℃时,0.100mol·L-1的NaA溶液中H+、OH-、Na+、A-、HA的物质的量浓度由大到小的顺序是:
②25℃时,0.100mol·L-1的NaHB溶液pH
③25℃时,向0.100mol·L-1的Na2B溶液中滴加足量0.100mol·L-1的HA溶液,反应的离子方程式为
(2)已知25℃时,向0.100mol·L-1的H3PO4溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变化的关系如图所示。

①当溶液pH由11到14时,所发生反应的离子方程式为:
更新时间:2020-04-10 15:46:44
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】用方铅矿精矿(主要为 )和软锰矿(主要为
)和软锰矿(主要为 ,还有少量
,还有少量 、
、 等杂质)制备
等杂质)制备 和
和 的工艺流程如图:
的工艺流程如图:

已知:① 。
。
②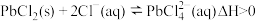 。
。
(1)80℃用盐酸处理两种矿石,为加快酸浸速率,还可采用的方法是____________ (任写一种)。
(2)向酸浸液中加入饱和食盐水的目的是_____________ ;加入物质X可用于调节酸浸液的 值,物质X可以是
值,物质X可以是___________ (填字母)。
A. B.
B. C.
C. D.
D.
(3)滤渣中含有两种金属杂质形成的化合物,其成分为___________ (写化学式)。
(4)向滤液2中通入 和
和 发生反应,写出总反应的离子方程式:
发生反应,写出总反应的离子方程式:________________ 。
(5)用 为原料可以获得金属锰,合适的冶炼方法为
为原料可以获得金属锰,合适的冶炼方法为____________ (填字母)。
A.热还原法 B.电解法 C.热分解法
 )和软锰矿(主要为
)和软锰矿(主要为 ,还有少量
,还有少量 、
、 等杂质)制备
等杂质)制备 和
和 的工艺流程如图:
的工艺流程如图:
已知:①
 。
。②
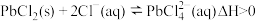 。
。(1)80℃用盐酸处理两种矿石,为加快酸浸速率,还可采用的方法是
(2)向酸浸液中加入饱和食盐水的目的是
 值,物质X可以是
值,物质X可以是A.
 B.
B. C.
C. D.
D.
(3)滤渣中含有两种金属杂质形成的化合物,其成分为
(4)向滤液2中通入
 和
和 发生反应,写出总反应的离子方程式:
发生反应,写出总反应的离子方程式:(5)用
 为原料可以获得金属锰,合适的冶炼方法为
为原料可以获得金属锰,合适的冶炼方法为A.热还原法 B.电解法 C.热分解法
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铁红( )常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为
)常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为 、
、 ,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:

回答下列问题:
(1)工业常将硫铁矿烧渣经过粉碎后再进行“酸浸”,其目的是_______ 。
(2)“酸浸”时加入的硫酸不宜过量太多的原因是_______ 。“酸浸”过程中主要反应的离子方程式为_______ 。
(3)“过滤1”所得滤液中含有的阳离子有_______ 。
(4)“过滤2”所得滤渣的主要成分为 和
和 ,所得滤液中的主要溶质是
,所得滤液中的主要溶质是_______ (填化学式)。
(5)写出 在空气中焙烧生成铁红的化学方程式:
在空气中焙烧生成铁红的化学方程式:_______ 。
(6)焙烧后的产物铁红中含有 ,欲验证其中存在
,欲验证其中存在 ,应选用的试剂是
,应选用的试剂是_______ 。
 )常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为
)常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为 、
、 ,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
回答下列问题:
(1)工业常将硫铁矿烧渣经过粉碎后再进行“酸浸”,其目的是
(2)“酸浸”时加入的硫酸不宜过量太多的原因是
(3)“过滤1”所得滤液中含有的阳离子有
(4)“过滤2”所得滤渣的主要成分为
 和
和 ,所得滤液中的主要溶质是
,所得滤液中的主要溶质是(5)写出
 在空气中焙烧生成铁红的化学方程式:
在空气中焙烧生成铁红的化学方程式:(6)焙烧后的产物铁红中含有
 ,欲验证其中存在
,欲验证其中存在 ,应选用的试剂是
,应选用的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。回答下列问题:
,探究其氧化还原性质。回答下列问题:
已知:
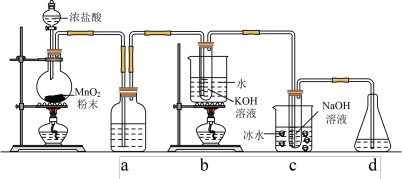
(1)制备氯气的离子方程式为___________ ,a中的试剂为___________ 。
(2)b中氧化剂和还原剂的质量比为___________ 。c中采用冰水浴冷却的目是___________ ,该反应的化学方程式是___________ 。
(3)d的作用是吸收多余的氯气,可选用试剂___________(填字母)。
(4)少量 和
和 溶液分别滴加到1号和2号淀粉
溶液分别滴加到1号和2号淀粉 试纸上。1号试纸颜色不变,2号试纸变
试纸上。1号试纸颜色不变,2号试纸变___________ 色。可知该条件下 的氧化能力
的氧化能力___________ (填“大于”或“小于”) 。
。
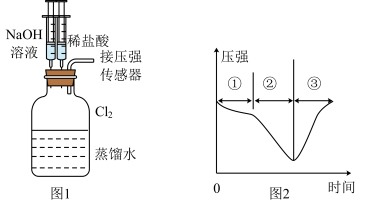
(5)用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________。
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________。
 和
和 ,探究其氧化还原性质。回答下列问题:
,探究其氧化还原性质。回答下列问题:已知:


(1)制备氯气的离子方程式为
(2)b中氧化剂和还原剂的质量比为
(3)d的作用是吸收多余的氯气,可选用试剂___________(填字母)。
A. | B. | C. | D. |
 和
和 溶液分别滴加到1号和2号淀粉
溶液分别滴加到1号和2号淀粉 试纸上。1号试纸颜色不变,2号试纸变
试纸上。1号试纸颜色不变,2号试纸变 的氧化能力
的氧化能力 。
。(5)用制得的氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加
 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________。
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________。
| A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应 |
| B.阶段②的压强变小,该过程发生了氧化还原反应 |
C.阶段③发生反应的离子方程式为 |
D.若将 换成 换成 ,所得的压强变化趋势与图2相似 ,所得的压强变化趋势与图2相似 |
您最近一年使用:0次
【推荐1】黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10mg/kg。一种制备黄雪盐的工艺如下:
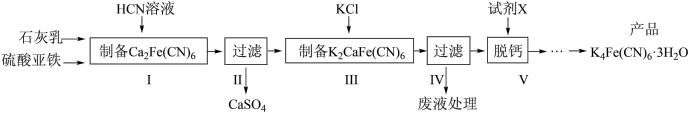
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为__________________________ 。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为____________ (填化学式)。
(3)步骤Ⅴ所用的试剂X是___________ 。(填化学式)
(4)工艺中用到剧毒的HCN溶液,含CN- 的废水必须处理后才能排放。
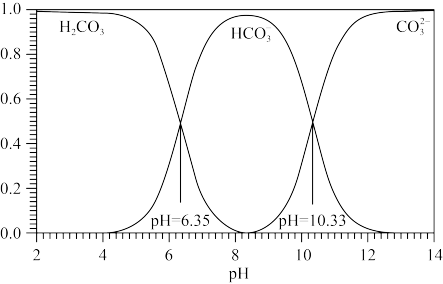
已知: HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:
①NaCN的电子式为___________ 。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是_______ ,第二步反应的离子方程式为____________ 。
(5)已知蓝色染料普鲁士蓝的合成方法如下:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如下:

若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请解释检测时试纸变蓝的原因:___________ 。
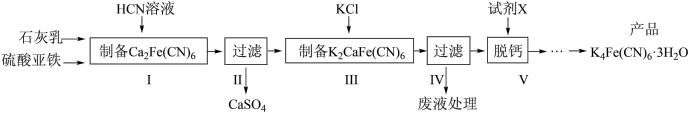
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为
(3)步骤Ⅴ所用的试剂X是
(4)工艺中用到剧毒的HCN溶液,含CN- 的废水必须处理后才能排放。
已知: HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:

①NaCN的电子式为
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是
(5)已知蓝色染料普鲁士蓝的合成方法如下:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如下:

若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请解释检测时试纸变蓝的原因:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】NaClO和KAl(SO4)2都是重要的化工产品,均可用于造纸业。
(1)NaClO溶液pH>7,用离子方程式表示原因_______ 。
(2)在纸浆中加入NaClO溶液的目的是_______ 。
(3)用如图装置探究饱和NaClO和KAl(SO4)2溶液反应的实验。打开活塞向烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式是________ 。

(4)下表为常温下浓度均为0.1mol/L的5种溶液的pH:
下列反应不能发生的是_______(填编号)。
(5)室温下,下列溶液中粒子的物质的量浓度关系正确的是_______。
(1)NaClO溶液pH>7,用离子方程式表示原因
(2)在纸浆中加入NaClO溶液的目的是
(3)用如图装置探究饱和NaClO和KAl(SO4)2溶液反应的实验。打开活塞向烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式是

(4)下表为常温下浓度均为0.1mol/L的5种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| A.CO2+H2O+2NaClO=Na2CO3+2HClO |
| B.CO2+H2O+NaClO=NaHCO3+HClO |
| C.CH3COOH+NaCN=CH3COONa+HCN |
| D.CH3COOH+NaClO=CH3COONa+HClO |
A.Na2CO3溶液:2c(Na+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| B.NaClO溶液:c(Na+)>c(ClO-)>c(OH-)>c(H+) |
C.NaHCO3溶液:c(H+)+c(HCO )+2c(H2CO3)=c(OH-) )+2c(H2CO3)=c(OH-) |
D.pH=2的HCl与pH=12的氨水等体积混合,所得溶液中:c(NH )+c(OH-)>c(Cl-)+c(H+) )+c(OH-)>c(Cl-)+c(H+) |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】气态亚硝酸( 或HONO)是大气中的一种污染物。
或HONO)是大气中的一种污染物。
(1)亚硝酸的电离平衡常数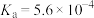 ,其电离方程式为
,其电离方程式为___________ 。
(2)亚硝酸进入人体可以与二甲胺[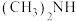 ]迅速反应生成亚硝酸胺[
]迅速反应生成亚硝酸胺[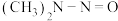 ],亚硝酸胺是一种化学致癌物。
],亚硝酸胺是一种化学致癌物。
①亚硝酸与二甲胺反应生成亚硝酸胺的一种反应机理如下:___________ 、消去反应。
②上述反应机理的反应过程与能量变化的关系如图所示。亚硝酸与二甲胺反应生成亚硝酸胺的△H___________ (填“>”或“<”)0。反应难度更大的是过程___________ (填“ⅰ”或“ⅱ”)。
①已知:
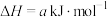 ;
;

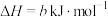 ;
;

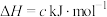 。
。
则反应 的∆H=
的∆H=___________  。
。
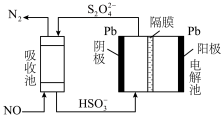
②用间接电化学法除去NO的过程如图所示。用离子方程式表示吸收池中除去NO的原理:___________ 。
 或HONO)是大气中的一种污染物。
或HONO)是大气中的一种污染物。(1)亚硝酸的电离平衡常数
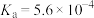 ,其电离方程式为
,其电离方程式为(2)亚硝酸进入人体可以与二甲胺[
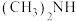 ]迅速反应生成亚硝酸胺[
]迅速反应生成亚硝酸胺[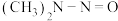 ],亚硝酸胺是一种化学致癌物。
],亚硝酸胺是一种化学致癌物。①亚硝酸与二甲胺反应生成亚硝酸胺的一种反应机理如下:
HONO+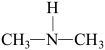

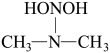


②上述反应机理的反应过程与能量变化的关系如图所示。亚硝酸与二甲胺反应生成亚硝酸胺的△H

①已知:

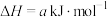 ;
;
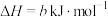 ;
;
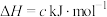 。
。则反应
 的∆H=
的∆H= 。
。②用间接电化学法除去NO的过程如图所示。用离子方程式表示吸收池中除去NO的原理:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】Ⅰ、某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸溶液分别加水稀释,其pH随加水体积的变化如图所示。
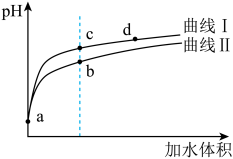
(1)曲线Ⅰ代表____ 溶液(填“HNO2”或“CH3COOH”,下同)。
(2)a点时,物质的量浓度较大的是______ 溶液。相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)较少的是_____ 。
(3)b、c两点溶液中水的电离程度较大的是___ (填“b”或“c”)。
(4)CH3COOH的稀释过程中,下列说法正确的是___ (填编号)。
a.CH3COOH的电离常数增大
b.H+的物质的量减小
c. 保持不变
保持不变
d. CH3COOH的电离程度增大,溶液的导电能力增强
Ⅱ、25℃,两种酸的电离平衡常数如表。
(5)HA-的电离平衡常数表达式K =_______ 。
(6)0.10 mol·L-1 NaHB溶液中H+、OH-、Na+、HB-的浓度由大到小的顺序为_______ 。
(7)等浓度的四种溶液:a. Na2A、b. NaHA、c. Na2B、d. NaHB的pH由大到小顺序是_______ (填字母)。

(1)曲线Ⅰ代表
(2)a点时,物质的量浓度较大的是
(3)b、c两点溶液中水的电离程度较大的是
(4)CH3COOH的稀释过程中,下列说法正确的是
a.CH3COOH的电离常数增大
b.H+的物质的量减小
c.
 保持不变
保持不变d. CH3COOH的电离程度增大,溶液的导电能力增强
Ⅱ、25℃,两种酸的电离平衡常数如表。
 |  | |
| H2A | 4.4×10-7 | 4.7×10-11 |
| H2B | 1.3×10-7 | 7.1×10-15 |
(5)HA-的电离平衡常数表达式K =
(6)0.10 mol·L-1 NaHB溶液中H+、OH-、Na+、HB-的浓度由大到小的顺序为
(7)等浓度的四种溶液:a. Na2A、b. NaHA、c. Na2B、d. NaHB的pH由大到小顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1) 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为_______ (写离子符号);若所得溶液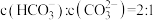 ,溶液
,溶液
_______ 。(室温下, 的
的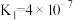 ;
;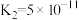 )
)
(2) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气:
①已知上述反应中相关的化学键键能数据如表:
则该反应的
_______ 。
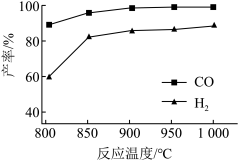
②按一定体积比加入 和
和 ,在恒压下发生反应,温度对
,在恒压下发生反应,温度对 和
和 产率的影响如图所示。此反应优选温度为900℃的原因是
产率的影响如图所示。此反应优选温度为900℃的原因是_______ 。
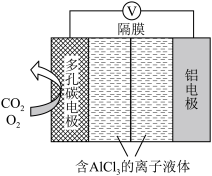
(3) 辅助的
辅助的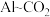 电池工作原理如图所示。该电池电容量大,能有效利用
电池工作原理如图所示。该电池电容量大,能有效利用 ,电池反应产物
,电池反应产物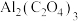 是重要的化工原料。电池的负极反应式:
是重要的化工原料。电池的负极反应式:_______ 。
 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:(1)
 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为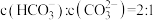 ,溶液
,溶液
 的
的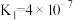 ;
;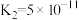 )
)(2)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气:
①已知上述反应中相关的化学键键能数据如表:
| 化学键 |  |  |  | 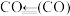 |
键能/ | 413 | 745 | 436 | 1075 |

②按一定体积比加入
 和
和 ,在恒压下发生反应,温度对
,在恒压下发生反应,温度对 和
和 产率的影响如图所示。此反应优选温度为900℃的原因是
产率的影响如图所示。此反应优选温度为900℃的原因是
(3)
 辅助的
辅助的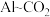 电池工作原理如图所示。该电池电容量大,能有效利用
电池工作原理如图所示。该电池电容量大,能有效利用 ,电池反应产物
,电池反应产物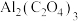 是重要的化工原料。电池的负极反应式:
是重要的化工原料。电池的负极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】(1)FeCl3溶液呈_______ 性,原因是__________ (用离子方程式表示)。把FeCl3溶液蒸干后并灼烧,最后得到的主要固体产物是_________ 。
(2)在25℃下,将a mol·L-1的CH3COOH与0.01 mol·L-1的NaOH等体积混合,反应平衡时溶液中c(CH3COO-)=c(Na+),则溶液显______ (填“酸”、“碱”或“中”)性;用含a的代数式表示CH3COOH的电离常数Ka=__________ 。
(3)已知298 K和101 kPa条件下:
N2(g)+3H2(g)=2NH3(g) ΔH1
2H2(g)+O2(g)=2H2O(l) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
4NH3(g)+O2(g)=2N2H4(l)+2H2O(l) ΔH4
则N2H4(l)的标准燃烧热ΔH=_______________ 。
(2)在25℃下,将a mol·L-1的CH3COOH与0.01 mol·L-1的NaOH等体积混合,反应平衡时溶液中c(CH3COO-)=c(Na+),则溶液显
(3)已知298 K和101 kPa条件下:
N2(g)+3H2(g)=2NH3(g) ΔH1
2H2(g)+O2(g)=2H2O(l) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
4NH3(g)+O2(g)=2N2H4(l)+2H2O(l) ΔH4
则N2H4(l)的标准燃烧热ΔH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】已知:草酸H2C2O4的Ka1=5.0×10-2, Ka2=5.4×10-5; Ksp(CaC2O4)=4.8×10-8
(1)在此溶液中逐滴滴加0.2mol/L的NaOH溶液,n( )的变化趋势是
)的变化趋势是_________________ 。
(2)用Ka1 、 Ka2、Kw 表示对应的K
① +2H+ =H2C2O4 K=
+2H+ =H2C2O4 K=____________ ② +OH- =
+OH- = +H2O K=
+H2O K=____________
③H2C2O4+ =2
=2 K=
K=____________
(3)0.1mol/L的Na2C2O4溶液100mL,该溶液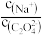
______ 2(填“>”、“<”或“=”,下同),向此溶液中加入草酸(H2C2O4)固体至pH=7,溶液中c( )
)_______ c( )。
)。
(4)在某温度下向含有草酸钙(CaC2O4)固体的CaC2O4饱和溶液中加入少量草酸(H2C2O4)固体,则CaC2O4的溶解量________ (填“增大”、“减小”或“不变”,下同),Ksp(CaC2O4)__________ ,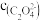
__________ 。
(5)将0.2mol/L的H2C2O4溶液与0.2mol/L的CaCl2溶液等体积混合,通过计算说明溶液中是否有沉淀生成_______ 。
(1)在此溶液中逐滴滴加0.2mol/L的NaOH溶液,n(
 )的变化趋势是
)的变化趋势是(2)用Ka1 、 Ka2、Kw 表示对应的K
①
 +2H+ =H2C2O4 K=
+2H+ =H2C2O4 K= +OH- =
+OH- = +H2O K=
+H2O K=③H2C2O4+
 =2
=2 K=
K=(3)0.1mol/L的Na2C2O4溶液100mL,该溶液
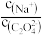
 )
) )。
)。(4)在某温度下向含有草酸钙(CaC2O4)固体的CaC2O4饱和溶液中加入少量草酸(H2C2O4)固体,则CaC2O4的溶解量
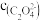
(5)将0.2mol/L的H2C2O4溶液与0.2mol/L的CaCl2溶液等体积混合,通过计算说明溶液中是否有沉淀生成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】SO2虽是大气污染物之一,但也是重要的工业原料,某同学在实验室设计如下实验,对SO2的部分性质进行了探究。
(1)二氧化硫的水溶液
①SO2易溶于水,常温常压下溶解度为1:40,其中有H2SO3生成。向SO2的饱和溶液中加入NaHSO3固体,有气体冒出,原因是_______ (结合有关平衡方程式简要说明)。
②欲验证酸性:H2SO3>HClO,选用下面的装置,其连接顺序为:A________ (按气流方向用大写字母表示即可)。能证明H2SO3的酸性强于HClO的实验现象为_________ 。

(2)①请设计简单实验方案比较室温下NaHSO3溶液中HSO 的电离平衡常数Ka与水解平衡常数Kb的相对大小:
的电离平衡常数Ka与水解平衡常数Kb的相对大小:________ 。
②25℃时,H2SO3 HSO
HSO +H+电离常数Ka=1×10-2mol·L-1,则该温度下pH=3、c(HSO
+H+电离常数Ka=1×10-2mol·L-1,则该温度下pH=3、c(HSO )=0.1mol·L-1的NaHSO3溶液中c(H2SO3)=
)=0.1mol·L-1的NaHSO3溶液中c(H2SO3)=_______ 。
(3)亚硫酰氯(俗称氯化亚砜,SOCl2)是一种液态化合物,沸点77℃,在农药、制药行业、有机合成等领域用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并常有刺激性气味的气体产生,实验室合成原理:SO2+Cl2+SCl2=2SOCl2。SOCl2与水反应的化学方程式为____ 。蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合加热可得到无水AlCl3,试解释原因:_______ 。
(1)二氧化硫的水溶液
①SO2易溶于水,常温常压下溶解度为1:40,其中有H2SO3生成。向SO2的饱和溶液中加入NaHSO3固体,有气体冒出,原因是
②欲验证酸性:H2SO3>HClO,选用下面的装置,其连接顺序为:A

(2)①请设计简单实验方案比较室温下NaHSO3溶液中HSO
 的电离平衡常数Ka与水解平衡常数Kb的相对大小:
的电离平衡常数Ka与水解平衡常数Kb的相对大小:②25℃时,H2SO3
 HSO
HSO +H+电离常数Ka=1×10-2mol·L-1,则该温度下pH=3、c(HSO
+H+电离常数Ka=1×10-2mol·L-1,则该温度下pH=3、c(HSO )=0.1mol·L-1的NaHSO3溶液中c(H2SO3)=
)=0.1mol·L-1的NaHSO3溶液中c(H2SO3)=(3)亚硫酰氯(俗称氯化亚砜,SOCl2)是一种液态化合物,沸点77℃,在农药、制药行业、有机合成等领域用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并常有刺激性气味的气体产生,实验室合成原理:SO2+Cl2+SCl2=2SOCl2。SOCl2与水反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】已知:常温下各物质的电离平衡常数见下表,按要求填空。
(1)常温下,实验测得醋酸铵溶液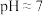 ,溶液呈中性,请用具体数据解释醋酸铵溶液显中性的原因
,溶液呈中性,请用具体数据解释醋酸铵溶液显中性的原因_______ 。此溶液中水电离的
_______  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(2)①25℃时,等浓度的a. 溶液b.
溶液b. 溶液c.
溶液c. 溶液,三种溶液的
溶液,三种溶液的 由大到小的顺序为
由大到小的顺序为_______ (填溶液前字母)
② 相同的
相同的 溶液与
溶液与 溶液相比,
溶液相比,
_______ 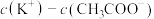 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
③写出将少量 通入
通入 溶液中的离子方程式
溶液中的离子方程式_______ 。
(3)室温下,若将 盐酸滴入
盐酸滴入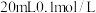 氨水中,溶液
氨水中,溶液 随加入盐酸体积的变化曲线如图所示。
随加入盐酸体积的变化曲线如图所示。
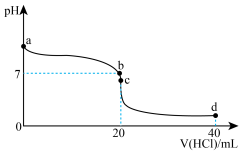
①b点所示溶液中的溶质是_______ 。
②若用 盐酸滴定未知浓度的氨水,混合溶液的
盐酸滴定未知浓度的氨水,混合溶液的 变化图。由此得出的结论错误的是
变化图。由此得出的结论错误的是_______
A.a点溶液的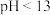
B.b点对应的溶液中:
C.d点对应的溶液中:
D.若用盐酸溶液滴定氨水溶液,可选用酚酞作指示剂
| 化学式 |  |  |  |  |
| 电离平衡常数 | 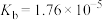 | 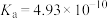 | 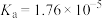 | 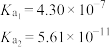 |
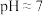 ,溶液呈中性,请用具体数据解释醋酸铵溶液显中性的原因
,溶液呈中性,请用具体数据解释醋酸铵溶液显中性的原因
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(2)①25℃时,等浓度的a.
 溶液b.
溶液b. 溶液c.
溶液c. 溶液,三种溶液的
溶液,三种溶液的 由大到小的顺序为
由大到小的顺序为②
 相同的
相同的 溶液与
溶液与 溶液相比,
溶液相比,
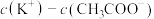 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)③写出将少量
 通入
通入 溶液中的离子方程式
溶液中的离子方程式(3)室温下,若将
 盐酸滴入
盐酸滴入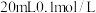 氨水中,溶液
氨水中,溶液 随加入盐酸体积的变化曲线如图所示。
随加入盐酸体积的变化曲线如图所示。
①b点所示溶液中的溶质是
②若用
 盐酸滴定未知浓度的氨水,混合溶液的
盐酸滴定未知浓度的氨水,混合溶液的 变化图。由此得出的结论错误的是
变化图。由此得出的结论错误的是A.a点溶液的
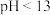
B.b点对应的溶液中:

C.d点对应的溶液中:

D.若用盐酸溶液滴定氨水溶液,可选用酚酞作指示剂
您最近一年使用:0次



