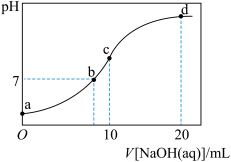
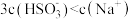25℃时,在20mL0.1mol·L-1一元弱酸HA溶液中滴加0.1mol·L-1NaOH溶液,溶液中1g 与pH关系如图所示。下列说法不正确的是
与pH关系如图所示。下列说法不正确的是
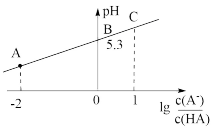
 与pH关系如图所示。下列说法不正确的是
与pH关系如图所示。下列说法不正确的是
| A.A点对应溶液中:c(A-)>c(Na+)>c(H+)>c(OH-) |
| B.25℃时,HA酸的电离常数的数量级为 10-6 |
C.对C点溶液加水稀释,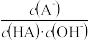 一定减小 一定减小 |
| D.当加入NaOH溶液体积为10 mL时,水的电离受到了抑制 |
2020·四川乐山·模拟预测 查看更多[2]
更新时间:2020-07-06 16:18:05
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述中正确的是
A.25℃时, 的盐溶液一定促进水的电离 的盐溶液一定促进水的电离 |
B.同体积浓度分别为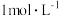 、 、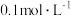 的醋酸,含H+的物质的量分别为amol、bmol,则 的醋酸,含H+的物质的量分别为amol、bmol,则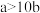 |
C.常温下,pH=4.75、浓度均为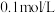 的 的 、 、 混合溶液: 混合溶液: 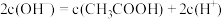 |
D.常温下,向 溶液中通入 溶液中通入 至中性: 至中性: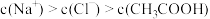 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,下列各组离子在指定溶液中能大量共存的是
A.pH=2的溶液:Na+、Fe2+、I-、 |
B.c(NaAlO2)=0.1 mol/L的溶液:K+、OH-、Cl-、 |
C.常温下pH=7的溶液中:K+、 、Al3+、Cl- 、Al3+、Cl- |
D.由水电离出的c(H+)=1.0×10-12 mol·L-1的溶液:Na+、ClO-、 、K+ 、K+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知亚硒酸(H2SeO3)为二元弱酸,常温下,向某浓度的亚硒酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中H2SeO3、 、
、 三种微粒的物质的量分数与溶液pH的关系如图所示。下列说法不正确的是
三种微粒的物质的量分数与溶液pH的关系如图所示。下列说法不正确的是
 、
、 三种微粒的物质的量分数与溶液pH的关系如图所示。下列说法不正确的是
三种微粒的物质的量分数与溶液pH的关系如图所示。下列说法不正确的是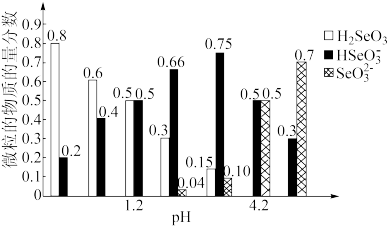
| A.常温下,亚硒酸的电离平衡常数Ka1=10-1.2 |
| B.向pH=1.2的溶液中滴加NaOH溶液至pH=4.2的过程中水的电离程度一直增大 |
| C.NaHSeO3溶液pH>7 |
D.pH=4.2时,溶液中c(Na+ )+c(H+ )=c(OH- )+3c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温时,有关 的计算结果一定正确的是
的计算结果一定正确的是
①强酸 ,加水稀释到
,加水稀释到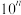 倍,则
倍,则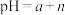
②弱酸 ,加水稀释到
,加水稀释到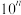 倍,则
倍,则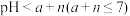
③强酸 ,加水稀释到
,加水稀释到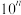 倍,则
倍,则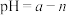
④弱酸 ,加水稀释到
,加水稀释到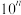 倍,则
倍,则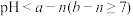
 的计算结果一定正确的是
的计算结果一定正确的是①强酸
 ,加水稀释到
,加水稀释到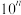 倍,则
倍,则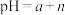
②弱酸
 ,加水稀释到
,加水稀释到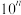 倍,则
倍,则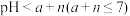
③强酸
 ,加水稀释到
,加水稀释到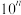 倍,则
倍,则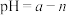
④弱酸
 ,加水稀释到
,加水稀释到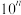 倍,则
倍,则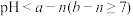
| A.①② | B.②③ |
| C.③④ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,向50 mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图象如下图所示。下列说法正确的是
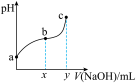
A.若a点pH=4,且c(Cl-)=m·c(ClO-),则Ka(HClO)=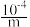 |
| B.若x=100,b点对应溶液中:c(OH-)>c(H+),可用pH试纸测定其pH |
C.b~c段,随NaOH溶液的滴入,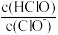 逐渐增大 逐渐增大 |
| D.若y=200,c点对应溶液中:c(OH-)-c(H+)=2c(Cl-)+c(HClO) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】有关25℃时的下列溶液,有关说法正确的是
| A.HCl溶液酸性一定强于NH4Cl溶液 |
| B.NaHA溶液呈酸性,可以推测H2A为强酸 |
| C.0.010mol/L、0.10mol/L的醋酸溶液,醋酸的电离度分别为α1、α2,则α1<α2 |
| D.100mL pH=10的Na2CO3溶液,水电离出OH-的物质的量为1.0×10-5mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各项比较中正确的是
A.微粒半径: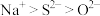 |
B.结合质子的能力: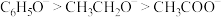 |
C.固体的热稳定性: |
D.相同物质的量浓度溶液中 : :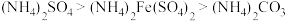 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,向10.00mL0.2000mol·L-1NH4Cl溶液中逐滴加入0.2000mol·L-1NaOH溶液,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑溶液混合时体积和温度的变化,不考虑操作过程中质量的损失),下列说法正确的是
A.a点溶液中, <1 <1 |
B.b点溶液中,c(Na+)+c(Cl-)+c(NH3·H2O)=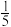 mol·L-1 mol·L-1 |
C.c点溶液中,c(Na+)=2c( )+2c(NH3·H2O) )+2c(NH3·H2O) |
D.d点溶液中,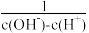 <15 <15 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
A.常温下, 的 的 溶液中,由水电离的 溶液中,由水电离的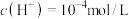 |
B.将 的HCl溶液和 的HCl溶液和 的 的 溶液等体积混合,所得溶液 溶液等体积混合,所得溶液 |
C. 氨水和 氨水和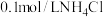 溶液等体积混合后所得溶液 溶液等体积混合后所得溶液 ,则 ,则 |
D.向 、 、 的NaHA溶液中加入NaOH溶液反应的离子方程式为: 的NaHA溶液中加入NaOH溶液反应的离子方程式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】盐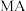 溶于水存在如图过程,下列说法正确的是
溶于水存在如图过程,下列说法正确的是
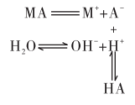
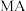 溶于水存在如图过程,下列说法正确的是
溶于水存在如图过程,下列说法正确的是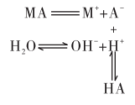
A.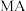 是弱电解质 是弱电解质 |
B.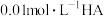 溶液的 溶液的 |
C. 与 与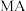 的混合溶液中其离子浓度大小关系可能为: 的混合溶液中其离子浓度大小关系可能为: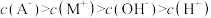 |
D.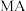 溶液中一定存在 溶液中一定存在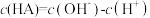 |
您最近一年使用:0次

 )是一种二元弱酸。常温下向草酸溶液中滴加
)是一种二元弱酸。常温下向草酸溶液中滴加 溶液,混合溶液中
溶液,混合溶液中 [X表示
[X表示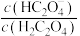 或
或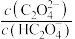 ]随溶液pH的变化如图所示。下列说法中错误的是
]随溶液pH的变化如图所示。下列说法中错误的是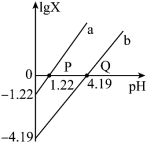
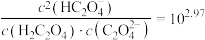
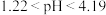 时,均有
时,均有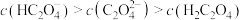
 时,溶液中
时,溶液中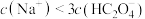
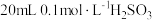 溶液中滴加
溶液中滴加 的
的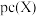 [
[ ](
](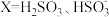 或
或 )随V(
)随V(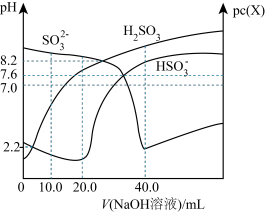
 的第一步电离平衡常数
的第一步电离平衡常数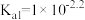
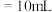 时,
时,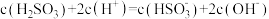
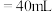 时,水的电离程度最大
时,水的电离程度最大 时,有
时,有