按要求回答下列问题:
(1)实验室中常用NaOH溶液来进行洗气和提纯,当用100 mL 3 mol/L的NaOH溶液吸收标准状况下4.48 L CO2时,所得溶液中各离子浓度由大到小的顺序为___________ 。
(2)常温下向一定体积的0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是___________ (填字母,下同)。
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中 不变
不变
D.当溶液极稀时,溶液中 减小
减小
(3)t ℃时,某稀硫酸溶液中c(H+)=10﹣a mol•L﹣1,c(OH﹣)=10﹣b mol•L﹣1,已知a+b=13。
①该温度下水的离子积常数Kw的数值为___________ 。
②该温度下(t ℃),将100 mL 0.1 mol•L﹣1的稀H2SO4与100 mL 0.4 mol•L﹣1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=___________ 。
(4)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的主要离子方程式为___________ ,由水电离出的c(OH﹣)=___________ mol•L﹣1。
(5)常温下,几种离子开始沉淀时的pH如表所示:
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液时,___________ (填离子符号)先沉淀,Ksp[Fe(OH)2]_______ Ksp[Mg(OH)2](填“>”、“=”或“<”)。
(1)实验室中常用NaOH溶液来进行洗气和提纯,当用100 mL 3 mol/L的NaOH溶液吸收标准状况下4.48 L CO2时,所得溶液中各离子浓度由大到小的顺序为
(2)常温下向一定体积的0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中
 不变
不变D.当溶液极稀时,溶液中
 减小
减小(3)t ℃时,某稀硫酸溶液中c(H+)=10﹣a mol•L﹣1,c(OH﹣)=10﹣b mol•L﹣1,已知a+b=13。
①该温度下水的离子积常数Kw的数值为
②该温度下(t ℃),将100 mL 0.1 mol•L﹣1的稀H2SO4与100 mL 0.4 mol•L﹣1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=
(4)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的主要离子方程式为
(5)常温下,几种离子开始沉淀时的pH如表所示:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液时,
更新时间:2020-12-22 19:37:45
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?________________________________________________
(2)c1________ (填“<”、“>”或“=”)0.2 mol·L-1。乙组实验中HA和NaOH溶液混合前,HA溶液中 与NaOH溶液中
与NaOH溶液中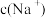 的关系是
的关系是________ (从下面选项中选择填空)。
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是__________________________ ,其中, =
=________ mol·L-1(不能做近似计算,回答准确值,结果不一定要化简)。
(4)丁组实验中,HA和NaOH溶液混合前
________ (填“<”、“>”或“=”)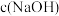 ,b
,b________ (填“<”、“>”或“=”)7。
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲 |  |  | pH=a |
| 乙 |  |  | pH=7 |
| 丙 |  |  | pH=9 |
| 丁 | pH=2 | pH=12 | pH=b |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?
(2)c1
 与NaOH溶液中
与NaOH溶液中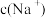 的关系是
的关系是A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
 =
=(4)丁组实验中,HA和NaOH溶液混合前

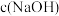 ,b
,b
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】常温下,有下列四种溶液:
①pH=4的NH4Cl溶液;②pH=10的NaOH溶液;③pH=4的盐酸;④pH=4的醋酸溶液。
请回答下列问题:
(1)溶液①和②中由水电离的c(H+)分别为a和b,则a:b=_________________ 。
(2)将②与④等体积混合,所得溶液的pH________________ 填“>”“<”或“=”)7,溶液中离子的物质的量浓度由大到小的顺序是______________ 。
(3)取等体积的③和④两种溶液,分别加水稀释到pH均等于5,所需水的体积分别为V1、V2,则V1____ (填“>”“<”或“=”)V2。
(4)取等体积的③和④两种溶液,加入质量不等的锌粒,反应结束后得到的等量的H2。下列说法正确的是____ 填字母符号)。
A.反应所需时间:③<④B.开始时,反应速率:③>④C.参加反应的锌粒的质量:③=④D.③中锌有剩余E.④中锌有剩余F.④中酸过量
①pH=4的NH4Cl溶液;②pH=10的NaOH溶液;③pH=4的盐酸;④pH=4的醋酸溶液。
请回答下列问题:
(1)溶液①和②中由水电离的c(H+)分别为a和b,则a:b=
(2)将②与④等体积混合,所得溶液的pH
(3)取等体积的③和④两种溶液,分别加水稀释到pH均等于5,所需水的体积分别为V1、V2,则V1
(4)取等体积的③和④两种溶液,加入质量不等的锌粒,反应结束后得到的等量的H2。下列说法正确的是
A.反应所需时间:③<④B.开始时,反应速率:③>④C.参加反应的锌粒的质量:③=④D.③中锌有剩余E.④中锌有剩余F.④中酸过量
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】已知水的电离平衡曲线如图所示,试回答下列问题:

(1)图中五点KW间的关系是__________________ .
(2)若从A点到D点,可采用的措施是________ .
a.升温 b.加入少量的NaOH c.加入少量的NH4Cl
(3)E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________ .
(4)25℃时,体积为Va、pH=a的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液均匀混合后,溶液的pH=7,已知b=2a,Va<Vb , 则a的取值范围为________ .

(1)图中五点KW间的关系是
(2)若从A点到D点,可采用的措施是
a.升温 b.加入少量的NaOH c.加入少量的NH4Cl
(3)E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(4)25℃时,体积为Va、pH=a的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液均匀混合后,溶液的pH=7,已知b=2a,Va<Vb , 则a的取值范围为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】(1)物质的量浓度相同的下列物质的溶液①NH4Cl ②NH4HSO4③CH3COONH4,c(NH4+)由小到大的顺序是_______________ (填序号)。
(2)同浓度的下列溶液:①CH3COONH4②NH4Cl ③Na2CO3④NaHCO3,其中pH由大到小的顺序 是_________________ 。
(3)物质的量浓度相同的 ①盐酸、②硫酸溶液、 ③醋酸(CH3COOH)溶液各100 mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是____________ 。
(4)CH3COONa溶液呈_____ 性(填“酸”、“碱”或“中”),其原因是______ (用离子方程式表示)。
(5)常温时,若10体积pH1=a的盐酸溶液与1体积pH2=b的氢氧化钠溶液混合后溶液呈中性,则混合前该强酸的pH1与强碱的pH2之间应满足的关系是_________________ 。
(2)同浓度的下列溶液:①CH3COONH4②NH4Cl ③Na2CO3④NaHCO3,其中pH由大到小的顺序 是
(3)物质的量浓度相同的 ①盐酸、②硫酸溶液、 ③醋酸(CH3COOH)溶液各100 mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是
(4)CH3COONa溶液呈
(5)常温时,若10体积pH1=a的盐酸溶液与1体积pH2=b的氢氧化钠溶液混合后溶液呈中性,则混合前该强酸的pH1与强碱的pH2之间应满足的关系是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:
请回答下面问题:
(1)上述四种酸中,酸性最弱的是_____________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________________ (填序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________ (选填“酸性”“中性”或“碱性”),理由是__________________ ,溶液中各离子浓度大小的关系是_____________________ 。
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为_____________________________________ 。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应 ≥____________ mol·L-1。
| 酸或碱 | 电离常数(Ka或Kb) | 难(微)溶物 | 溶度积常数(Ksp) |
| CH3COOH | 1.8×10-5 | BaSO4 | 1×10-10 |
| HNO2 | 4.6×10-4 | BaCO3 | 2.6×10-9 |
| HCN | 5×10-10 | CaSO4 | 7×10-5 |
| HClO | 3×10-8 | CaCO3 | 5×10-9 |
| NH3·H2O | 1.8×10-5 |
请回答下面问题:
(1)上述四种酸中,酸性最弱的是
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应 ≥
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】醋酸是一种常见的弱酸,回答下列问题:
(1)下列哪些措施能够使醋酸溶液中 增大___________。
增大___________。
(2)向100mL0.1mol·L-1的醋酸中加入VmL0.1mol·L-1的NaOH溶液完全反应后,溶液呈中性,则V___________ 100mL(填“>”,“<”或“=”)。
(3)在CH3COOH与CH3COONa的混合溶液中,测得某一时刻混合溶液中: =18,则此时溶液的pH=
=18,则此时溶液的pH=___________ 。(已知:CH3COOH的电离常数Ka=1.9×10-5)
(4)常温下,将amol·L-1的醋酸与bmol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=___________ (用含a和b的代数式表示)。
(5)某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室的标准NaOH溶液对其进行滴定实验以测定它的准确浓度,完全反应时所得溶液的pH大约为9。
①该实验应选用___________ 作指示剂。
②为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为cmol/L,三次实验结果记录如下:
从表可以看出,第一次实验中记录消耗NaOH溶液的体积明显少于后两次,其原因可能是___________ 。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积。
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液。
C.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
D.锥形瓶用蒸馏水洗过后未干燥。
E.盛装氢氧化钠溶液的滴定管用蒸馏水洗过,未用氢氧化钠溶液润洗。
③根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):c(CH3COOH)=___________ mol/L。
(1)下列哪些措施能够使醋酸溶液中
 增大___________。
增大___________。| A.升温 | B.通入HCl气体 | C.加入NaHSO4固体 | D.加入NaOH固体 |
(3)在CH3COOH与CH3COONa的混合溶液中,测得某一时刻混合溶液中:
 =18,则此时溶液的pH=
=18,则此时溶液的pH=(4)常温下,将amol·L-1的醋酸与bmol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=
(5)某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室的标准NaOH溶液对其进行滴定实验以测定它的准确浓度,完全反应时所得溶液的pH大约为9。
①该实验应选用
②为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为cmol/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 24.72 | 25.35 | 25.30 |
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积。
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液。
C.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
D.锥形瓶用蒸馏水洗过后未干燥。
E.盛装氢氧化钠溶液的滴定管用蒸馏水洗过,未用氢氧化钠溶液润洗。
③根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):c(CH3COOH)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】25℃时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因_______ (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)_______ 0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)
(3)将混合溶液从25 ℃升温至30 ℃,溶液中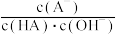 将
将 _______ (填增大或减小)
(4)求出混合液中下列算式的计算结果(填具体数字):c (HA)+c (A-)=_______ mol·L-1;
(5)若向0.1 mol·L-1HA溶液中加入少量水,溶液中 将
将_______ (填增大或减小)
(6)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,将相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列_______ (填序号)
(1)混合溶液的pH=8的原因
(2)混合溶液中由水电离出的c(H+)
(3)将混合溶液从25 ℃升温至30 ℃,溶液中
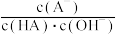 将
将 (4)求出混合液中下列算式的计算结果(填具体数字):c (HA)+c (A-)=
(5)若向0.1 mol·L-1HA溶液中加入少量水,溶液中
 将
将(6)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,将相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】请回答下列问题:
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。则相同条件下破坏1molNO中化学键需要吸收的能量为_______ kJ。
(2)25℃时,pH=5的CH3COOH溶液中,由水电离出的氢离子浓度c(H+)=____ kJ·mol-1;若加入少量NaOH固体,则溶液中
_____ (填“增大”、“减小”或“不变”)。
(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其含碳元素的微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。
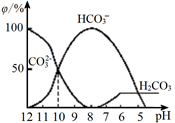
①在同一溶液中,H2CO3、HCO3-、CO32-______ (填“能”或“不能”)大量共存。
②当pH =7时,溶液中含碳元素的微粒主要为________ 。溶液中各种离子的物质的量浓度大小关系为______________ 。
③反应的CO32-+H2O HCO3-+OH-的平衡常数Kh=
HCO3-+OH-的平衡常数Kh=______ 。
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。则相同条件下破坏1molNO中化学键需要吸收的能量为
(2)25℃时,pH=5的CH3COOH溶液中,由水电离出的氢离子浓度c(H+)=

(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其含碳元素的微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。

①在同一溶液中,H2CO3、HCO3-、CO32-
②当pH =7时,溶液中含碳元素的微粒主要为
③反应的CO32-+H2O
 HCO3-+OH-的平衡常数Kh=
HCO3-+OH-的平衡常数Kh=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】电解原理和原电池原理是电化学的两个重要内容.某兴趣小组做如下探究实验:

(1)如图1为某实验小组依据氧化还原反应设计的原电池装置,该反应的离子方程式为__________________ ,反应前两电极质量相等,一段时间后,两电极质量相差15g,导线中通过__ mol电子.
(2)如图1,其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极的电极反应式为___________________________________ ,这是由于NH4Cl溶液显____ 性,用离子方程式表示溶液显此性的原因__________________________________________
(3)如图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成∩型,则乙装置中石墨电极(1)为__ 极,甲装置中铜电极上电极反应式为_____

(4)如图2乙装置中改为加入400mL CuSO4溶液,一段时间后,若电极质量增重1.28g,则此时溶液的pH为__

(1)如图1为某实验小组依据氧化还原反应设计的原电池装置,该反应的离子方程式为
(2)如图1,其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极的电极反应式为
(3)如图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成∩型,则乙装置中石墨电极(1)为

(4)如图2乙装置中改为加入400mL CuSO4溶液,一段时间后,若电极质量增重1.28g,则此时溶液的pH为
您最近一年使用:0次
【推荐1】雌黄 和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。 可转化为治疗白血病的亚砷酸(
可转化为治疗白血病的亚砷酸( )。
)。
(1)向 中滴加
中滴加 溶液反应,溶液中
溶液反应,溶液中 、
、 、
、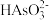 、
、 的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。
的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。

① 溶液呈
溶液呈_______ (填酸性、碱性或中性)。
②25℃时, 的第一电离平衡常数
的第一电离平衡常数 的值为
的值为_______ 。
③人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是_______ 。
④下列说法正确的是_______ (填字母序号)。
a.M点对应的溶液中:
b.N点,
c.在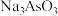 溶液中,
溶液中,
d. 时,溶液中:
时,溶液中:
⑤将 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至12.8时发生反应的离子方程式是
调至12.8时发生反应的离子方程式是__ 。
(2)P和As属于同主族元素,存在亚磷酸( ),常温下,
),常温下,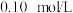 的
的 溶液的
溶液的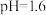 ,亚磷酸与足量的
,亚磷酸与足量的 溶液反应生成
溶液反应生成 。则
。则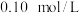 的
的 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是_______ 。
(3)25℃,在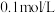 的
的 溶液中,通入
溶液中,通入 气体或加入
气体或加入 固体以调节溶液
固体以调节溶液 ,溶液
,溶液 与c(S2-)关系如图(忽略溶液体积的变化、
与c(S2-)关系如图(忽略溶液体积的变化、 的挥发)。某溶液含
的挥发)。某溶液含 、
、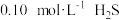 ,当溶液
,当溶液
_______ 时, 开始沉淀[已知
开始沉淀[已知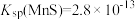 ]。
]。

 和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。 可转化为治疗白血病的亚砷酸(
可转化为治疗白血病的亚砷酸( )。
)。(1)向
 中滴加
中滴加 溶液反应,溶液中
溶液反应,溶液中 、
、 、
、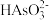 、
、 的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。
的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。
①
 溶液呈
溶液呈②25℃时,
 的第一电离平衡常数
的第一电离平衡常数 的值为
的值为③人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是
④下列说法正确的是
a.M点对应的溶液中:

b.N点,

c.在
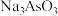 溶液中,
溶液中,
d.
 时,溶液中:
时,溶液中:
⑤将
 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至12.8时发生反应的离子方程式是
调至12.8时发生反应的离子方程式是(2)P和As属于同主族元素,存在亚磷酸(
 ),常温下,
),常温下,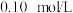 的
的 溶液的
溶液的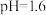 ,亚磷酸与足量的
,亚磷酸与足量的 溶液反应生成
溶液反应生成 。则
。则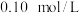 的
的 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(3)25℃,在
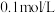 的
的 溶液中,通入
溶液中,通入 气体或加入
气体或加入 固体以调节溶液
固体以调节溶液 ,溶液
,溶液 与c(S2-)关系如图(忽略溶液体积的变化、
与c(S2-)关系如图(忽略溶液体积的变化、 的挥发)。某溶液含
的挥发)。某溶液含 、
、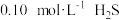 ,当溶液
,当溶液
 开始沉淀[已知
开始沉淀[已知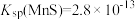 ]。
]。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______ (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) _______ c(CH3COO-)(填“ >”或“=”或“<” )。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________ ,溶液中c(Na+) ___________ c(CH3COO-) (填“ >” 或“=”或“<” )
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈________ .
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】完成下列填空
(1)氯化铝水溶液呈_______ 性,(填“酸”、“中”、“碱”)原因是:_______ (用离子方程式表示)。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______
(2)硫化钠溶于水时发生水解,其水解的离子方程为:_______ ,在配制硫化钠溶液时可以加入少量的_______ 以抑制其水解。
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______ (填“酸性”、“中性”或“碱性”,下同),溶液中c(Na+)_______ c(CH3COO-)(填“>”、“=”或“<”,下同)。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈_______ ,溶液中c(Na+)_______ c(CH3COO-)。
(1)氯化铝水溶液呈
(2)硫化钠溶于水时发生水解,其水解的离子方程为:
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
您最近一年使用:0次



