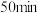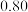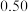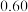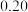催化加氢能生成乙烯和
催化加氢能生成乙烯和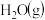 ,按
,按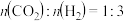 投料,保持压强为
投料,保持压强为 ,反应达到平衡时,四种气体组分的物质的量分数
,反应达到平衡时,四种气体组分的物质的量分数 随温度
随温度 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是
A.表示 变化的曲线是 变化的曲线是 |
B. 催化加氢合成 催化加氢合成 和 和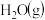 反应的 反应的 大于0 大于0 |
C.当反应达到平衡时,若增大压强,则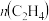 变小 变小 |
D.图中点 对应的平衡常数 对应的平衡常数 为 为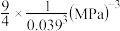 |
更新时间:2021-01-08 13:45:00
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
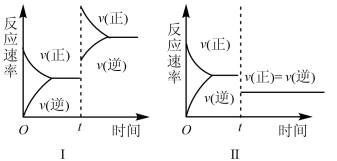
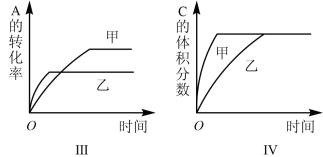
【推荐1】在容积不变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g)+D(s) △H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
3C(g)+D(s) △H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
 3C(g)+D(s) △H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
3C(g)+D(s) △H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是

| A.图I表示增加反应物浓度对该平衡的影响 |
| B.图II表示减小压强对该平衡的影响 |
| C.图III表示温度对该平衡的影响,温度:乙>甲 |
| D.图IV表示催化剂对该平衡的影响,反应速率:甲>乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
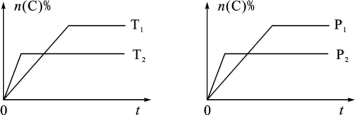
【推荐2】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示变化规律(p表示压强,T表示温度,n表示物质的量):
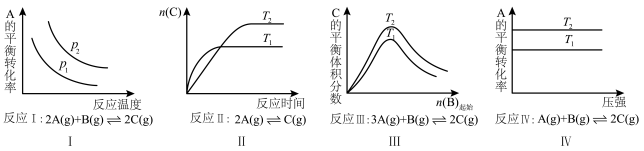
根据以上规律判断,下列结论正确的是( )

根据以上规律判断,下列结论正确的是( )
| A.反应Ⅰ:△H>0,p2>p1 |
| B.反应Ⅲ:△H>0,T2>T1或△H<0,T2<T1 |
| C.反应Ⅱ:△H>0,T1>T2 |
| D.反应Ⅳ:△H<0,T2>T1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,将3mol A和2.5mol B混合,充入2 L密闭容器中,发生反应: 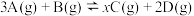 △H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是
△H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是
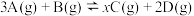 △H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是
△H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是| A.x的值为1 | B.平衡时A的浓度为0.75mol·L-1 |
| C.B的转化率为20% | D.反应速率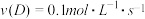 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将一定物质的量的HI(g)置于2L的恒容密闭容器中,只发生反应2HI(g)  H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
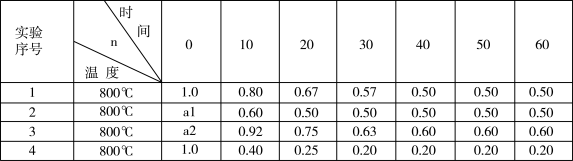
根据表中数据,下列说法正确的是
 H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
根据表中数据,下列说法正确的是
| A.在实验1中,反应在10至20分钟时间内v(HI)=1.3×10-2mol/(L•min) |
| B.在实验2中,第20min时反应恰好达到平衡状态 |
| C.根据实验2和实验3,无法说明浓度越大反应速率越快 |
| D.根据实验2和实验4,无法判断反应△H的正负号 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】可用下面图像表示的是
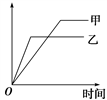

| 反应 | 纵坐标 | 甲 | 乙 | |
| A | SO2与O2在同温、同体积容器中反应 | SO2的转化率 | 2 mol SO2和 1 mol O2 | 2 mol SO2和 2 mol O2 |
| B | 一定质量的氮气和氢气,在同一固定容积的容器中反应 | 氨气的浓度 | 400 ℃ | 500 ℃ |
| C | 2 mol SO2与1 mol O2在同温、体积可变的恒压容器中反应 | SO2的转化率 | 1×106Pa | 1×105Pa |
| D | 体积比为1:3的N2、H2在同温、体积可变的恒压容器中反应 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】利用CH4消除NO2污染,反应原理为CH4(g)+2NO2(g)⇌N2(g)+CO(g)+2H2O(g)。在10L密闭容器中,分别加入0.50molCH4和1.20molNO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是
| 组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.该反应在高温下才能自发进行 |
| B.T2温度下,若容器内的密度不变则该反应处于平衡状态 |
| C.可以利用40min时的数据,计算T2温度下的平衡常数K |
| D.高温下CH4消除NO2速率较快,所以温度越高越有利于消除NO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知某化学反应的平衡常数表达式为K= ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:
下列有关叙述不正确的是
 ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A.该反应的化学方程式是:CO(g)+H2O(g)⇌CO2(g)+H2(g) |
| B.上述反应的正反应是放热反应 |
C.若平衡浓度符合下列关系式: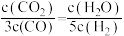 ,则此时的温度是为1000℃ ,则此时的温度是为1000℃ |
| D.在1L的密闭容器中通入CO2和H2各1mol,5min后温度升高到830℃,此时测得CO2为0.4 mol时,则该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某化学反应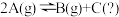 在三种不同条件下进行,
在三种不同条件下进行, 、
、 起始的物质的量为
起始的物质的量为 。反应物
。反应物 的浓度(
的浓度( )随反应时间的变化情况见下表,下列说法不正确的是
)随反应时间的变化情况见下表,下列说法不正确的是
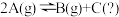 在三种不同条件下进行,
在三种不同条件下进行, 、
、 起始的物质的量为
起始的物质的量为 。反应物
。反应物 的浓度(
的浓度( )随反应时间的变化情况见下表,下列说法不正确的是
)随反应时间的变化情况见下表,下列说法不正确的是| 实验序号 |  |
|
|
|
|
|
|
 |  |
|
|
|
|
|
|
 |  |
|
|
|
|
|
|
 |  |
|
|
|
|
|
|
A.实验1中,前 中A的平均反应速率为 中A的平均反应速率为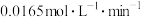 |
| B.实验1、2中,实验2可能使用了催化剂也可能压缩了体积 |
C.该反应的 |
D.实验3中,在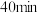 时加入一定量的C物质,平衡可能不移动 时加入一定量的C物质,平衡可能不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应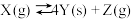 ,其他条件相同,在200℃和a℃时,
,其他条件相同,在200℃和a℃时, 的浓度随时间变化的曲线如图所示,下列有关说法正确的是( )
的浓度随时间变化的曲线如图所示,下列有关说法正确的是( )
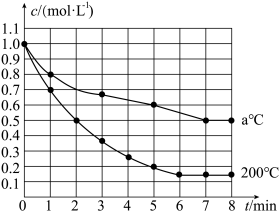
 ,其他条件相同,在200℃和a℃时,
,其他条件相同,在200℃和a℃时, 的浓度随时间变化的曲线如图所示,下列有关说法正确的是( )
的浓度随时间变化的曲线如图所示,下列有关说法正确的是( )
A.其他条件不变,增加压强或 的物质的量时反应速率都增大 的物质的量时反应速率都增大 |
B.a℃、8min时, 的浓度一定为 的浓度一定为 |
| C.由图可知,a大于200 |
D.a℃时,0~1min内 的平均反应速率为 的平均反应速率为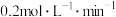 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于可逆反应2AB3(g)⇌A2(g)+3B2(g) ΔH>0,(注:A%、B2%、AB3%分别表示混合气体中的体积分数),下列图象正确的是
A. | B. | C.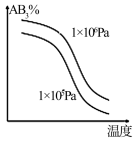 | D.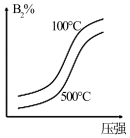 |
您最近一年使用:0次

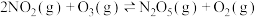 ,若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
,若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是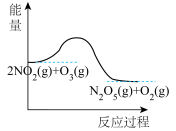

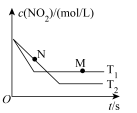

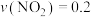 mol·L
mol·L ·s
·s