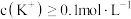常温下,几种弱酸的电离常数的负对数pKa(pKa=-lg Ka)如下:
下列说法错误的是
| 弱酸 | HCN | HNO2 | HClO | HF |
| pKa | 9.31 | 3.37 | 7.52 | 3.43 |
| A.常温下,加水稀释NaClO溶液时水电离的c(H+)·c(OH-)减小 |
| B.常温下,0.1 mol·L-1溶液的pH:NaNO2>NaF>NaClO>NaCN |
C.0.2 mol·L-1 HNO2溶液和0.1 mol·L-1 KOH溶液等体积混合,所得溶液中:c(NO )>c(K+)>c(H+)>c(OH-) )>c(K+)>c(H+)>c(OH-) |
| D.常温下,KCN溶液中KCN的水解常数的负对数pKh=4.69 |
2021高三·全国·专题练习 查看更多[2]
山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期第一次月考化学试题 (已下线)专题11 水溶液中的离子平衡(水的电离、电离常数、水解常数、电离水解判断、KSP)-2021年高考化学必做热点专题
更新时间:2021-02-17 11:20:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.用广泛pH试纸测某盐酸的pH=2.3 |
| B.某醋酸溶液的pH=a,将此溶液稀释100倍后,溶液的pH=b,则a > b-2 |
| C.常温下反应2Na2SO3(s)+O2(g)=2Na2SO4(s)能自发进行,则ΔH>0 |
| D.增大压强(对于气体反应),活化分子百分数增大,故反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,物质的量浓度均为0.1 mol·L-1的下列溶液:①Na2CO3溶液;②NaOH溶液;③NaHSO4溶液;④NH4Cl溶液;⑤NaNO3溶液;已知电离常数K(HSO4-)=1.2×10-2,K2(H2CO3)=5.6×10-11,K(NH3·H2O)=1.8×10-5,pH由小到大的排列顺序是
| A.③<④<⑤<①<② | B.④<③<⑤<①<② |
| C.④<③<①<⑤<② | D.①<④<③<⑤<② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】K、Ka、KW分别表示化学平衡常数、电离平衡常数和水的离子积常数,下列判断正确的是
| A.温度升高,三者都增大 |
| B.化学平衡常数的大小与温度、浓度、催化剂等有关 |
| C.室温下Ka(HCN)<Ka(HF),说明HF的电离度比HCN大 |
D.2SO2(g)+O2(g) 2SO3(g)平衡后,仅增大压强,平衡向右移动,K值不变 2SO3(g)平衡后,仅增大压强,平衡向右移动,K值不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某化学研究性学习小组对电解质溶液作如下归纳总结(均在常温下),正确的是
①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度均降低
②pH=2的盐酸和pH=1的盐酸, 之比为1:10
之比为1:10
③液态HCl、固体NaCl均不导电,所以HCl、NaCl均不是电解质
④已知醋酸电离平衡常数为 ;醋酸根水解常数为
;醋酸根水解常数为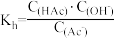 ;水的离子积为
;水的离子积为 ;则三者关系为
;则三者关系为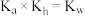
⑤pH值相同的醋酸和盐酸,分别用蒸馏水稀释到原来体积的m倍和n倍,稀释后两溶液的pH值仍相同,则m>n
①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度均降低
②pH=2的盐酸和pH=1的盐酸,
 之比为1:10
之比为1:10③液态HCl、固体NaCl均不导电,所以HCl、NaCl均不是电解质
④已知醋酸电离平衡常数为
 ;醋酸根水解常数为
;醋酸根水解常数为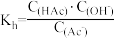 ;水的离子积为
;水的离子积为 ;则三者关系为
;则三者关系为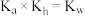
⑤pH值相同的醋酸和盐酸,分别用蒸馏水稀释到原来体积的m倍和n倍,稀释后两溶液的pH值仍相同,则m>n
| A.①②④ | B.③④⑤ | C.①②⑤ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于0.1 mol/L Na2CO3溶液,下列说法正确的是
| A.加入NaOH固体,溶液pH减小 |
| B.升高温度,溶液中c(OH-)增大 |
| C.稀释溶液,溶液中c(H+)减少 |
D.c(Na+)+c(H+) =c( )+c( )+c( )+c(OH-) )+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于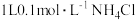 溶液中粒子的浓度关系错误的是( )
溶液中粒子的浓度关系错误的是( )
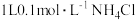 溶液中粒子的浓度关系错误的是( )
溶液中粒子的浓度关系错误的是( )A. | B.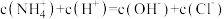 |
C.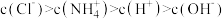 | D.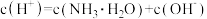 |
您最近一年使用:0次

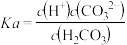
 和
和 );
); 、
、 、
、 、
、 、
、 、
、 。取200mL该溶液,分为等体积的两份,第一份中加入足量的烧碱溶液并加热,产生的气体在标准状况下的体积为224mL。第二份中先加入足量的盐酸,无明显现象,再加入足量的
。取200mL该溶液,分为等体积的两份,第一份中加入足量的烧碱溶液并加热,产生的气体在标准状况下的体积为224mL。第二份中先加入足量的盐酸,无明显现象,再加入足量的 溶液,得到固体2.33g。下列说法不正确的是
溶液,得到固体2.33g。下列说法不正确的是