"绿水青山就是金山银山",在造福人类的同时,保护环境也是化学必不可少的责任。磷酸铁锂电池由橄榄石结构的LiFePO4作为电池的正极,碳(石墨)吸附锂离子组成电池负极(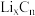 ),电极上附着铝箔、铜箔。如图流程可以回收磷酸铁锂电池电极材料中的石墨并制备相应化工产品。
),电极上附着铝箔、铜箔。如图流程可以回收磷酸铁锂电池电极材料中的石墨并制备相应化工产品。

(1)LiFePO4中Fe的化合价为_______ ,滤渣I的主要成分除LFePO4还有_______ ,滤渣I中加入H2O2的目的是:_______ 。
(2)向滤液Ⅲ中通 H2S的目的是沉铜,当溶液中铜离子浓度为1×10-5mol/L时可认为铜离子沉淀完全,则此时溶液中S2-与Cu2+浓度之比为:_______ (已知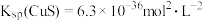 )。
)。
(3)碳酸锂在水中的溶解度随温度升高而减小,则操作X是_______ 。
a.静置、过滤 b.加热后,趁热过滤 c. 蒸发浓缩、冷却结晶 d.蒸发结晶
(4)回收后的Fe2O3可以与KOH和KNO3混合物加热共熔,从而制得净水剂高铁酸钾(K2FeO4)及其副产物KNO2,该反应的化学方程式为:_______ 。
(5)该流程中分离出的Li2CO3可以和NH4H2PO4及(CH3COO)2Fe制备正极材料LiFePO4,已知NH3·H2O的电离常数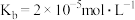 ,H3PO4的各级电离常数为
,H3PO4的各级电离常数为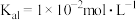 、
、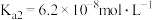 、
、 ,则常温下 NH4H2PO4溶液中
,则常温下 NH4H2PO4溶液中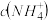
_______ 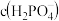 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
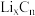 ),电极上附着铝箔、铜箔。如图流程可以回收磷酸铁锂电池电极材料中的石墨并制备相应化工产品。
),电极上附着铝箔、铜箔。如图流程可以回收磷酸铁锂电池电极材料中的石墨并制备相应化工产品。
(1)LiFePO4中Fe的化合价为
(2)向滤液Ⅲ中通 H2S的目的是沉铜,当溶液中铜离子浓度为1×10-5mol/L时可认为铜离子沉淀完全,则此时溶液中S2-与Cu2+浓度之比为:
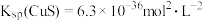 )。
)。(3)碳酸锂在水中的溶解度随温度升高而减小,则操作X是
a.静置、过滤 b.加热后,趁热过滤 c. 蒸发浓缩、冷却结晶 d.蒸发结晶
(4)回收后的Fe2O3可以与KOH和KNO3混合物加热共熔,从而制得净水剂高铁酸钾(K2FeO4)及其副产物KNO2,该反应的化学方程式为:
(5)该流程中分离出的Li2CO3可以和NH4H2PO4及(CH3COO)2Fe制备正极材料LiFePO4,已知NH3·H2O的电离常数
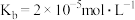 ,H3PO4的各级电离常数为
,H3PO4的各级电离常数为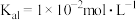 、
、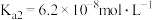 、
、 ,则常温下 NH4H2PO4溶液中
,则常温下 NH4H2PO4溶液中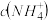
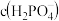 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
2021·山东德州·一模 查看更多[2]
更新时间:2021-03-19 15:15:33
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应原理在科研和生产中有广泛的应用:
(1)利用“化学蒸气转移法”制备 晶体,发生如下反应:
晶体,发生如下反应: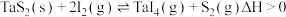 ,若反应(Ⅰ)的平衡常数
,若反应(Ⅰ)的平衡常数 ,向某恒容容器中加入
,向某恒容容器中加入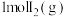 和足量
和足量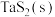 ,
, 的平衡转化率为
的平衡转化率为___________ 。
(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为 的一段放入未提纯的
的一段放入未提纯的 粉末和少量
粉末和少量 ,一段时间后,在温度为
,一段时间后,在温度为 一端得到了纯净
一端得到了纯净 晶体,则温度
晶体,则温度
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。

(3)利用的 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为 ,然后用一定浓度的
,然后用一定浓度的 溶液进行滴定,所用指示剂为
溶液进行滴定,所用指示剂为___________ ,滴定反应的离子方程式为___________ 。
(4) 时,
时, 的电离常数
的电离常数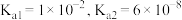 ,则该温度下
,则该温度下 水解反应的平衡常数
水解反应的平衡常数
___________ ,若向 溶液中加入少量
溶液中加入少量 ,则溶液中
,则溶液中 将
将___________ (填“增大”、“减小”或“不变”)。
(1)利用“化学蒸气转移法”制备
 晶体,发生如下反应:
晶体,发生如下反应: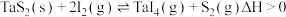 ,若反应(Ⅰ)的平衡常数
,若反应(Ⅰ)的平衡常数 ,向某恒容容器中加入
,向某恒容容器中加入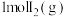 和足量
和足量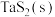 ,
, 的平衡转化率为
的平衡转化率为(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为
 的一段放入未提纯的
的一段放入未提纯的 粉末和少量
粉末和少量 ,一段时间后,在温度为
,一段时间后,在温度为 一端得到了纯净
一端得到了纯净 晶体,则温度
晶体,则温度
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)利用的
 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为
的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为 ,然后用一定浓度的
,然后用一定浓度的 溶液进行滴定,所用指示剂为
溶液进行滴定,所用指示剂为(4)
 时,
时, 的电离常数
的电离常数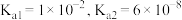 ,则该温度下
,则该温度下 水解反应的平衡常数
水解反应的平衡常数
 溶液中加入少量
溶液中加入少量 ,则溶液中
,则溶液中 将
将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题。
(1)碳酸钠溶液中的电荷守恒式___________ ,物料守恒式___________ ,质子守恒式___________ ,碳酸氢钠溶液的质子守恒式___________ ,物质的量浓度之比为1:1的Na2CO3和NaHCO3混合溶液中的物料守恒式为___________ ,向10ml0.1mol/L的氨水中加入5mL0.1mol/L的盐酸,所得溶液中的质子守恒式为___________ 。
(2)物质的量浓度相同的下列溶液,c( )由大到小的顺序为
)由大到小的顺序为___________ 。
①NH4Cl②NH4HCO3③(NH4)2CO3④(NH4)2SO4⑤NH4HSO4⑥(NH4)2Fe(SO4)2
(3)25℃时,下列有关电解质溶液的说法正确的是___________。
(1)碳酸钠溶液中的电荷守恒式
(2)物质的量浓度相同的下列溶液,c(
 )由大到小的顺序为
)由大到小的顺序为①NH4Cl②NH4HCO3③(NH4)2CO3④(NH4)2SO4⑤NH4HSO4⑥(NH4)2Fe(SO4)2
(3)25℃时,下列有关电解质溶液的说法正确的是___________。
| A.加水稀释0.1mol·L-1氨水,溶液中c(H+)·c(OH-)和c水(H+)·c水(OH-)均保持不变 |
B.向CH3COONa溶液中加入少量CH3COONa,溶液中 的值增大 的值增大 |
C.向CH3COOH溶液中加水稀释,溶液中 的值增大 的值增大 |
D.将浓度为0.1mol·L-1HF溶液加水不断稀释过程中, 增大 增大 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某小组探究FeCl3溶液和NaHSO3溶液的反应
(1)配制溶液
①配制100mL0.10mol•L-1的FeCl3溶液A.配制过程中用到玻璃仪器有烧杯、玻璃棒、量筒、____ 和_______ 。
②配制100mL0.10mol•L-1NaHSO3溶液B,测得溶液B的pH为4.5.分析NaHSO3溶液显酸性的原因,填写如表。
资料:Ka1(H2SO3)=1.4×10-2 Ka2(H2SO3)=6.0×10-8
(2)实验探究
①各取50mLA、B两种溶液在烧杯中混合,观察到无沉淀和气泡产生,所得混合溶液C为红褐色。用激光笔照射,有丁达尔现象。上述现象说明发生了非氧化还原反应,离子方程式为______ (反应1)。
②小组同学认为还有可能发生了氧化还原反应,离子方程式为_______ (反应2)。并设计了以下两种方法证明发生了反应2。
a.取少量溶液C,向其中加入______ ,出现白色沉淀,证明有 。
。
b.取少量溶液C,向其中滴加K3[Fe(CN)6]溶液,出现蓝色沉淀,证明有Fe2+。
分析以上两种方法中a法不科学,理由是_______ 。
将溶液C放置,溶液颜色越来越浅,30分钟后颜色几乎消失。
(3)得出结论:
i.反应1和反应2同时共存,存在竞争。
ii._______ 。
(1)配制溶液
①配制100mL0.10mol•L-1的FeCl3溶液A.配制过程中用到玻璃仪器有烧杯、玻璃棒、量筒、
②配制100mL0.10mol•L-1NaHSO3溶液B,测得溶液B的pH为4.5.分析NaHSO3溶液显酸性的原因,填写如表。
资料:Ka1(H2SO3)=1.4×10-2 Ka2(H2SO3)=6.0×10-8
| 离子方程式 | 平衡常数值 | |
 电离平衡 电离平衡 |  ⇌H++ ⇌H++ | |
 水解平衡 水解平衡 | ||
| 结论 | 电离程度>水解程度,所以NaHSO3溶液显酸性 | |
①各取50mLA、B两种溶液在烧杯中混合,观察到无沉淀和气泡产生,所得混合溶液C为红褐色。用激光笔照射,有丁达尔现象。上述现象说明发生了非氧化还原反应,离子方程式为
②小组同学认为还有可能发生了氧化还原反应,离子方程式为
a.取少量溶液C,向其中加入
 。
。b.取少量溶液C,向其中滴加K3[Fe(CN)6]溶液,出现蓝色沉淀,证明有Fe2+。
分析以上两种方法中a法不科学,理由是
将溶液C放置,溶液颜色越来越浅,30分钟后颜色几乎消失。
(3)得出结论:
i.反应1和反应2同时共存,存在竞争。
ii.
您最近一年使用:0次
【推荐1】“NaH2PO2还原法”制备高纯度氢碘酸和亚磷酸钠(Na2HPO3)的工业流程如图。
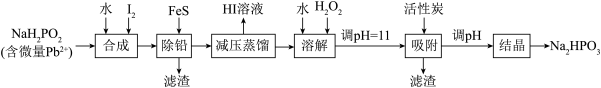
已知:25℃时,H3PO3的pKa1=1.3,pKa2=6.6。
(1)“合成”过程,主要氧化产物为H3PO3,相应的化学方程式为___________ 。
(2)“除铅”过程,FeS除去微量Pb2+的离子方程式为___________ 。
(3)“减压蒸馏”过程,I-回收率为95%,则剩余固体的主要成分为___________ (填化学式)。
(4)“调pH=11”的作用是___________ 。
(5)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;A、B为离子交换膜。
①B膜最佳应选择___________
②阳极的电极反应式是___________ 。
③少量的I-因为浓度差通过BPM膜,若撤去A膜,其缺点是:___________
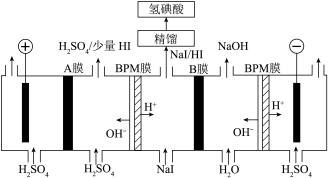

已知:25℃时,H3PO3的pKa1=1.3,pKa2=6.6。
(1)“合成”过程,主要氧化产物为H3PO3,相应的化学方程式为
(2)“除铅”过程,FeS除去微量Pb2+的离子方程式为
(3)“减压蒸馏”过程,I-回收率为95%,则剩余固体的主要成分为
(4)“调pH=11”的作用是
(5)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;A、B为离子交换膜。
①B膜最佳应选择
②阳极的电极反应式是
③少量的I-因为浓度差通过BPM膜,若撤去A膜,其缺点是:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为了测定Na2CS3溶液的浓度,按图装置进行实验,将35.0mLNa2CS3溶液置于装置A的三颈瓶中,打开仪器d的活塞,滴入足量2.0 mol·L-1H2SO4,关闭活塞。

已知:CS +2H+=CS2+H2S↑,CS2和H2S均有毒,CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O
+2H+=CS2+H2S↑,CS2和H2S均有毒,CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O
(1)反应开始时需要先通入一段时间N2,其作用为_______
(2)B中发生反应的离子方程式是_______
(3)反应结束后打开止水夹K,再缓慢通入热N2一段时间,其目的是_______

已知:CS
 +2H+=CS2+H2S↑,CS2和H2S均有毒,CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O
+2H+=CS2+H2S↑,CS2和H2S均有毒,CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O(1)反应开始时需要先通入一段时间N2,其作用为
(2)B中发生反应的离子方程式是
(3)反应结束后打开止水夹K,再缓慢通入热N2一段时间,其目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】镁在工业、医疗等领域均有重要用途。某小组利用工厂废弃物(主要含MgCO3、MgSiO3、Al2O3和Fe2O3等)设计回收镁的工艺流程如图:
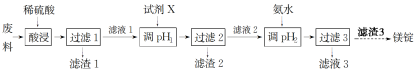
各种阳离子开始沉淀(浓度均为0.1 mol·L-1)和结束沉淀时的pH:
(1)酸浸前将“废料”粉碎,酸浸过程中采用“加热、适当提高稀硫酸的浓度等”措施的目的是___ ,为达到此目的,还可以采取的措施是___ (任写一条)。
(2)滤渣1的名称是___ 。
(3)第一次调节pH的目的是___ 。为了提高产品的纯度,试剂X不可能是___ (填字母)。
A.氨水 B.MgO C.MgCO3 D.CuO
设计简单方案分离滤渣2中的成分,简述实验过程:___ 。
(4)生成滤渣3的离子方程式为___ 。工业上由滤渣3得到镁锭发生的最后一步化学方程式为___ 。

各种阳离子开始沉淀(浓度均为0.1 mol·L-1)和结束沉淀时的pH:
| 金属阳离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀pH | 1.1 | 3.0 | 8.4 |
| 完全沉淀pH | 3.0 | 4.7 | 10.8 |
(1)酸浸前将“废料”粉碎,酸浸过程中采用“加热、适当提高稀硫酸的浓度等”措施的目的是
(2)滤渣1的名称是
(3)第一次调节pH的目的是
A.氨水 B.MgO C.MgCO3 D.CuO
设计简单方案分离滤渣2中的成分,简述实验过程:
(4)生成滤渣3的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】25℃时,部分物质的电离平衡常数如表所示
请回答下列问题:
(1)同浓度的CH3COO-、 、
、 、ClO- 结合H+的能力由强到弱的顺序为
、ClO- 结合H+的能力由强到弱的顺序为___________ 。
(2)常温下,0.1mol•L-1 的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是___________(填序号)。
(3)在一定温度下,冰醋酸加水稀释过程如下图所示,a、b、c三点处,电离程度最大的是___________ 。

(4)25℃时,pH=4的盐酸中水的电离程度___________ pH=10的Ba(OH)2溶液中水的电离程度(填“<”“>”或“=”)。
(5)某温度下,测得0.1 mol/L NaOH溶液pH为11,则该温度下水的离子积常数Kw=___________ 。
(6)浓度相等的盐酸和醋酸各100mL,分别与过量的Zn反应,相同条件下生成H2的体积分别为V1和V2,则V1___________ V2 (填“>”、“<”或“=”)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)同浓度的CH3COO-、
 、
、 、ClO- 结合H+的能力由强到弱的顺序为
、ClO- 结合H+的能力由强到弱的顺序为(2)常温下,0.1mol•L-1 的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是___________(填序号)。
| A.c(H+) | B. | C.c(H+)•c(OH-) | D. |
(3)在一定温度下,冰醋酸加水稀释过程如下图所示,a、b、c三点处,电离程度最大的是

(4)25℃时,pH=4的盐酸中水的电离程度
(5)某温度下,测得0.1 mol/L NaOH溶液pH为11,则该温度下水的离子积常数Kw=
(6)浓度相等的盐酸和醋酸各100mL,分别与过量的Zn反应,相同条件下生成H2的体积分别为V1和V2,则V1
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】我国化学家侯德榜发明了“联合制碱法”,将制碱技术发展到一个新水平,赢得了国际化工界的高度评价。回答下列问题:
(1)“联合制碱法”的主要原料为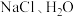 、
、___________ (填化学式)。
(2)某学科组探究 溶液与盐酸的反应。常温下,向
溶液与盐酸的反应。常温下,向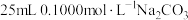 溶液中缓慢滴加
溶液中缓慢滴加 盐酸,利用数字传感技术绘制的滴定曲线如图所示。
盐酸,利用数字传感技术绘制的滴定曲线如图所示。

①由图可知, 水溶液显
水溶液显___________ (填“酸”“碱”或“中”)性。
②由图可知,常温下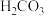 的二级电离常数
的二级电离常数 约为
约为___________ 。
(3)某学科组采用双指示剂的滴定法测定利用“联合制碱法”制得的纯碱(含少量 杂质)的纯度,步骤如下:
杂质)的纯度,步骤如下:
(i)准确称取纯碱样品wg放入锥形瓶中,加蒸馏水溶解,加入1~2滴指示剂Ⅰ;
(ⅱ)用0.1000mol/L盐酸滴定该溶液至恰好出现现象Ⅰ,消耗盐酸的体积为 ;
;
(ⅲ)再在步骤(ⅱ)的溶液中加入1-2滴甲基橙指示剂,继续用0.1000mol/L盐酸滴定至恰好出现现象Ⅱ,消耗盐酸的体积为 。
。
①指示剂Ⅰ为___________ ,现象Ⅰ是___________ ;现象Ⅱ是___________ 。
②滴定过程中酸式滴定管的三次读数位置如图所示:

其中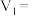
___________ ,
___________ ;该样品中纯碱的纯度是___________ %(结果保留三位有效数字)。
(1)“联合制碱法”的主要原料为
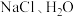 、
、(2)某学科组探究
 溶液与盐酸的反应。常温下,向
溶液与盐酸的反应。常温下,向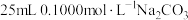 溶液中缓慢滴加
溶液中缓慢滴加 盐酸,利用数字传感技术绘制的滴定曲线如图所示。
盐酸,利用数字传感技术绘制的滴定曲线如图所示。
①由图可知,
 水溶液显
水溶液显②由图可知,常温下
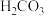 的二级电离常数
的二级电离常数 约为
约为(3)某学科组采用双指示剂的滴定法测定利用“联合制碱法”制得的纯碱(含少量
 杂质)的纯度,步骤如下:
杂质)的纯度,步骤如下:(i)准确称取纯碱样品wg放入锥形瓶中,加蒸馏水溶解,加入1~2滴指示剂Ⅰ;
(ⅱ)用0.1000mol/L盐酸滴定该溶液至恰好出现现象Ⅰ,消耗盐酸的体积为
 ;
;(ⅲ)再在步骤(ⅱ)的溶液中加入1-2滴甲基橙指示剂,继续用0.1000mol/L盐酸滴定至恰好出现现象Ⅱ,消耗盐酸的体积为
 。
。①指示剂Ⅰ为
②滴定过程中酸式滴定管的三次读数位置如图所示:

其中
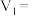

您最近一年使用:0次
【推荐3】直接排放含SO2的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
(1)如图所示:1molCH4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化。
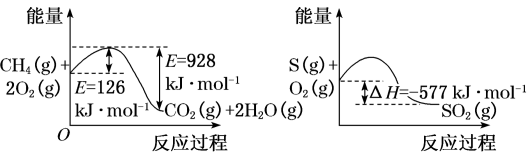
在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式___ 。
(2)焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g) S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:

①A、B、C、D四点对应的状态中,达到平衡状态的有___ (填字母)。
②该反应的ΔH___ 0(填“>”“<”或“=”)
③下列措施能够增大SO2平衡转化率的是___ 。
A.降低温度 B.增加C的量 C.减小容器体积 D.添加高效催化剂
(3)用氨水吸收SO2。25℃时2.0mol·L-1的氨水中,NH3·H2O的电离度α=___ (α= ×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的
×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的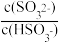 =
=___ 。(已知25℃,Kb(NH3·H2O)=1.8×10-5;Ka1(H2SO3)=1.3×10-2,Ka2(H2SO3)=6.2×10-8)
(4)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8。

写出电解NH4HSO4溶液的化学方程式___ 。
(1)如图所示:1molCH4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化。

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式
(2)焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g)
 S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率和S2(g)的生成速率随温度变化的关系如图所示:
①A、B、C、D四点对应的状态中,达到平衡状态的有
②该反应的ΔH
③下列措施能够增大SO2平衡转化率的是
A.降低温度 B.增加C的量 C.减小容器体积 D.添加高效催化剂
(3)用氨水吸收SO2。25℃时2.0mol·L-1的氨水中,NH3·H2O的电离度α=
 ×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的
×100%)。。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的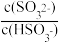 =
=(4)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8。

写出电解NH4HSO4溶液的化学方程式
您最近一年使用:0次



