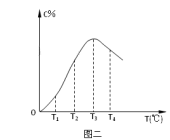
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二。下列分析不正确的是
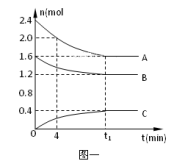


A.0~4 时,A的平均反应速率为0.01mol/(L·min) 时,A的平均反应速率为0.01mol/(L·min) |
B.该反应的平衡常数表达式为: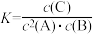 |
| C.由T1向T2变化时,v正>v逆 |
| D.此反应的正反应为吸热反应 |
更新时间:2021-04-10 15:23:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应:3A(g)+B(g)=2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,分别为
①v(A)=0.6mol·L-1·min-1
②v(B)=0.45mol·L-1·min-1
③v(C)=0.15mol·L-1·min-1
④v(D)=0.45mol·L-1·min-1
则此反应在不同条件下进行快慢顺序正确的是
①v(A)=0.6mol·L-1·min-1
②v(B)=0.45mol·L-1·min-1
③v(C)=0.15mol·L-1·min-1
④v(D)=0.45mol·L-1·min-1
则此反应在不同条件下进行快慢顺序正确的是
| A.①>②>③>④ | B.①>②=④>③ | C.②>④>③>① | D.②>④>①>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】T°C时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
 PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A.反应在前50s内的平均速率为v(PCl3)=0.0032mol·L-1·s-1 |
| B.反应350s时,反应放出的Cl2的体积为4.48L |
| C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2达到平衡前v正<v逆 |
| D.平衡时,再充入1.0molPCl5(g),达到新平衡时PCl5的体积分数大于原平衡PCl5的体积分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害。一定温度下,在容积不变的密闭容器中,充入一定量的CO与H2S使之发生下列反应并达到平衡:CO(g)+ H2S(g) COS(g)+ H2(g)。若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1.下列说法正确的是
COS(g)+ H2(g)。若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1.下列说法正确的是
 COS(g)+ H2(g)。若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1.下列说法正确的是
COS(g)+ H2(g)。若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1.下列说法正确的是| A.若升高温度,H2S的浓度增大,则表明该反应是吸热反应 |
| B.通入CO后,正反应速率逐渐增大 |
| C.反应前H2S的物质的量为7 mol |
| D.向平衡体系中再加入所有反应物和生成物各4 mol,则反应向右进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在恒容密闭容器中按物质的量之比 充入
充入 和
和 ,发生反应:
,发生反应: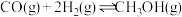 ,测得平衡混合物中
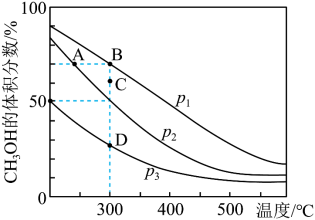
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
 充入
充入 和
和 ,发生反应:
,发生反应: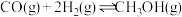 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
A.该反应的 | B.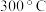 时,该反应的平衡常数 时,该反应的平衡常数 |
C.压强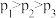 | D.压强为 、温度为 、温度为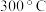 的条件下,C点 的条件下,C点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知:CO2(g) + 3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
CH3OH(g)+H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是

 CH3OH(g)+H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
CH3OH(g)+H2O(g) ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
A.10min后,升高温度能使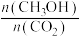 增大 增大 |
| B.反应达到平衡状态时,CO2的平衡转化率为75% |
| C.3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 |
| D.从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 mol·L-1•min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】治理汽车尾气中NO和CO污染的一种方法的反应原理为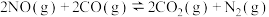 ,某一温度下,其化学平衡常数
,某一温度下,其化学平衡常数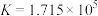 。下列说法正确的是
。下列说法正确的是
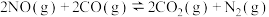 ,某一温度下,其化学平衡常数
,某一温度下,其化学平衡常数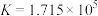 。下列说法正确的是
。下列说法正确的是| A.反应达到平衡时,CO、NO的转化率相等 |
B.化学平衡常数的表达式为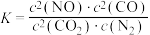 |
| C.此温度下,因K值较大,故化学反应速率较快 |
| D.加入催化剂,反应物的活化分子百分数增大,有效碰撞次数增多,反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时两个恒容密闭容器中仅发生反应
 。实验测得:
。实验测得: ,
,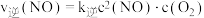 ,
, 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。
下列说法不正确 的是

 。实验测得:
。实验测得: ,
,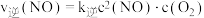 ,
, 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。| 容器编号 | 起始浓度 (mol/L) | 平衡浓度(mol/L) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.6 | 0.1 | 0 | |
| A.升高温度,该反应的化学平衡常数增大 |
B.Ⅰ中 的平衡转化率约为66.7% 的平衡转化率约为66.7% |
C.Ⅱ中达到平衡状态时, |
D.该反应的化学平衡常数可表示为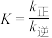 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对于二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是
 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是| A.该反应的ΔS>0 |
B.该反应平衡常数的表达式为K=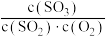 |
| C.反应中每消耗22.4LO2(标准状况),转移电子数约为2×6.02×1023 |
| D.温度不变,提高O2的起始浓度或增大反应压强,均能提高反应速率和SO2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
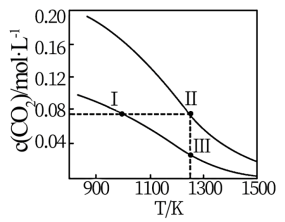
【推荐1】在体积均为1.0L的两个恒容密闭容器中加入足量的相同质量的固体B,再分别加入0.1mol A和0.2molA,在不同温度下反应A(g) +B(s) 2C(g)达到平衡,平衡时A的物质的量浓度c( A)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2C(g)达到平衡,平衡时A的物质的量浓度c( A)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
 2C(g)达到平衡,平衡时A的物质的量浓度c( A)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2C(g)达到平衡,平衡时A的物质的量浓度c( A)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
A.反应 A(g)+ B(s) 2C(g) △S>0、△H<0 2C(g) △S>0、△H<0 |
| B.A的转化率:a(状态Ⅱ)>a(状态Ⅲ) |
| C.体系中c(C)∶c(C,状态Ⅱ)>(C,状态Ⅲ) |
| D.化学平衡常数:K (状态Ⅰ) =K (状态Ⅲ)>K(状态Ⅱ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应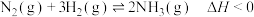 ,平衡时
,平衡时 的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是

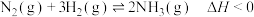 ,平衡时
,平衡时 的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
A.平衡常数值: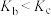 |
B. 温度下,若由a点达到 温度下,若由a点达到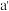 ,可以采取减小压强的方法 ,可以采取减小压强的方法 |
C.d点: |
D.从b点变为 点,增加 点,增加 的物质的量 的物质的量 |
您最近一年使用:0次

 与
与 反应制取
反应制取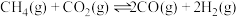 ,在
,在 恒容密闭容器中加入起始浓度均为
恒容密闭容器中加入起始浓度均为 的
的
 的体积分数
的体积分数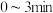 内用
内用 表示的反应速率为
表示的反应速率为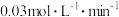
 时压缩容器的体积,正反应速率增大,逆反应速率减小
时压缩容器的体积,正反应速率增大,逆反应速率减小



