在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)
(1)保持容器容积不变,向其中充入1 mol H2,反应速率_________ 。
(2)升高温度,反应速率________ 。
(3)扩大容器体积,反应速率______ 。
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率________ 。
(5)保持容器体积不变,向其中充入1 mol N2,反应速率________ 。
(6)保持容器内气体压强不变,向其中充入1 mol N2,反应速率________ 。
(1)保持容器容积不变,向其中充入1 mol H2,反应速率
(2)升高温度,反应速率
(3)扩大容器体积,反应速率
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率
(5)保持容器体积不变,向其中充入1 mol N2,反应速率
(6)保持容器内气体压强不变,向其中充入1 mol N2,反应速率
20-21高二下·青海海东·阶段练习 查看更多[9]
湖南省长长沙市德成学校2023-2024学年高二上学期11月期中考试化学试题(已下线)第二章 化学反应速率与化学平衡(A卷·知识通关练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)第06讲 影响化学反应速率的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.1.2 影响化学反应速率的因素(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第2章 化学反应速率与化学平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第二章 第二节 影响化学反应速率的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)青海省海东市第二中学2020-2021学年高二4月月考化学试题
更新时间:2021-05-25 16:02:24
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入足量 的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
①哪一段时间内反应速率最大:____ min(填“0~1”或“1~2”或“2~3”或“3~4” 或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是____ (填字母序号)。
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:
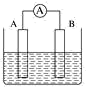
①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是_______ (填“铝片”或“镁片”)。
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:____ ;若该电池反应消耗了 0.1mol FeCl3, 则转移电子的数目为 _____ 。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:

①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下列说法中正确的是_______
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞可能发生化学反应
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④加入反应物,活化分子百分数不变,化学反应速率可能不变
⑤催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率
⑥有气体参加的化学反应,若增大压强(缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞可能发生化学反应
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④加入反应物,活化分子百分数不变,化学反应速率可能不变
⑤催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率
⑥有气体参加的化学反应,若增大压强(缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
①哪一段时间内反应速率最大:___________ min。(填“0~ 1” “1~2”“2~3”“3~4”或“4~ 5”)
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是___________ 。(填字母序号)
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是___________ 反应 (填“放热”或“吸热”)
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称___________ , B 电极反应式:___________ ,该电池在工作时,溶液中Fe3+向___________ (填“A”、“B” )移动,A电极的质量将___________ 。 (填“增加”、“减小”或“不变”)
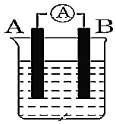
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一、某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值) :
| 时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL (标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A. KCl溶液 B.浓盐酸 C.蒸馏水 D. CuSO4溶液
③该反应还伴随着化学能与热能的转化,是
(2)如图为原电池装置示意图。A为Cu, B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2.写出A的电极名称

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】反应H2(g)+I2(g)⇌2HI(g),在一容积可变的密闭容器中进行,试回答:
(1)将容器的体积缩小一半,其正反应速率_______ (填“增大”、“不变”或“减小”,下同),平衡_______ 移动(填“不”、“向正反应方向”或“向逆反应方向”,下同)。
(2)保持体积不变,充入氩气使体系压强增大,其正反应速率_______ ,平衡_______ 移动。
(3)保持体积不变,充入氢气,其正反应速率_______ ,平衡_______ 移动。
(1)将容器的体积缩小一半,其正反应速率
(2)保持体积不变,充入氩气使体系压强增大,其正反应速率
(3)保持体积不变,充入氢气,其正反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
(1)增加Fe的物质的量,其正反应速率__________ ,逆反应速率__________ 。
(2)将容器的体积缩小一半,其正反应速率________ ,逆反应速率_________ 。
(3)若保持体积不变,充入Ar,其逆反应速率________ ,逆反应速率_________ 。
(4)保持压强不变,充入Ar,其正反应速率__________ ,逆反应速率_________ 。
(5)使用催化剂,其正反应速率__________ ,逆反应速率_________ 。
 Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。(1)增加Fe的物质的量,其正反应速率
(2)将容器的体积缩小一半,其正反应速率
(3)若保持体积不变,充入Ar,其逆反应速率
(4)保持压强不变,充入Ar,其正反应速率
(5)使用催化剂,其正反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】影响化学反应速率的其他因素
(1)浓度:底物浓度越大,化学反应速率___________ 。
(2)温度:当其他条件相同时,___________ 反应速率增大,___________ 反应速率减小。
(3)催化剂:同一反应,用不同催化剂,反应速率不相同。
(4)压强:对有气体参加的反应,压强对化学反应速率的影响可简化理解如下
①对于气体来说,在一定温度下,一定质量的气体所占的体积与压强成___________ ,其他条件不变时,增大压强,气体体积___________ ,浓度___________ 。
②对于有气体参加的化学反应,在相同温度下,增大压强,反应速率___________ ;减小压强,反应速率___________ 。
(1)浓度:底物浓度越大,化学反应速率
(2)温度:当其他条件相同时,
(3)催化剂:同一反应,用不同催化剂,反应速率不相同。
(4)压强:对有气体参加的反应,压强对化学反应速率的影响可简化理解如下
①对于气体来说,在一定温度下,一定质量的气体所占的体积与压强成
②对于有气体参加的化学反应,在相同温度下,增大压强,反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
(1)实验4和5表明_______ 对反应速率有影响,_______ 反应速率越快,能表明同一规律的实验还有_______ (填实验序号);
(2)实验2和5表明_______ 对反应速率有影响;
(3)本实验中影响反应速率的其他因素还有_______ ,其实验序号是_______ 。
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:_______ 。
| 实验序号 | 金属质量/g | 金属状态 | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
(1)实验4和5表明
(2)实验2和5表明
(3)本实验中影响反应速率的其他因素还有
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①写出H2O2在二氧化锰作用下发生反应的化学方程式___________ 。
②实验时放出气体的总体积是________ mL。
③放出1/3气体所需时间为________ min。
④反应放出3/4气体所需时间约为_______ min。
⑤A、B、C、D各点反应速率由快到慢的顺序为_________ 。
⑥解释反应速率变化的原因____________ 。
⑦计算H2O2的初始物质的量浓度___________ 。(请保留两位有效数字)

①写出H2O2在二氧化锰作用下发生反应的化学方程式
②实验时放出气体的总体积是
③放出1/3气体所需时间为
④反应放出3/4气体所需时间约为
⑤A、B、C、D各点反应速率由快到慢的顺序为
⑥解释反应速率变化的原因
⑦计算H2O2的初始物质的量浓度
您最近一年使用:0次



