用还原法处理 是环境科学研究的热点课题。
是环境科学研究的热点课题。
(1)用 还原法处理氮的氧化物,有关反应如下:
还原法处理氮的氧化物,有关反应如下:
①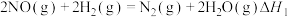
②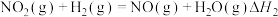
③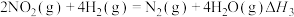
上述反应中, 、
、 、
、 之间的关系式为
之间的关系式为___________ 。
(2)氨还原法处理 的原理为:
的原理为: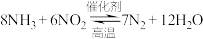 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入 和
和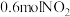 ,在一定条件下进行反应,达到平衡时氧化产物比还原产物多
,在一定条件下进行反应,达到平衡时氧化产物比还原产物多
①下列能说明上述反应达到平衡状态的是____________ (填代号)
A.混合气体的密度保持不变 B. 、
、 的浓度之比为
的浓度之比为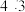
C.混合气体的平均相对分子质量保持不变 D.断裂 键速率等于断裂
键速率等于断裂 键速率
键速率
②上述反应达到平衡时转移___________ mol电子。
(3) 还原法处理NO的原理为
还原法处理NO的原理为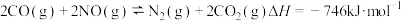 。在某密闭容器中充入
。在某密闭容器中充入 和
和 ,发生该反应。平衡体系中NO的体积分数与温度、压强的关系如图所示。
,发生该反应。平衡体系中NO的体积分数与温度、压强的关系如图所示。
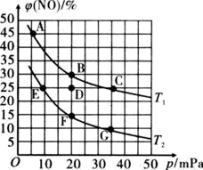
①下列有关说法正确的是___________ (填代号)
a.温度: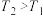
b.NO的平衡转化率: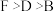
c.反应速率: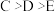
②某温度下,上述反应进行5min时放出的热量为373kJ,则 的平均反应速率v(N2)=
的平均反应速率v(N2)=_______________ mol/min
③用气体分压代替浓度计算的平衡常数叫压强平衡常数 ,已知某气体分压
,已知某气体分压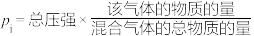 。某温度下,上述反应达到平衡D点时,压强平衡常数
。某温度下,上述反应达到平衡D点时,压强平衡常数 为
为___________  (结果保留2位有效数字)
(结果保留2位有效数字)
 是环境科学研究的热点课题。
是环境科学研究的热点课题。(1)用
 还原法处理氮的氧化物,有关反应如下:
还原法处理氮的氧化物,有关反应如下:①
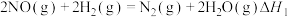
②
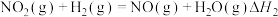
③
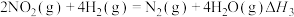
上述反应中,
 、
、 、
、 之间的关系式为
之间的关系式为(2)氨还原法处理
 的原理为:
的原理为: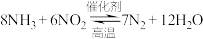 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入 和
和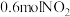 ,在一定条件下进行反应,达到平衡时氧化产物比还原产物多
,在一定条件下进行反应,达到平衡时氧化产物比还原产物多
①下列能说明上述反应达到平衡状态的是
A.混合气体的密度保持不变 B.
 、
、 的浓度之比为
的浓度之比为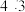
C.混合气体的平均相对分子质量保持不变 D.断裂
 键速率等于断裂
键速率等于断裂 键速率
键速率②上述反应达到平衡时转移
(3)
 还原法处理NO的原理为
还原法处理NO的原理为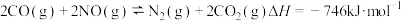 。在某密闭容器中充入
。在某密闭容器中充入 和
和 ,发生该反应。平衡体系中NO的体积分数与温度、压强的关系如图所示。
,发生该反应。平衡体系中NO的体积分数与温度、压强的关系如图所示。
①下列有关说法正确的是
a.温度:
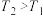
b.NO的平衡转化率:
c.反应速率:
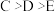
②某温度下,上述反应进行5min时放出的热量为373kJ,则
 的平均反应速率v(N2)=
的平均反应速率v(N2)=③用气体分压代替浓度计算的平衡常数叫压强平衡常数
 ,已知某气体分压
,已知某气体分压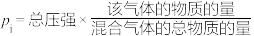 。某温度下,上述反应达到平衡D点时,压强平衡常数
。某温度下,上述反应达到平衡D点时,压强平衡常数 为
为 (结果保留2位有效数字)
(结果保留2位有效数字)
更新时间:2021-08-26 07:18:32
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业上常以水煤气(CO和H2)为原料合成甲醇。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
则C(s)与H2O(g)制备水煤气的热化学方程式为_______ 。
(2)工业上通常用水煤气在恒容、催化剂和加热条件下生产甲醇,其热化学方程式为:CO(g)+2H2(g)⇌CH3OH(g) ΔH=-90.8kJ·mol-1。以下各项能说明该反应达到平衡状态的是_______。
(3)在2L恒容容器中,分别在T1、T2两种温度下模拟工业合成甲醇。两种温度下不同H2和CO起始组成比[n(H2)/n(CO)]与CO平衡转化率的关系如图所示:
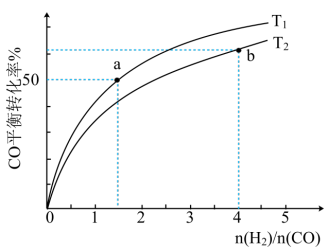
①温度T1_______ T2(填“>”、“<”或“=”)。
②T1时,往恒容容器中充入1molCO、1.5molH2,经过5min达到平衡,则5min内用H2表示的反应速率为v(H2)=_______ ,反应平衡常数K=_______ 。平衡后向容器中再通入0.4molCO、0.7molH2和0.4molCH3OH,此时v正_______ v逆(填“>”、“<”或“=”)。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
则C(s)与H2O(g)制备水煤气的热化学方程式为
(2)工业上通常用水煤气在恒容、催化剂和加热条件下生产甲醇,其热化学方程式为:CO(g)+2H2(g)⇌CH3OH(g) ΔH=-90.8kJ·mol-1。以下各项能说明该反应达到平衡状态的是_______。
| A.混合气体的密度保持不变 | B.容器内总压强保持不变 |
| C.CO的体积分数保持不变 | D.2v逆(H2)=v正(CH3OH) |

①温度T1
②T1时,往恒容容器中充入1molCO、1.5molH2,经过5min达到平衡,则5min内用H2表示的反应速率为v(H2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氨是重要的基础化工原料,可以制备亚硝酸(HNO2)、连二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多种含氮的化工产品。
(1)已知:①4NH3(g)+3O2(g) 2N2(g)+6H2O(g)△H=-1266.2k/mol,②2H2(g)+O2(g)
2N2(g)+6H2O(g)△H=-1266.2k/mol,②2H2(g)+O2(g) 2H2O(g) △H=-483.6kJ/mol则合成氨反应的热化学反应方程式为
2H2O(g) △H=-483.6kJ/mol则合成氨反应的热化学反应方程式为______________ 。
(2)已知:25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaNO2)_________ pH(NaHN2O2)(填“>”“<”或“=”)。
②25℃时,NaHN2O2溶液中存在水解平衡,其水解常数Kh=_______________ 。
③0.1mol/L Na2N2O2溶液中离子浓度由大到小的顺序为_______________________________ 。
(3)400℃时在甲、乙、丙三个容积均为2L的密闭容器中,以不同的投料比投入N2、H2共4mol,测得N2的体积分数如图所示。
①乙容器中N2、H2的投料比为___________ 。
②反应达到平衡后,测得乙容器中H2的体积分数为25%,则400℃时,合成氨反应的平衡常数为______ L2/mol2。
(4)在M、N两个相同的容器中分别充入相同投料比的N2、H2,进行合成氨反应,各反应1小时,测定不同温度下N2的转化率如图所示。
①N2、H2在M、N两容器中反应时,不同的反应条件可能是______________________ 。
②在300℃时,a、b两点转化率不同的原因是______________________ 。
(1)已知:①4NH3(g)+3O2(g)
 2N2(g)+6H2O(g)△H=-1266.2k/mol,②2H2(g)+O2(g)
2N2(g)+6H2O(g)△H=-1266.2k/mol,②2H2(g)+O2(g) 2H2O(g) △H=-483.6kJ/mol则合成氨反应的热化学反应方程式为
2H2O(g) △H=-483.6kJ/mol则合成氨反应的热化学反应方程式为(2)已知:25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
| 化学式 | HNO2 | H2N2O2 |
| 电离常数 | Ka=5.1×10−4 | Ka1=6.0×10−8 、Ka2=2.9×10−12 |
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaNO2)
②25℃时,NaHN2O2溶液中存在水解平衡,其水解常数Kh=
③0.1mol/L Na2N2O2溶液中离子浓度由大到小的顺序为
(3)400℃时在甲、乙、丙三个容积均为2L的密闭容器中,以不同的投料比投入N2、H2共4mol,测得N2的体积分数如图所示。

①乙容器中N2、H2的投料比为
②反应达到平衡后,测得乙容器中H2的体积分数为25%,则400℃时,合成氨反应的平衡常数为
(4)在M、N两个相同的容器中分别充入相同投料比的N2、H2,进行合成氨反应,各反应1小时,测定不同温度下N2的转化率如图所示。

①N2、H2在M、N两容器中反应时,不同的反应条件可能是
②在300℃时,a、b两点转化率不同的原因是
您最近一年使用:0次
【推荐3】丙烯(C3H6)是仅次于乙烯(C2H4)的重要基本有机原料,工业上常利用丙烷(C3H8)催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
①C3H8→C3H6+H2 ②2 C3H6+9O2→6CO2+9H2O ③C3H8→CH4+C2H4
根据以下所给条件回答问题:
(1)已知各物质的燃烧热如下表,请计算反应①的反应热ΔH1=_________ .
(2)如果要加快石油工业中丙烷的裂解速度,可以采取的措施是_________ .
A.高温低压B.低温高压C.高温高压D.低温低压
(3)在500℃下,按一定的原料气比和气流速度的条件下,不同载体催化剂对丙烷脱氢反应的影响如图所示。其中某一组实验数据如下表所示。(其中丙烷的转化率指的是总转化率,丙烯的选择性指最终转化为丙烯的丙烷占反应丙烷的百分比。)

①磷酸钙、磷酸锆、磷酸铝三种载体的催化效率最高的是_________ .
②经研究发现,不同载体的催化效果与载体本身的酸碱性有关,以下三种催化剂中催化效果最好的是_________ .
A.SiO2 B.Al2O3 C.MgO
③由上表计算该条件下,丙烷的转化率=_________ .;丙烯的选择性=_________ .
④根据化学平衡理论催化剂并不会改变平衡体系中的转化率和产率,但在丙烷催化生产丙烯的反应中,使用不同的催化剂所得到的丙烯的选择性却有不同。请说明原因:_________ .
(4)目前有一种便携式固体氧化物燃料电池,它以丙烷气体为燃料。电池中的一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,请写出该电池负极的电极反应式:_________
①C3H8→C3H6+H2 ②2 C3H6+9O2→6CO2+9H2O ③C3H8→CH4+C2H4
根据以下所给条件回答问题:
(1)已知各物质的燃烧热如下表,请计算反应①的反应热ΔH1=
| 物质 | H2 | CH4 | C2H4 | C3H6 | C3H8 |
| 燃烧热(KJ/mol) | 285.8 | 891.0 | 1411.0 | 2013.4 | 2217.8 |
A.高温低压B.低温高压C.高温高压D.低温低压
(3)在500℃下,按一定的原料气比和气流速度的条件下,不同载体催化剂对丙烷脱氢反应的影响如图所示。其中某一组实验数据如下表所示。(其中丙烷的转化率指的是总转化率,丙烯的选择性指最终转化为丙烯的丙烷占反应丙烷的百分比。)

| 物质 | 反应前(mol) | 反应后(mol) |
| C3H8 | 10 | |
| C3H6 | 0 | 1.02 |
| CO2 | 0 | 1.98 |
| C2H4 | 0 | 0.02 |
| CH4 | 0 | 0.02 |
①磷酸钙、磷酸锆、磷酸铝三种载体的催化效率最高的是
②经研究发现,不同载体的催化效果与载体本身的酸碱性有关,以下三种催化剂中催化效果最好的是
A.SiO2 B.Al2O3 C.MgO
③由上表计算该条件下,丙烷的转化率=
④根据化学平衡理论催化剂并不会改变平衡体系中的转化率和产率,但在丙烷催化生产丙烯的反应中,使用不同的催化剂所得到的丙烯的选择性却有不同。请说明原因:
(4)目前有一种便携式固体氧化物燃料电池,它以丙烷气体为燃料。电池中的一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,请写出该电池负极的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】在体积为 的密闭容器中,进行如下化学反应:
的密闭容器中,进行如下化学反应: ,化学平衡常数
,化学平衡常数 与温度
与温度 的关系如下表:
的关系如下表:
回答下列问题:
(1)升高温度,化学平衡向______ (填“正反应”或“逆反应”)方向移动。
(2)在等温等容条件下,能判断该反应达到化学平衡状态的依据是______ 。
A. B.浓度商
B.浓度商 不再改变
不再改变
C.容器中的气体密度不再改变 D.
E. 不再改变 F.混合气体的平均相对分子质量不再改变
不再改变 F.混合气体的平均相对分子质量不再改变
(3)若某温度下,体系平衡浓度符合下列关系: ,在此温度下,若该容器中含有
,在此温度下,若该容器中含有 、
、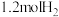 、
、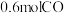 、
、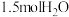 ,则此时反应所处的状态为
,则此时反应所处的状态为______ 。(填“向正反应方向进行中”、“向逆反应方向进行中”或“平衡状态”)
(4)在一定条件下发生上述反应,反应过程中速率随时间的变化如图所示,请根据速率的变化回答采取的措施。 时刻改变的条件是
时刻改变的条件是______ ; 时刻改变的条件是
时刻改变的条件是______ 。

(5)在 条件下,将
条件下,将 和
和 按体积比
按体积比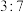 通入
通入 的恒容密闭容器中发生上述反应,
的恒容密闭容器中发生上述反应, 后反应达平衡,此时压强为
后反应达平衡,此时压强为 。则
。则 条件下
条件下 的转化率是
的转化率是______ ;该反应的分压平衡常数
______ 。( 为以分压表示的平衡常数,分压
为以分压表示的平衡常数,分压 总压
总压 物质的量分数)
物质的量分数)
 的密闭容器中,进行如下化学反应:
的密闭容器中,进行如下化学反应: ,化学平衡常数
,化学平衡常数 与温度
与温度 的关系如下表:
的关系如下表:
| 700 | 800 | 850 | 1000 | 1200 |
| 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)升高温度,化学平衡向
(2)在等温等容条件下,能判断该反应达到化学平衡状态的依据是
A.
 B.浓度商
B.浓度商 不再改变
不再改变C.容器中的气体密度不再改变 D.

E.
 不再改变 F.混合气体的平均相对分子质量不再改变
不再改变 F.混合气体的平均相对分子质量不再改变(3)若某温度下,体系平衡浓度符合下列关系:
 ,在此温度下,若该容器中含有
,在此温度下,若该容器中含有 、
、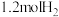 、
、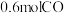 、
、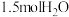 ,则此时反应所处的状态为
,则此时反应所处的状态为(4)在一定条件下发生上述反应,反应过程中速率随时间的变化如图所示,请根据速率的变化回答采取的措施。
 时刻改变的条件是
时刻改变的条件是 时刻改变的条件是
时刻改变的条件是
(5)在
 条件下,将
条件下,将 和
和 按体积比
按体积比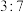 通入
通入 的恒容密闭容器中发生上述反应,
的恒容密闭容器中发生上述反应, 后反应达平衡,此时压强为
后反应达平衡,此时压强为 。则
。则 条件下
条件下 的转化率是
的转化率是
 为以分压表示的平衡常数,分压
为以分压表示的平衡常数,分压 总压
总压 物质的量分数)
物质的量分数)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】二甲醚是一种清洁能源,用水煤气制取甲醚的原理如下:
I.CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
II.2CH3OH(g)===CH3OCH3(g)+H2O(g)
(1)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为_______ 反应(填“吸热”或“放热”)。
(2)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是______________ (填“a”或“b”)。

②下列说法能表明反应已达平衡状态的是____ (填标号)。
A.容器中气体的压强不再变化 B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化 D.v正(H2)=2v正(CH3OH)
(3)500K时,在2L密闭容器中充入4 mol CO和8 mol H2,4 min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3) ,则:
① 0~4 min,反应I的v(H2)=______ ,反应I的平衡常数K=______ 。
② 反应II中CH3OH的转化率α=_______ 。

(4)二甲醚燃料电池的工作原理如图所示,则X电极的电极反应式为_______ 。用该电池对铁制品镀铜,当铁制品质量增加64 g时,理论上消耗二甲醚的质量为_______ g(精确到0.01)。
I.CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)II.2CH3OH(g)===CH3OCH3(g)+H2O(g)
(1)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为
(2)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是

②下列说法能表明反应已达平衡状态的是
A.容器中气体的压强不再变化 B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化 D.v正(H2)=2v正(CH3OH)
(3)500K时,在2L密闭容器中充入4 mol CO和8 mol H2,4 min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3) ,则:
① 0~4 min,反应I的v(H2)=
② 反应II中CH3OH的转化率α=

(4)二甲醚燃料电池的工作原理如图所示,则X电极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为两种无毒气体。T ℃时,将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟汽车尾气转化,容器中NO的物质的量随时间变化如图所示。
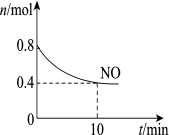
(1)NO、CO转化为两种无毒气体的化学方程式是___________ 。
(2)反应开始至10 min,v(NO)=___________ mol/(L·min)。
(3)下列说法正确的是___________ 。
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/L
Ⅱ.在恒温下,将4mol的H2(g)和2mol的CO(g)充入1L恒容的密闭容器中发生如下反应:CO(g) + 2H2(g) CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
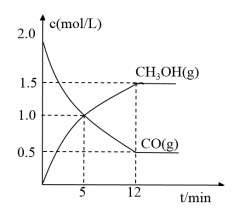
回答下列问题:
(4)0-5min内,H2 (g)的平均反应速率是___________ mol/(L·min)。
(5)12min时,v正___________ v逆(填“>”“<”或“=”)。
(6)设起始压强为P,平衡时压强为P0,则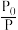 的值为
的值为___________ 。
(7)根据反应原理下列描述能说明反应达到最大限度的是___________。

(1)NO、CO转化为两种无毒气体的化学方程式是
(2)反应开始至10 min,v(NO)=
(3)下列说法正确的是
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/L
Ⅱ.在恒温下,将4mol的H2(g)和2mol的CO(g)充入1L恒容的密闭容器中发生如下反应:CO(g) + 2H2(g)
 CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
回答下列问题:
(4)0-5min内,H2 (g)的平均反应速率是
(5)12min时,v正
(6)设起始压强为P,平衡时压强为P0,则
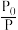 的值为
的值为(7)根据反应原理下列描述能说明反应达到最大限度的是___________。
| A.CO(g)、H2(g)、CH3OH(g)的物质的量比为1∶2∶1 |
| B.混合气体的压强不随时间的变化而改变 |
| C.单位时间内每消耗2amolH2(g),同时生成amolCH3OH(g) |
| D.反应速率:v(H2)=2v(CO) |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】二氧化碳的过量排放可对环境造成很大影响。

(1)写出图1中岩溶的化学方程式:___ 。
(2)CO2是引起温室效应的主要物质,可用于生产甲醇。在恒容的密闭容器中,通入1molCO2和1.5molH2,发生的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H<0,测得CO2的转化率随温度和压强的变化如图2。
CH3OH(g)+H2O(g)△H<0,测得CO2的转化率随温度和压强的变化如图2。
①X代表的物理量是___ 。
②Y1___ (填“>”或“<”)Y2,判断的理由是___ 。
③保持温度不变,反应达到平衡后,测得气体压强p为起始压强p0的0.8倍,则反应平衡常数KP=___ (用p表示,分压=物质的量分数×总压,列出计算式即可)。
(3)已知常温下,H2CO3的电离平衡常数:K1=4.4×10-7、K2=4.7×10-11,则CO +H2O
+H2O HCO
HCO +OH-的平衡常数K=
+OH-的平衡常数K=___ (保留两位有效数字)。

(1)写出图1中岩溶的化学方程式:
(2)CO2是引起温室效应的主要物质,可用于生产甲醇。在恒容的密闭容器中,通入1molCO2和1.5molH2,发生的反应为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H<0,测得CO2的转化率随温度和压强的变化如图2。
CH3OH(g)+H2O(g)△H<0,测得CO2的转化率随温度和压强的变化如图2。①X代表的物理量是
②Y1
③保持温度不变,反应达到平衡后,测得气体压强p为起始压强p0的0.8倍,则反应平衡常数KP=
(3)已知常温下,H2CO3的电离平衡常数:K1=4.4×10-7、K2=4.7×10-11,则CO
 +H2O
+H2O HCO
HCO +OH-的平衡常数K=
+OH-的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】减少NOx、CO2的排放,实现资源化利用是化学工作者研究的重要课题。
(1)尿素水解生成的NH3催化还原NO是重要的烟气脱硝技术,且为可逆过程。反应过程与能量关系如图1,在以Fe2O3为主的催化剂表面可能发生的反应过程如图2。
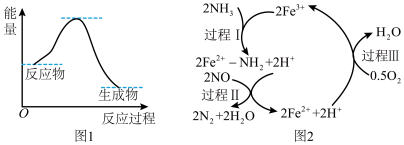
①NH3催化还原NO为_______ (填“放热”“吸热”)反应。
②上述脱硝的总反应化学方程式为:_______ 。
(2)电厂烟气脱氮的反应为:4NH3(g) + 6NO(g) 5N2(g) + 6H2O(g) ΔH<0,现向某2 L密闭容器中分别投入一定量的NH3、NO发生以上反应,其他条件相同时,在甲、乙两种催化剂的作用下,相同时间内NO的转化率与温度的关系如图3。工业上应选择催化剂
5N2(g) + 6H2O(g) ΔH<0,现向某2 L密闭容器中分别投入一定量的NH3、NO发生以上反应,其他条件相同时,在甲、乙两种催化剂的作用下,相同时间内NO的转化率与温度的关系如图3。工业上应选择催化剂_______ (填“甲”或“乙”)。在催化剂甲的作用下,温度高于210°C时,NO转化率降低的可能原因是_______ 。
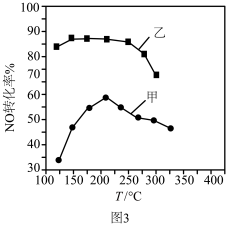
(3)工业以NH3和CO2为原料合成尿素。液相中,合成尿素的热化学方程式为:2NH3(l) + CO2(l) H2O(l) + NH2CONH2(l) ΔH<0,在液相中,CO2的平衡转化率与温度、初始氨碳比(用L表示,L=
H2O(l) + NH2CONH2(l) ΔH<0,在液相中,CO2的平衡转化率与温度、初始氨碳比(用L表示,L= )、初始水碳比(用W表示,W=
)、初始水碳比(用W表示,W=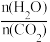 )关系如图4。
)关系如图4。
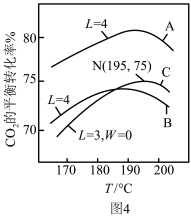
①曲线A、B中,_______ (填“A”或“B”)的W较小。
②对于液相反应,常用某组分M达到平衡时的物质的量分数x(M)代替平衡浓度来计算平衡常数(记作Kx)。195°C时,2NH3(l) + CO2(l) H2O(l) + NH2CONH2(l)的Kx的值为
H2O(l) + NH2CONH2(l)的Kx的值为_______ 。
(4)氨气可以用于燃料电池,其原理是氨气与氧气在碱性条件下反应生成一种常见的无毒气体和水,负极的电极反应式是_______ 。
(1)尿素水解生成的NH3催化还原NO是重要的烟气脱硝技术,且为可逆过程。反应过程与能量关系如图1,在以Fe2O3为主的催化剂表面可能发生的反应过程如图2。

①NH3催化还原NO为
②上述脱硝的总反应化学方程式为:
(2)电厂烟气脱氮的反应为:4NH3(g) + 6NO(g)
 5N2(g) + 6H2O(g) ΔH<0,现向某2 L密闭容器中分别投入一定量的NH3、NO发生以上反应,其他条件相同时,在甲、乙两种催化剂的作用下,相同时间内NO的转化率与温度的关系如图3。工业上应选择催化剂
5N2(g) + 6H2O(g) ΔH<0,现向某2 L密闭容器中分别投入一定量的NH3、NO发生以上反应,其他条件相同时,在甲、乙两种催化剂的作用下,相同时间内NO的转化率与温度的关系如图3。工业上应选择催化剂
(3)工业以NH3和CO2为原料合成尿素。液相中,合成尿素的热化学方程式为:2NH3(l) + CO2(l)
 H2O(l) + NH2CONH2(l) ΔH<0,在液相中,CO2的平衡转化率与温度、初始氨碳比(用L表示,L=
H2O(l) + NH2CONH2(l) ΔH<0,在液相中,CO2的平衡转化率与温度、初始氨碳比(用L表示,L= )、初始水碳比(用W表示,W=
)、初始水碳比(用W表示,W=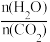 )关系如图4。
)关系如图4。
①曲线A、B中,
②对于液相反应,常用某组分M达到平衡时的物质的量分数x(M)代替平衡浓度来计算平衡常数(记作Kx)。195°C时,2NH3(l) + CO2(l)
 H2O(l) + NH2CONH2(l)的Kx的值为
H2O(l) + NH2CONH2(l)的Kx的值为(4)氨气可以用于燃料电池,其原理是氨气与氧气在碱性条件下反应生成一种常见的无毒气体和水,负极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮氧化物(NOx)的排放对环境造成严重污染。工业上可利用C(s)+2NO(g)⇌CO2(g)+N2(g)反应处理氮氧化物。回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ·mol-1,碳的燃烧热为393.5kJ·mol-1,则C(s)+2NO(g)⇌CO2(g)+N2(g) ΔH2=_______ kJ·mol-1
(2)一定温度下,在恒容密闭容器中充入足量单质C和一定量NO,发生上述反应。下列情况能说明反应达到化学平衡状态的是_______ (填字母标号),反应达平衡后继续通入一定量NO,NO的转化率_______ (填“增大”、“减小”或“不变”)。
A.υ(NO)=2υ(CO2) B.容器内气体的压强保持不变
C.NO与CO2的浓度比保持不变 D.混合气体的平均相对分子质量保持不变
(3)某温度下,向盛有足量单质C的恒容密闭容器通入NO,使其初始浓度为1mol·L-1,根据平衡时以某物质表示的 正(或
正(或 逆)、浓度的数值,绘制出图中甲乙两点。
逆)、浓度的数值,绘制出图中甲乙两点。
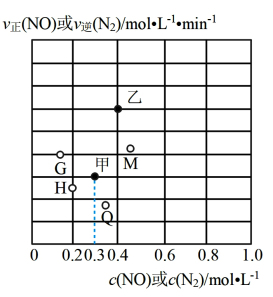
①甲点对应的物质是_______ (填化学式);该反应的平衡常数为_______ 。
②将温度降低至某一温度时,反应重新达到平衡,此时体系的压强为p=105Pa,NO的体积分数为30%,则N2的分压为p(N2)=_______ Pa(气体分压=总压×该气体物质的量分数),则图中甲点可能移动至点位置_______ (填字母标号)。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ·mol-1,碳的燃烧热为393.5kJ·mol-1,则C(s)+2NO(g)⇌CO2(g)+N2(g) ΔH2=
(2)一定温度下,在恒容密闭容器中充入足量单质C和一定量NO,发生上述反应。下列情况能说明反应达到化学平衡状态的是
A.υ(NO)=2υ(CO2) B.容器内气体的压强保持不变
C.NO与CO2的浓度比保持不变 D.混合气体的平均相对分子质量保持不变
(3)某温度下,向盛有足量单质C的恒容密闭容器通入NO,使其初始浓度为1mol·L-1,根据平衡时以某物质表示的
 正(或
正(或 逆)、浓度的数值,绘制出图中甲乙两点。
逆)、浓度的数值,绘制出图中甲乙两点。
①甲点对应的物质是
②将温度降低至某一温度时,反应重新达到平衡,此时体系的压强为p=105Pa,NO的体积分数为30%,则N2的分压为p(N2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】建设“美丽中国”,研究消除氮氧化物污染对打造绿色宜居环境意义重大。
(1)CO与 在
在 催化作用下,反应分两步进行。
催化作用下,反应分两步进行。
Ⅰ.
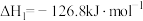
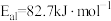
Ⅱ.
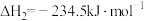

决定总反应速率的是第_______ (填“Ⅰ”或“Ⅱ”)步反应。总反应的热化学方程式为_______ 。
(2)在催化剂作用下 还原
还原 的反应如下:
的反应如下: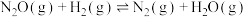
 。已知该反应的
。已知该反应的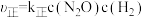
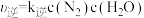 (
( 、
、 分别为正、逆反应速率常数)。该反应的
分别为正、逆反应速率常数)。该反应的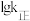 、
、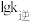 随温度倒数变化的曲线如图所示。
随温度倒数变化的曲线如图所示。

①表示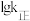 变化的曲线是
变化的曲线是_______ (填“a”或“b”)。
②M点对应温度下的平衡常数K=_______ 。
(3)T℃时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol ,发生反应:
,发生反应: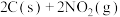
 。经t min,测得各容器中
。经t min,测得各容器中 的转化率与容器容积的关系如图所示。
的转化率与容器容积的关系如图所示。

①a、c两点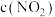 的大小是a
的大小是a_______ c(填“>”“=”或“<”)。
②a点对应的容器,t min内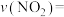
_______ (用含字母的代数式表示)。
③a、b、c三点中,已达平衡状态的有_______ 。
④b点前 转化率随容器容积增大而增大的原因是
转化率随容器容积增大而增大的原因是_______ 。
(1)CO与
 在
在 催化作用下,反应分两步进行。
催化作用下,反应分两步进行。Ⅰ.

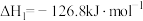
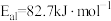
Ⅱ.

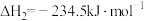

决定总反应速率的是第
(2)在催化剂作用下
 还原
还原 的反应如下:
的反应如下: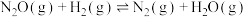
 。已知该反应的
。已知该反应的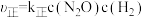
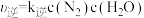 (
( 、
、 分别为正、逆反应速率常数)。该反应的
分别为正、逆反应速率常数)。该反应的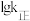 、
、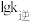 随温度倒数变化的曲线如图所示。
随温度倒数变化的曲线如图所示。
①表示
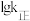 变化的曲线是
变化的曲线是②M点对应温度下的平衡常数K=
(3)T℃时,向容积不等的恒容密闭容器中分别加入足量活性炭和1mol
 ,发生反应:
,发生反应: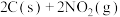
 。经t min,测得各容器中
。经t min,测得各容器中 的转化率与容器容积的关系如图所示。
的转化率与容器容积的关系如图所示。
①a、c两点
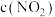 的大小是a
的大小是a②a点对应的容器,t min内
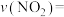
③a、b、c三点中,已达平衡状态的有
④b点前
 转化率随容器容积增大而增大的原因是
转化率随容器容积增大而增大的原因是
您最近一年使用:0次
【推荐2】控制和治理 是解决温室效应及能源问题的有效途径。
是解决温室效应及能源问题的有效途径。
(1)研究表明,在 催化剂作用下,
催化剂作用下, 和
和 反应生成液态甲醇和液态水,该反应的热化学方程式为
反应生成液态甲醇和液态水,该反应的热化学方程式为_______ 。[已知25℃、 下,
下, 和
和 的摩尔燃烧焓分别为
的摩尔燃烧焓分别为 和
和 。]
。]
(2)已知
 ,在两个固定容积均为
,在两个固定容积均为 的密闭容器中以不同的
的密闭容器中以不同的 充入
充入 和
和 ,
, 的平衡转化率
的平衡转化率 与温度的关系如图所示。
与温度的关系如图所示。

①X________ (填“>”“<”或“=”)2.0。
②若起始加入的 、
、 的物质的量分别为
的物质的量分别为 和
和 ,计算P点时的化学平衡常数K=
,计算P点时的化学平衡常数K=______ 。
③比较P点和Q点的化学平衡常数:K P______ KQ (填“>”“<”或“=”)。
(3)以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能电池将 转化为低碳烯烃的工作原理如图所示。产生乙烯的电极反应式为
转化为低碳烯烃的工作原理如图所示。产生乙烯的电极反应式为_______ 。

 是解决温室效应及能源问题的有效途径。
是解决温室效应及能源问题的有效途径。(1)研究表明,在
 催化剂作用下,
催化剂作用下, 和
和 反应生成液态甲醇和液态水,该反应的热化学方程式为
反应生成液态甲醇和液态水,该反应的热化学方程式为 下,
下, 和
和 的摩尔燃烧焓分别为
的摩尔燃烧焓分别为 和
和 。]
。](2)已知

 ,在两个固定容积均为
,在两个固定容积均为 的密闭容器中以不同的
的密闭容器中以不同的 充入
充入 和
和 ,
, 的平衡转化率
的平衡转化率 与温度的关系如图所示。
与温度的关系如图所示。
①X
②若起始加入的
 、
、 的物质的量分别为
的物质的量分别为 和
和 ,计算P点时的化学平衡常数K=
,计算P点时的化学平衡常数K=③比较P点和Q点的化学平衡常数:K P
(3)以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能电池将
 转化为低碳烯烃的工作原理如图所示。产生乙烯的电极反应式为
转化为低碳烯烃的工作原理如图所示。产生乙烯的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】在某一容积为5 L的体积不变的密闭容器内,加入 0.3 mol的CO和0.3 mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:

(1)根据图上数据,反应开始至达到平衡时,CO的化学反应速率为v(CO)=________ mol/(L·min),该温度(800℃)下的平衡常数K=____________ 。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有_______ (填字母)
E.加入催化剂
G.移出一氧化碳气体
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.2 mol的CO2和0.2 mol的H2,在相同的条件下,反应达平衡时,c(CO)=___________ mol/L。
(4)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol 的水蒸气,重新达到平衡后,H2O的转化率_____________ (填“升高”、“降低”还是“不变”)。
(5)在催化剂存在和800℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09mol/L,c(CO2)=c(H2)=0.13mol/L,则此反应是否处于平衡状态:____________ (填“是”或“否”),若没有处于平衡状态则该反应向____________ 方向移动。(填“正反应”或“逆反应”)
 CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:
(1)根据图上数据,反应开始至达到平衡时,CO的化学反应速率为v(CO)=
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有
| A.升高温度 |
| B.降低温度 |
| C.增大压强 |
| D.减小压强 |
E.加入催化剂
G.移出一氧化碳气体
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.2 mol的CO2和0.2 mol的H2,在相同的条件下,反应达平衡时,c(CO)=
(4)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol 的水蒸气,重新达到平衡后,H2O的转化率
(5)在催化剂存在和800℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09mol/L,c(CO2)=c(H2)=0.13mol/L,则此反应是否处于平衡状态:
您最近一年使用:0次




