某工业废水中Pb2+及其与OH-形成的微粒的浓度分数a随溶液pH变化的关系如图所示。已知NH3·H2O的Kb=1.74×10-5。向Pb(NO3)2溶液中滴加氨水,关于该过程的说法错误的是


A.c(NO )与c(Pb2+)的比值减小后增大,pH>10后不变 )与c(Pb2+)的比值减小后增大,pH>10后不变 |
| B.Pb2+的浓度分数值减小 |
C.pH=7时,存在的阳离子仅有Pb2+、Pb(OH)+、H+以及NH |
D.溶液中Pb2+与Pb(OH)2浓度相等时,氨主要以NH 的形式存在 的形式存在 |
更新时间:2021-09-10 14:58:02
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时,将1.0LWmol/LCH3COOH溶液与0.1molNaOH固体混合充分反应后,向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述中错误的是
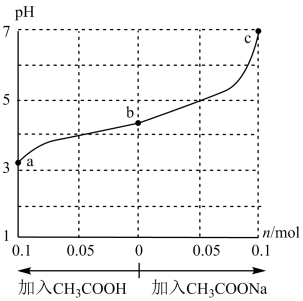

A.b点混合液中 |
| B.a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b |
| C.加入CH3COONa至CH3COOH与CH3COONa的物质的量之比为1:1时,存在2c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-) |
D.25℃时,CH3COOH的电离平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,向某Na2CO3溶液中加入稀盐酸,溶液中含碳微粒的物质的量分数(φ)随溶液pH变化的部分情况如图所示。下列说法中正确的是
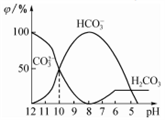

| A.Na2CO3溶液中c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3) |
| B.pH=8时,溶液中c(Cl-)=c(Na+) |
| C.pH =7时,溶液中的c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-) |
D.25℃时,CO32-+H2O HCO3-+OH-的Kh=10-10mol·L-1 HCO3-+OH-的Kh=10-10mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】痛风性关节病的发病机理和尿酸钠有关。室温下,将尿酸钠(NaUr)的悬浊液静置,取上层清液滴加盐酸,溶液中尿酸的浓度c(HUr)与pH的关系如图所示。已知Ksp(NaUr)=4.9×10-5mol2·L-2,Ka(HUr)=2.0×10-6mol·L-1。下列说法错误的是( )


| A.上层清液中,c(Ur-)=7.0×10-3mol·L-1 |
B.M→N的变化过程中,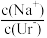 逐渐减小 逐渐减小 |
| C.N点时,c(Cl-)=c(HUr) |
| D.当c(HUr)=c(Ur-)时,c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】如图为室温时不同pH下磷酸钠盐溶液中含磷微粒形态的分布,其中a、b、c三点对应的pH分别为2.12、7.21、12.66,其中δ表示含磷微粒的物质的量分数。下列说法正确的是


A.选择酚酞作指示剂,用NaOH溶液滴加磷酸溶液的反应为H3PO4+3OH-=PO +3H2O +3H2O |
| B.室温下,水电离的c(H+)·c(OH-):a<b<c |
C.a、b、c点对应水溶液中c(H3PO4)+c(H2PO )+c(HPO )+c(HPO )+c(PO )+c(PO )之和相等 )之和相等 |
| D.室温下,H3PO4的第三级电离常数的数量级为10-12 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液的pH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是


| A.a点溶液中:c(NH3•H2O)+c(H+)=c(OH-) |
B.c点溶液中:n(NH3•H2O)<n(NH ) ) |
C.在0<V(NaOH)≦100的区间,发生的反应是NH +OH-═NH3•H2O +OH-═NH3•H2O |
| D.a、b、c、d四个点中,水的电离程度最大的是b |
您最近一年使用:0次



