在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)一定温度下,将2molN2和6molH2置于1L的恒容密闭容器中发生如下反应: N2(g)+3H2(g) 2NH3(g) ΔH<0,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:
2NH3(g) ΔH<0,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:
①上表中T1_____ T2(填“>”或“ <”或“=”),其中a、b、80%三者的大小关系是_____ (用含“>”“<”“=”的关系式表示)。
②研究表明,合成氨的速率与相关物质的浓度关系为v= ,k为速率常数。以下说法正确的是
,k为速率常数。以下说法正确的是_____ (填字母序号)。
A.升高温度,k值增大
B.T2℃时若容器内混合气体平均相对分子质量为12且保持不变,则反应达到平衡状态
C.一定温度下将原容器中的NH3及时分离出来可使v减小
D.合成氨达到平衡后,增大c(N2)可使正反应速率在达到新平衡的过程中始终增大。
③已知某温度下该反应达平衡时各物质均为1mol,容器容积为1L,保持温度和压强不变,又充入3molN2后,平衡_____ (填“向左移动”“向右移动”或“不移动”)。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g) 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:

①该反应的ΔH______ 0(填“>”或“<”)。
②若容器Ⅰ的体积为2 L,反应在370 ℃下进行,20 s后达到平衡,则0~20 s内容器Ⅰ中用O2表示的反应速率为___________ 。B点对应的平衡常数K=_____ (保留两位有效数字)。
③图中A、C、D三点容器内气体密度由大到小的顺序是___________ 。
④若容器Ⅳ体积为1 L,反应在370 ℃下进行,则起始时反应___________ 移动(填“向正反应方向”“向逆反应方向”或“不”)。
(1)一定温度下,将2molN2和6molH2置于1L的恒容密闭容器中发生如下反应: N2(g)+3H2(g)
 2NH3(g) ΔH<0,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:
2NH3(g) ΔH<0,测得不同温度、不同时间段内合成氨反应中N2的转化率,数据如下:| 1小时 | 2小时 | 3小时 | 4小时 | |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a | b |
①上表中T1
②研究表明,合成氨的速率与相关物质的浓度关系为v=
 ,k为速率常数。以下说法正确的是
,k为速率常数。以下说法正确的是A.升高温度,k值增大
B.T2℃时若容器内混合气体平均相对分子质量为12且保持不变,则反应达到平衡状态
C.一定温度下将原容器中的NH3及时分离出来可使v减小
D.合成氨达到平衡后,增大c(N2)可使正反应速率在达到新平衡的过程中始终增大。
③已知某温度下该反应达平衡时各物质均为1mol,容器容积为1L,保持温度和压强不变,又充入3molN2后,平衡
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g)
 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示:
①该反应的ΔH
②若容器Ⅰ的体积为2 L,反应在370 ℃下进行,20 s后达到平衡,则0~20 s内容器Ⅰ中用O2表示的反应速率为
③图中A、C、D三点容器内气体密度由大到小的顺序是
④若容器Ⅳ体积为1 L,反应在370 ℃下进行,则起始时反应
21-22高二上·重庆沙坪坝·阶段练习 查看更多[3]
山东师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)期中试卷02-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题
更新时间:2021-10-13 09:57:55
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。用 生产甲醇、乙醇。
生产甲醇、乙醇。
(1)已知: 的燃烧热为
的燃烧热为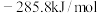 ,
, 的燃烧热为
的燃烧热为 ,
,
 ,则
,则

_______ kJ/mol。
(2)为探究用 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入 和
和 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 和
和 的物质的量(n)随时间的变化如图所示:
的物质的量(n)随时间的变化如图所示:

①从反应开始到平衡,氢气的平均反应速率
_______ 。
②下列措施能使 的平衡转化率增大的是
的平衡转化率增大的是_______ (填序号)。
A.在原容器中再充入
B.在原容器中再充入
C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
(3) 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为
 。设m为起始时的投料比,即
。设m为起始时的投料比,即 。通过实验得到如图所示图象:
。通过实验得到如图所示图象:

①图甲中投料比相同,温度从高到低的顺序为_______ 。
②图乙中 、
、 、
、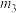 从大到小的顺序为
从大到小的顺序为_______ 。
③图丙表示在总压为5MPa的恒压条件下,且 时,平衡状态时各物质的物质的量分数与温度的关系,
时,平衡状态时各物质的物质的量分数与温度的关系, 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算表达式为
的计算表达式为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,代入数据,不用计算)。
 生产甲醇、乙醇。
生产甲醇、乙醇。(1)已知:
 的燃烧热为
的燃烧热为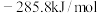 ,
, 的燃烧热为
的燃烧热为 ,
,
 ,则
,则

(2)为探究用
 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入 和
和 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 和
和 的物质的量(n)随时间的变化如图所示:
的物质的量(n)随时间的变化如图所示:
①从反应开始到平衡,氢气的平均反应速率

②下列措施能使
 的平衡转化率增大的是
的平衡转化率增大的是A.在原容器中再充入

B.在原容器中再充入

C.在原容器中充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
(3)
 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为
 。设m为起始时的投料比,即
。设m为起始时的投料比,即 。通过实验得到如图所示图象:
。通过实验得到如图所示图象:
①图甲中投料比相同,温度从高到低的顺序为
②图乙中
 、
、 、
、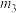 从大到小的顺序为
从大到小的顺序为③图丙表示在总压为5MPa的恒压条件下,且
 时,平衡状态时各物质的物质的量分数与温度的关系,
时,平衡状态时各物质的物质的量分数与温度的关系, 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算表达式为
的计算表达式为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】南京邮电大学有机电子与信息显示国家重点实验马延文教授课题组合成一种具有自修复功能的新型聚合物电解质,其部分合成流程如图所示,回答下列问题:
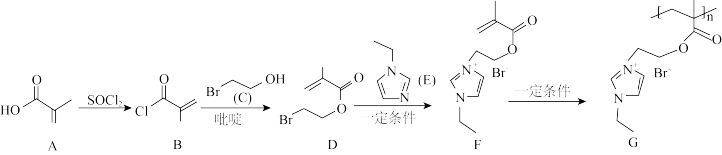
(1)A中含氧官能团的名称是___________ ;F→G的反应类型是___________ ;F的化学式为___________ 。
(2)溴乙烷难溶于水,而C(2—溴乙醇)能与水互溶,其原因是___________ 。
(3)写出B→D的化学方程式:___________ ;吪啶的作用是___________ (已知:吡啶的结构简式为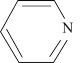 ,具有芳香性和弱碱性)。
,具有芳香性和弱碱性)。
(4)T是A的同分异构体,T同时具备下列条件的稳定结构有___________ 种(已知羟基连在双键的碳原子上不稳定,不考虑立体异构)。
①能发生银镜反应;
②与钠反应生成 。
。
其中,在核磁共振氢谱上有3组峰且峰的面积比为1:1:4的结构简式为___________ ;含手性碳原子的结构简式为___________ (写一种即可)。

(1)A中含氧官能团的名称是
(2)溴乙烷难溶于水,而C(2—溴乙醇)能与水互溶,其原因是
(3)写出B→D的化学方程式:
 ,具有芳香性和弱碱性)。
,具有芳香性和弱碱性)。(4)T是A的同分异构体,T同时具备下列条件的稳定结构有
①能发生银镜反应;
②与钠反应生成
 。
。其中,在核磁共振氢谱上有3组峰且峰的面积比为1:1:4的结构简式为
您最近一年使用:0次
【推荐3】CO2既是温室气体,也是重要的化工原料,二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g) N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①根据图表数据分析T1℃时,该反应在0~10min内的平均反应速率v(N2)=___ mol·L-1·min-1;计算该反应的平衡常数K=__ 。
②若30min后只改变某一条件,据上表中的数据判断改变的条件可能是__ (填字母编号)。
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:3:3,则达到新平衡时NO的转化率___ (填“升高”或“降低”),△H__ 0(填“>”或“<”)。
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.1kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1kJ·mol-1
2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5kJ·mol-1
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式___ 。
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=__ 。[常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
② 欲用5L Na2CO3溶液将23.3 g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为_________ 。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6]。(忽略溶液体积积的变化)
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g)
 N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的浓度如下:| 浓度/(mol/L)/时间/min | 0 | 10 | 20 | 30 | 40 |
| NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 |
| N2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
| CO2 | 0 | 0.42 | 080 | 0.80 | 1.2 |
①根据图表数据分析T1℃时,该反应在0~10min内的平均反应速率v(N2)=
②若30min后只改变某一条件,据上表中的数据判断改变的条件可能是
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:3:3,则达到新平衡时NO的转化率
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.1kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1kJ·mol-12CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-24.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5kJ·mol-1写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=
② 欲用5L Na2CO3溶液将23.3 g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】近日,科学家发现通过光照射铑(Rh)纳米粒子,优化 甲烷化反应。
甲烷化反应。 甲烷化涉及主要反应有:
甲烷化涉及主要反应有:
主反应:

副反应:

(1)已知: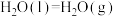
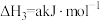 ,几种可燃物燃烧热的
,几种可燃物燃烧热的 数据如下表。
数据如下表。


___________  (用含a、b、d的字母表示)。
(用含a、b、d的字母表示)。
(2)在恒温恒容反应器中充入 和
和 ,假设只发生主反应,下列叙述错误的是___________(填字母标号)。
,假设只发生主反应,下列叙述错误的是___________(填字母标号)。
(3)近日,研究人员向两个反应室中均加入少量的 催化剂,并分别通入
催化剂,并分别通入 和
和 的混合气体,分别用高频率紫外LED灯照射、300℃热源加热,测得
的混合气体,分别用高频率紫外LED灯照射、300℃热源加热,测得 转化率、
转化率、 选择性与时间关系如图所示(提示:
选择性与时间关系如图所示(提示: 的选择性等于甲烷的物质的量与
的选择性等于甲烷的物质的量与 和
和 总物质的量之比,相当于
总物质的量之比,相当于 的收率)。
的收率)。

①以热源加热至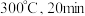 时生成的
时生成的 为
为___________  。
。
②根据图甲数据可知,LED光源的 的转化速率约等于热源的
的转化速率约等于热源的 的转化速率
的转化速率___________ (填整数)倍。实验结果表明,要提高 的收率,宜选择条件是
的收率,宜选择条件是___________ (填“光源”或“热源”)。
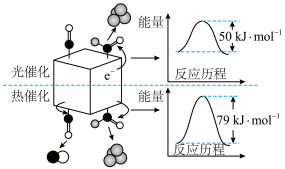
(4)研究人员利用如图所示的反应机理,解释图甲所示的实验结果,光催化条件下 选择性高、反应速率大的根本原因是
选择性高、反应速率大的根本原因是___________ 。
(5) 时,向恒容密闭容器中充入
时,向恒容密闭容器中充入 和
和 发生上述反应,起始总压强为
发生上述反应,起始总压强为 ,测得
,测得 的平衡转化率为50%,
的平衡转化率为50%, 的选择性为
的选择性为 ,则该温度下,上述主反应的平衡常数
,则该温度下,上述主反应的平衡常数 为
为___________ (列出计算式即可,要求带单位)。
 甲烷化反应。
甲烷化反应。 甲烷化涉及主要反应有:
甲烷化涉及主要反应有:主反应:


副反应:


(1)已知:
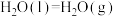
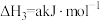 ,几种可燃物燃烧热的
,几种可燃物燃烧热的 数据如下表。
数据如下表。| 物质 |  |  |  |
燃烧热的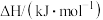 | b | c | d |


 (用含a、b、d的字母表示)。
(用含a、b、d的字母表示)。(2)在恒温恒容反应器中充入
 和
和 ,假设只发生主反应,下列叙述错误的是___________(填字母标号)。
,假设只发生主反应,下列叙述错误的是___________(填字母标号)。A.加入高效催化剂,能提高单位时间内 的产率 的产率 |
| B.混合气体的压强不随时间变化时达到平衡状态 |
C.反应体系中甲烷体积分数小于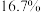 |
D.体系中 体积分数不变时一定达到平衡状态 体积分数不变时一定达到平衡状态 |
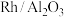 催化剂,并分别通入
催化剂,并分别通入 和
和 的混合气体,分别用高频率紫外LED灯照射、300℃热源加热,测得
的混合气体,分别用高频率紫外LED灯照射、300℃热源加热,测得 转化率、
转化率、 选择性与时间关系如图所示(提示:
选择性与时间关系如图所示(提示: 的选择性等于甲烷的物质的量与
的选择性等于甲烷的物质的量与 和
和 总物质的量之比,相当于
总物质的量之比,相当于 的收率)。
的收率)。
①以热源加热至
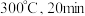 时生成的
时生成的 为
为 。
。②根据图甲数据可知,LED光源的
 的转化速率约等于热源的
的转化速率约等于热源的 的转化速率
的转化速率 的收率,宜选择条件是
的收率,宜选择条件是(4)研究人员利用如图所示的反应机理,解释图甲所示的实验结果,光催化条件下
 选择性高、反应速率大的根本原因是
选择性高、反应速率大的根本原因是
(5)
 时,向恒容密闭容器中充入
时,向恒容密闭容器中充入 和
和 发生上述反应,起始总压强为
发生上述反应,起始总压强为 ,测得
,测得 的平衡转化率为50%,
的平衡转化率为50%, 的选择性为
的选择性为 ,则该温度下,上述主反应的平衡常数
,则该温度下,上述主反应的平衡常数 为
为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】研究二氧化碳的回收对我国2060年实现碳中和具有现实意义:
(1)已知:①
②
③
写出 与
与 反应生成
反应生成 和
和 的热化学方程式:。
的热化学方程式:。_______ 。
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
①通过表格中的数值可以推断:该反应的
_______ 0(填“>”、“<”、或“=”),其正反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
② 的平衡转化率与压强、温度及氢碳比
的平衡转化率与压强、温度及氢碳比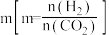 的关系分别如图a和图b所示。
的关系分别如图a和图b所示。
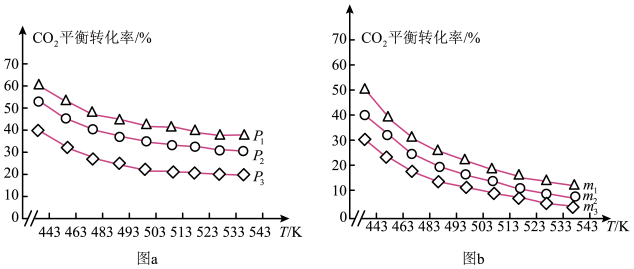
图a中压强从大到小的顺序为_______ ,图b中氢碳比m从大到小的顺序为_______ 。
(3)工业上也可以利用 和
和 合成甲醇:
合成甲醇: 某
某 恒温恒容密闭容器中充入
恒温恒容密闭容器中充入 和
和 发生反应,测得
发生反应,测得 和
和 浓度随时间变化如图所示:
浓度随时间变化如图所示:
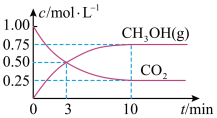
① 内,
内, 的平均反应速率为
的平均反应速率为_______  ,该温度下的平衡常数为
,该温度下的平衡常数为
_______ (单位可忽略)。若达平衡时,保持温度不变,向容器中再充入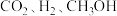 和
和 各
各 ,则此时v正
,则此时v正_______ v逆(填“>”、“<”、或“=”)。
②下列说法能说明反应达到化学平衡状态的是_______ 。
A. 的消耗速率与
的消耗速率与 的消耗速率之比为3∶1
的消耗速率之比为3∶1
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D. 和
和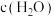 的浓度相等时
的浓度相等时
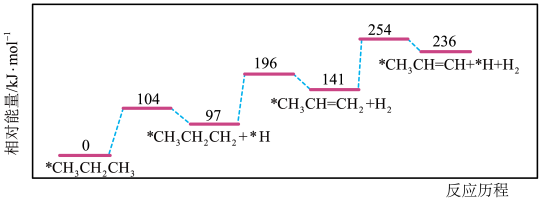
(4)丙烷脱氢是制备丙烯的一种常见方法,下图是某催化剂催化该过程的能量变化,*表示吸附在催化剂表面的物种。下列有关说法正确的是_______。
(1)已知:①

②

③

写出
 与
与 反应生成
反应生成 和
和 的热化学方程式:。
的热化学方程式:。(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:

| 温度/ | 400 | 500 |
| 平衡常数K | 9 | 5.3 |
①通过表格中的数值可以推断:该反应的

②
 的平衡转化率与压强、温度及氢碳比
的平衡转化率与压强、温度及氢碳比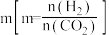 的关系分别如图a和图b所示。
的关系分别如图a和图b所示。
图a中压强从大到小的顺序为
(3)工业上也可以利用
 和
和 合成甲醇:
合成甲醇: 某
某 恒温恒容密闭容器中充入
恒温恒容密闭容器中充入 和
和 发生反应,测得
发生反应,测得 和
和 浓度随时间变化如图所示:
浓度随时间变化如图所示:
①
 内,
内, 的平均反应速率为
的平均反应速率为 ,该温度下的平衡常数为
,该温度下的平衡常数为
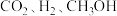 和
和 各
各 ,则此时v正
,则此时v正②下列说法能说明反应达到化学平衡状态的是
A.
 的消耗速率与
的消耗速率与 的消耗速率之比为3∶1
的消耗速率之比为3∶1 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.
 和
和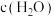 的浓度相等时
的浓度相等时(4)丙烷脱氢是制备丙烯的一种常见方法,下图是某催化剂催化该过程的能量变化,*表示吸附在催化剂表面的物种。下列有关说法正确的是_______。

A. 丙烷中的总键能大于 丙烷中的总键能大于 丙烯及 丙烯及 氢气的总键能之和 氢气的总键能之和 |
| B.在该条件下,所得丙烯中不含其它有机物 |
| C.该过程中发生了碳碳键的断裂与形成 |
D.相同条件下在该催化剂表面,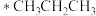 比 比 脱氢更困难 脱氢更困难 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】探究H2的合成反应平衡的影响因素,有利于提高H2的产率。以C、H2O为原料合成H2涉及的主要反应如下:
I.C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131 kJ/mol
II.CO(g) +H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ/mol
(1)已知反应II逆反应活化能为210 kJ/mol,则反应II的正反应活化能为_______ 。
(2)在一装有压强传感器的恒温恒容密闭容器中,加入足量的C(s)和一定量的H2O(g),发生上述反应,测得压强变化如下表:
①随着反应的进行,压强变化越来越慢,原因是_______ 。
②反应达平衡后,p(CO)+p(CO2)=_______ ,已知该温度下,反应I压强平衡常数Kp(I)=3 MPa,则反应II压强平衡常数Kp(II)=_______ 。
(3)不同压强下,投入足量C(s)和一定量H2O(g),实验测定C(s)的平衡转化率和H2(g)的平衡产率随温度的变化关系如下图所示。

其中纵坐标表示C(s)的平衡转化率的是图_______ .(填“甲”或“乙”);压强P1、P2、P3由大到小的顺序为_______ ;图乙中T,温度时,三条曲线几乎交于一点的原因是_______ 。
I.C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131 kJ/mol
II.CO(g) +H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ/mol
(1)已知反应II逆反应活化能为210 kJ/mol,则反应II的正反应活化能为
(2)在一装有压强传感器的恒温恒容密闭容器中,加入足量的C(s)和一定量的H2O(g),发生上述反应,测得压强变化如下表:
| 时间(min) | 0 | 10 | 20 | 30 | 40 | ∞ |
| 压强(MPa) | 5.0 | 6.5 | 7.0 | 7.4 | 7.5 | 7.5 |
②反应达平衡后,p(CO)+p(CO2)=
(3)不同压强下,投入足量C(s)和一定量H2O(g),实验测定C(s)的平衡转化率和H2(g)的平衡产率随温度的变化关系如下图所示。

其中纵坐标表示C(s)的平衡转化率的是图
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】镓(31Ga)、锗(32Ge)都是重要的稀有金属,在化学催化剂、半导体材料、新能源等领域应用广泛,可从锗煤燃烧后的粉煤灰(含 Ga2O3、GeO2、SiO2、Al2O3)中提取, 部分流程如下:

已知:
(1)滤渣的主要成分为_____ 。
(2)①中发生的反应有 Al2O3+6H+=2Al3++3H2O、Ga2O3+6H+=2Ga3++3H2O 和_____ 。
(3)操作 a 的名称是_____ ,②中控制温度的范围是_____ (填字母序号)。
a.20~84℃ b.84~183℃ c.84~201℃
(4)④中发生反应的化学方程式是__________________________________________ 。
(5)镓能与沸水剧烈反应生成氢气,锗在加热条件下与盐酸或稀硫酸不反应。从原子结构角度解释其原因:______________________
(6)用浓盐酸酸化的磷酸三丁酯(TBP)可以从残液中萃取 Ga3+,相关反应为:TBP+GaCl3+HCl TBPH+·GaCl
TBPH+·GaCl 。用稀 NaOH 溶液对有机相进行反萃取,用盐酸调节反萃取液 pH 至 5~6,然后升温至 85~95℃水解得到 Ga(OH)3,经后续处理得到粗镓。结合化学用语解释用稀 NaOH 溶液对有机相进行反萃取的原因:
。用稀 NaOH 溶液对有机相进行反萃取,用盐酸调节反萃取液 pH 至 5~6,然后升温至 85~95℃水解得到 Ga(OH)3,经后续处理得到粗镓。结合化学用语解释用稀 NaOH 溶液对有机相进行反萃取的原因:_________________ 。
(7)电解法可以提纯粗镓,具体原理如图所示。镓在阳极溶解生成的 Ga3+与 NaOH 溶液反应生成 GaO ,GaO
,GaO 在阴极放电的电极反应式是
在阴极放电的电极反应式是_____________________ 。


已知:
| 物质 | GaCl3 | GeCl4 | AlCl3 |
| 沸点/℃ | 201 | 84 | 183(升华) |
(1)滤渣的主要成分为
(2)①中发生的反应有 Al2O3+6H+=2Al3++3H2O、Ga2O3+6H+=2Ga3++3H2O 和
(3)操作 a 的名称是
a.20~84℃ b.84~183℃ c.84~201℃
(4)④中发生反应的化学方程式是
(5)镓能与沸水剧烈反应生成氢气,锗在加热条件下与盐酸或稀硫酸不反应。从原子结构角度解释其原因:
(6)用浓盐酸酸化的磷酸三丁酯(TBP)可以从残液中萃取 Ga3+,相关反应为:TBP+GaCl3+HCl
 TBPH+·GaCl
TBPH+·GaCl 。用稀 NaOH 溶液对有机相进行反萃取,用盐酸调节反萃取液 pH 至 5~6,然后升温至 85~95℃水解得到 Ga(OH)3,经后续处理得到粗镓。结合化学用语解释用稀 NaOH 溶液对有机相进行反萃取的原因:
。用稀 NaOH 溶液对有机相进行反萃取,用盐酸调节反萃取液 pH 至 5~6,然后升温至 85~95℃水解得到 Ga(OH)3,经后续处理得到粗镓。结合化学用语解释用稀 NaOH 溶液对有机相进行反萃取的原因:(7)电解法可以提纯粗镓,具体原理如图所示。镓在阳极溶解生成的 Ga3+与 NaOH 溶液反应生成 GaO
 ,GaO
,GaO 在阴极放电的电极反应式是
在阴极放电的电极反应式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某学习小组探究 Mg 与 NaHCO3溶液反应的机理,做了如下探究。
实验一:
(1)写出 B 中生成气体的化学方程式_____ 。
实验二:
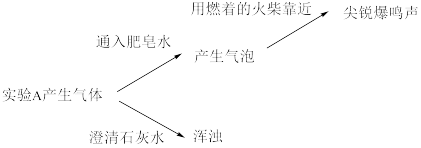
(2)实验 A 产生的气体有_____ 。
实验三:分别取少量实验 A 和 B 的上层清液于两支试管中,各加入 2 滴 BaCl2溶液,A 中立即产生白色沉淀,B 中无明显现象。
(3)实验三说明 Mg 与 NaHCO3溶液反应产生了_____ (填离子符号)。对 A 中白色固体的成分提出假设:
I.白色固体是 Mg(OH)2;II.白色固体是 MgCO3;III.白色固体是碱式碳酸镁。
实验四:
将 A 中白色沉淀过滤、洗涤后,取 0.1mol 加入 1mol/L 盐酸 800mL 恰好完全反应,产生标况下的 CO2气体 6.72L。
(4)白色沉淀的主要成分为_____ (写化学式)。
(5)综上所述,结合平衡移动原理解释实验 A 中产生现象的原因____________________________ 。
实验一:
| 实验 A | 实验 B | |
操作 | 在注射器中加入过量镁片(擦去表面氧化膜), 吸入 15mL 饱和 NaHCO3溶液。 | 在注射器中加入过量镁片(擦去表面 氧化膜),吸入 15mL 蒸馏水。 |
现象 | 有气体产生,20min 后注射器内壁和底部产生 大量白色沉淀 | 缓慢产生气体 |
(1)写出 B 中生成气体的化学方程式
实验二:

(2)实验 A 产生的气体有
实验三:分别取少量实验 A 和 B 的上层清液于两支试管中,各加入 2 滴 BaCl2溶液,A 中立即产生白色沉淀,B 中无明显现象。
(3)实验三说明 Mg 与 NaHCO3溶液反应产生了
I.白色固体是 Mg(OH)2;II.白色固体是 MgCO3;III.白色固体是碱式碳酸镁。
实验四:
将 A 中白色沉淀过滤、洗涤后,取 0.1mol 加入 1mol/L 盐酸 800mL 恰好完全反应,产生标况下的 CO2气体 6.72L。
(4)白色沉淀的主要成分为
(5)综上所述,结合平衡移动原理解释实验 A 中产生现象的原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】(一)合成氨工艺(流程如图所示)是人工固氮最重要的途径。

(1)利于提高合成氨平衡产率的条件有_______ 。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)标准平衡常数 ,其中
,其中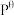 为标准压强(1X105Pa),pNH3、pN2和pH2为各组分的平衡分压,如pNH3=xNH3p,p为平衡总压,xNH3为平衡系统中NH3的物质的量分数。
为标准压强(1X105Pa),pNH3、pN2和pH2为各组分的平衡分压,如pNH3=xNH3p,p为平衡总压,xNH3为平衡系统中NH3的物质的量分数。
①N2和H2起始物质的量之比为1:3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则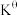 =
=_______ (用含w的最简式表示)
②图中可以示意标准平衡常数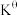 随温度T变化趋势的是
随温度T变化趋势的是_______ 。
A. B.
B. 
C. D.
D. 
(3)实际生产中,常用工艺条件,Fe作催化剂,控制温度773K,压强3.0X105Pa,原料中N2和H2物质的量之比为1:2.8。
①分析说明原料气中N2过量的理由_______ 。
②关于合成氨工艺的下列理解,正确的是_______ 。
A.合成氨反应在不同温度下的∆H和∆S都小于零
B.控制温度(773K)远高于室温,是为了保证尽可能的平衡转化率和快的反应速率
C.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
D.基于NH3有较强的分子间作用力可将其液化,不断将液氨移去,利于反应正向进行
E.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生。
(二)高铁酸钾(K2FeO4)可用作水处理剂。某同学通过“化学-电解法”探究的合成,其原理如图所示。接通电源,调节电压,将一定量Cl2通入KOH溶液,然后滴入含Fe3+的溶液,控制温度,可制得K2FeO4。

(4)请写出“化学法”得到FeO 的离子方程式
的离子方程式_______ 。
(5)请写出阳极的电极反应式(含FeO )
)_______ 。

(1)利于提高合成氨平衡产率的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)标准平衡常数
 ,其中
,其中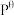 为标准压强(1X105Pa),pNH3、pN2和pH2为各组分的平衡分压,如pNH3=xNH3p,p为平衡总压,xNH3为平衡系统中NH3的物质的量分数。
为标准压强(1X105Pa),pNH3、pN2和pH2为各组分的平衡分压,如pNH3=xNH3p,p为平衡总压,xNH3为平衡系统中NH3的物质的量分数。①N2和H2起始物质的量之比为1:3,反应在恒定温度和标准压强下进行,NH3的平衡产率为w,则
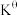 =
=②图中可以示意标准平衡常数
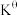 随温度T变化趋势的是
随温度T变化趋势的是A.
 B.
B. 
C.
 D.
D. 
(3)实际生产中,常用工艺条件,Fe作催化剂,控制温度773K,压强3.0X105Pa,原料中N2和H2物质的量之比为1:2.8。
①分析说明原料气中N2过量的理由
②关于合成氨工艺的下列理解,正确的是
A.合成氨反应在不同温度下的∆H和∆S都小于零
B.控制温度(773K)远高于室温,是为了保证尽可能的平衡转化率和快的反应速率
C.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
D.基于NH3有较强的分子间作用力可将其液化,不断将液氨移去,利于反应正向进行
E.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生。
(二)高铁酸钾(K2FeO4)可用作水处理剂。某同学通过“化学-电解法”探究的合成,其原理如图所示。接通电源,调节电压,将一定量Cl2通入KOH溶液,然后滴入含Fe3+的溶液,控制温度,可制得K2FeO4。

(4)请写出“化学法”得到FeO
 的离子方程式
的离子方程式(5)请写出阳极的电极反应式(含FeO
 )
)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】水煤气可作为燃料以及合成氨、有机合成、氢气制造等的原料。金属氧化物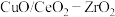 是制备水煤气的高效催化剂。回答下列问题:
是制备水煤气的高效催化剂。回答下列问题:
(1)一定温度下,在催化剂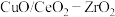 (用
(用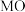 表示)的作用下合成水煤气的过程经历如下反应:
表示)的作用下合成水煤气的过程经历如下反应:
反应ⅰ:
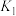
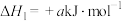
反应ⅱ:

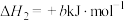 (已知
(已知 、
、 均大于0)
均大于0)
反应ⅲ:


_______  (用含
(用含 、
、 的代数式表示),平衡常数
的代数式表示),平衡常数
_______ (用含 、
、 的代数式表示)。
的代数式表示)。
(2)在恒容密闭容器中,加入足量的催化剂、碳单质和 水蒸气发生上述反应,达到平衡时各气体的物质的量与温度的关系如图所示。已知
水蒸气发生上述反应,达到平衡时各气体的物质的量与温度的关系如图所示。已知 时,容器中起始压强为
时,容器中起始压强为 。
。 的曲线的是
的曲线的是_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
② ,水蒸气的平衡转化率为
,水蒸气的平衡转化率为_______ 。
③ ,反应ⅲ的分压平衡常数
,反应ⅲ的分压平衡常数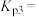
_______ ;升高温度,
_______ (填“增大”“减小”或“不变”)。
④ ,若起始压强由
,若起始压强由 升高为
升高为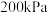 ,反应体系重新达到平衡时,反应ⅱ的分压平衡常数
,反应体系重新达到平衡时,反应ⅱ的分压平衡常数
_______ (填“增大”“减小”或“不变”);容器中 的分压
的分压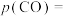
_______ 。
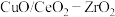 是制备水煤气的高效催化剂。回答下列问题:
是制备水煤气的高效催化剂。回答下列问题:(1)一定温度下,在催化剂
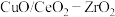 (用
(用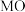 表示)的作用下合成水煤气的过程经历如下反应:
表示)的作用下合成水煤气的过程经历如下反应:反应ⅰ:

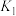
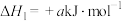
反应ⅱ:


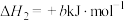 (已知
(已知 、
、 均大于0)
均大于0)反应ⅲ:



 (用含
(用含 、
、 的代数式表示),平衡常数
的代数式表示),平衡常数
 、
、 的代数式表示)。
的代数式表示)。(2)在恒容密闭容器中,加入足量的催化剂、碳单质和
 水蒸气发生上述反应,达到平衡时各气体的物质的量与温度的关系如图所示。已知
水蒸气发生上述反应,达到平衡时各气体的物质的量与温度的关系如图所示。已知 时,容器中起始压强为
时,容器中起始压强为 。
。
 的曲线的是
的曲线的是②
 ,水蒸气的平衡转化率为
,水蒸气的平衡转化率为③
 ,反应ⅲ的分压平衡常数
,反应ⅲ的分压平衡常数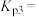

④
 ,若起始压强由
,若起始压强由 升高为
升高为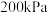 ,反应体系重新达到平衡时,反应ⅱ的分压平衡常数
,反应体系重新达到平衡时,反应ⅱ的分压平衡常数
 的分压
的分压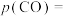
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】研究含氮和含硫化合物的性质在工业生产和环境保护中有重要意义。
(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)=2SO3(g) △H=-198kJ·mol-1
SO2(g)+NO2(g)=SO3(g)+NO(g) △H=-41.8kJ·mol-1
若CO的燃烧热为283 kJ·mol-1,则1molNO2和1mol CO 反应生成CO2和NO的能量变化示意图中E2=_________ kJ·mol-1
(2)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g) S(l)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:
S(l)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:_________
②第8分钟时,保持其他条件不变,将容器体积迅速压缩至1L,在10分钟时达到平衡,CO的物质的量变化了1mol。请在图B中画出SO2浓度从6~11分钟的变化曲线。
(3)已知某温度下,H2SO3的电离常数为K1≈l.5×10-2, K2≈1.0×10-7,用NaOH溶液吸收SO2,当溶液中HSO3-, SO32-离子相等时,溶液的pH值约为_________
(4)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为_________ ,连二亚硫酸根与HNO2反应的离子方程式_________ 。
(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)=2SO3(g) △H=-198kJ·mol-1
SO2(g)+NO2(g)=SO3(g)+NO(g) △H=-41.8kJ·mol-1
若CO的燃烧热为283 kJ·mol-1,则1molNO2和1mol CO 反应生成CO2和NO的能量变化示意图中E2=

(2)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g)
 S(l)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:
S(l)+2CO2(g)。某温度下在2L恒容密闭容器中通入2 molSO2和一定量的CO发生反应,5min后达到平衡,生成1molCO2。其他条件不变时SO2的平衡转化率反应温度的变化如图A,请解释其原因:②第8分钟时,保持其他条件不变,将容器体积迅速压缩至1L,在10分钟时达到平衡,CO的物质的量变化了1mol。请在图B中画出SO2浓度从6~11分钟的变化曲线。

(3)已知某温度下,H2SO3的电离常数为K1≈l.5×10-2, K2≈1.0×10-7,用NaOH溶液吸收SO2,当溶液中HSO3-, SO32-离子相等时,溶液的pH值约为
(4)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】苯乙烯是生产塑料和合成橡胶的重要有机原料,乙苯催化脱氢制备苯乙烯是目前生产苯乙烯的主要方法,反应如下: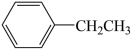 (g)
(g) 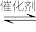
 (g) +H2(g)
(g) +H2(g)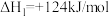 。
。
(1)工业上,通常在乙苯蒸气中掺混水蒸气,反应温度维持在600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了 以外的产物中苯乙烯的物质的量分数)示意图如下:
以外的产物中苯乙烯的物质的量分数)示意图如下:

①一般控制原料气中水油比n(水):n(乙苯)为9∶1,若水油比增大,乙苯的平衡转化率______ (填“增大”或“减小”),理由是________________________ 。
②控制反应温度为600℃的理由是________________________ 。
(2)某研究机构用 代替水蒸气开发了绿色化学合成工艺。反应方程式为:
代替水蒸气开发了绿色化学合成工艺。反应方程式为: (g)+CO2(g)
(g)+CO2(g)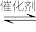
 (g)+CO(g)+H2O(g)
(g)+CO(g)+H2O(g) 。反应历程如图:
。反应历程如图:

①已知:
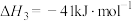 。则
。则
______  。
。
②催化剂表面酸碱性对乙苯脱氢反应性能影响较大,根据反应历程分析,如果催化剂表面碱性太强,对反应造成的影响为:________________________ (说出一点即可)。
③一定温度下,向恒容密闭容器中充入2mol乙苯和2mol ,起始压强为p0,平衡时容器内气体总物质的量为5mol,乙苯的转化率为
,起始压强为p0,平衡时容器内气体总物质的量为5mol,乙苯的转化率为______ ,用平衡分压代替平衡浓度表示的化学平衡常数
______ 。(已知:气体分压=气体总压×气体体积分数)
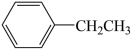 (g)
(g) 
 (g) +H2(g)
(g) +H2(g)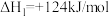 。
。(1)工业上,通常在乙苯蒸气中掺混水蒸气,反应温度维持在600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了
 以外的产物中苯乙烯的物质的量分数)示意图如下:
以外的产物中苯乙烯的物质的量分数)示意图如下:
①一般控制原料气中水油比n(水):n(乙苯)为9∶1,若水油比增大,乙苯的平衡转化率
②控制反应温度为600℃的理由是
(2)某研究机构用
 代替水蒸气开发了绿色化学合成工艺。反应方程式为:
代替水蒸气开发了绿色化学合成工艺。反应方程式为: (g)+CO2(g)
(g)+CO2(g)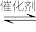
 (g)+CO(g)+H2O(g)
(g)+CO(g)+H2O(g) 。反应历程如图:
。反应历程如图:
①已知:

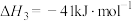 。则
。则
 。
。②催化剂表面酸碱性对乙苯脱氢反应性能影响较大,根据反应历程分析,如果催化剂表面碱性太强,对反应造成的影响为:
③一定温度下,向恒容密闭容器中充入2mol乙苯和2mol
 ,起始压强为p0,平衡时容器内气体总物质的量为5mol,乙苯的转化率为
,起始压强为p0,平衡时容器内气体总物质的量为5mol,乙苯的转化率为
您最近一年使用:0次



