化学平衡移动原理同样也适用于其它平衡,已知在氨水中存在下列平衡:NH3·H2O NH
NH +OH-
+OH-
(1)向氨水中加入NH4Cl固体时,平衡___________ 移动,(填“向右”或“向左”),c(OH-)___________ (填“增大”或“减小”或“不变”)。
(2)向氨水中加入MgCl2固体时,平衡___________ 移动,(填“向右”或“向左”), c(NH )
)___________ (填“增大”或“减小”或“不变”)
(3)常温下,将pH=8的氨水和pH=6的盐酸等体积混合,混合后c(H+)___________ c(OH-)(填“大于”、“小于”或“等于”)
(4)用物质的量分别为0.1mol的HCN和NaCN配成1L混合溶液,已知其中c(CN-)小于c(Na+),则溶液中c(H+)___________ c(OH-)(填“大于”。“小于”或“等于”),c(HCN)+c(CN-)=___________ mol/L
(5)室温下将amol/L的HCN与0.1mol/L的NaOH溶液等体积混合,反应后溶液中c(Na+)=c(CN-),则溶液显___________ 性(填“酸”“碱”“中”),用a 的代数式表示HCN的电离平衡常数Ka= ___________
 NH
NH +OH-
+OH-(1)向氨水中加入NH4Cl固体时,平衡
(2)向氨水中加入MgCl2固体时,平衡
 )
)(3)常温下,将pH=8的氨水和pH=6的盐酸等体积混合,混合后c(H+)
(4)用物质的量分别为0.1mol的HCN和NaCN配成1L混合溶液,已知其中c(CN-)小于c(Na+),则溶液中c(H+)
(5)室温下将amol/L的HCN与0.1mol/L的NaOH溶液等体积混合,反应后溶液中c(Na+)=c(CN-),则溶液显
更新时间:2021-11-02 19:57:39
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】已知25 ℃时0.1 mol·L-1醋酸溶液的pH约为3,向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了c(OH-),因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)上述两种解释中________ (填“甲”或“乙”)正确。
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的________ (填写编号字母),然后测定溶液的pH。
(3)若________ (填“甲”或“乙”)的解释正确,溶液的pH应________ (填“增大”、“减小”或“不变”)(已知25 ℃ 时,CH3COONH4溶液呈中性)。
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液。判断:
①溶液中共有________ 种粒子。
②溶液中有两种粒子的物质的量的和一定等于0.010 mol,它们是________ 和________ 。
③溶液中n(CH3COO-)+n(OH-)-n(H+)=________ mol。
(1)上述两种解释中
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的
| A.固体CH3COOK | B.固体CH3COONH4 |
| C.气体NH3 | D.固体NaHCO3 |
(3)若
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液。判断:
①溶液中共有
②溶液中有两种粒子的物质的量的和一定等于0.010 mol,它们是
③溶液中n(CH3COO-)+n(OH-)-n(H+)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)合成氨反应中使用的催化剂是______ (填名称),该反应温度一般控制在500℃,主要原因是______ 。
(2)下列措施,既能加快合成氨反应的反应速率,又能增大反应物转化率的是( )
A. 使用催化剂 B. 缩小容积体积 C. 提高反应温度 D. 移走NH3
(3)在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件下不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在下图中补充画出从t2到t4时刻正反应速率随时间的变化曲线__________ 。

(4)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是( )
A.溶液的pH增大 B.氨水的电离程度减小 C.c(NH4+)减小 D.c(OH-)减小
(5)石蕊(用HZ表示)试液中存在的电离平衡HZ(红色)HZ(蓝色)。通入氨气后石蕊试液呈蓝色,请用平衡移动原理解释____________ 。
(2)下列措施,既能加快合成氨反应的反应速率,又能增大反应物转化率的是
A. 使用催化剂 B. 缩小容积体积 C. 提高反应温度 D. 移走NH3
(3)在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件下不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在下图中补充画出从t2到t4时刻正反应速率随时间的变化曲线

(4)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的pH增大 B.氨水的电离程度减小 C.c(NH4+)减小 D.c(OH-)减小
(5)石蕊(用HZ表示)试液中存在的电离平衡HZ(红色)HZ(蓝色)。通入氨气后石蕊试液呈蓝色,请用平衡移动原理解释
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室从废电路板粉碎金属料(主要含金属Cu,还含少量Zn、Fe、Pb等金属)中回收铜,其实验流程如下:

已知:一定pH范围内, 、
、 等能与氨形成配离子。
等能与氨形成配离子。
(1)“氨浸”在如图所示的装置中进行。
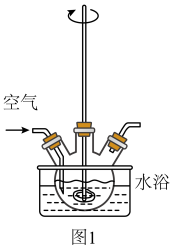
①鼓入空气,金属Cu可被氧化生成 ,其离子方程式为
,其离子方程式为_______ ;
②空气流量过大,会降低Cu元素的浸出率,其原因是_______ 。
③“氨浸”时向氨水中加入一定量 固体,有利于
固体,有利于 转化为
转化为 ,其原因是
,其原因是_______ 。
(2)洗涤滤渣所得的滤液与“过滤”所得滤液合并的目的是_______ 。
(3)滤液中主要阳离子为 、
、 ,还含有一定量的
,还含有一定量的 。某有机溶剂HR可高效萃取离解出的
。某有机溶剂HR可高效萃取离解出的 (实现
(实现 与
与 的有效分离),其原理为(org表示有机相):
的有效分离),其原理为(org表示有机相):
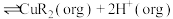 ;再向有机相中加入稀硫酸,反萃取得到
;再向有机相中加入稀硫酸,反萃取得到 溶液。
溶液。

结合图2和图3,补充完整以滤液为原料,制取较纯净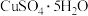 晶体的实验方案:
晶体的实验方案:_______ ,蒸发浓缩,冷却结晶,过滤,洗涤,干燥。(实验中可选用的试剂:有机溶剂HR、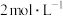 硫酸、
硫酸、 硫酸)。
硫酸)。

已知:一定pH范围内,
 、
、 等能与氨形成配离子。
等能与氨形成配离子。(1)“氨浸”在如图所示的装置中进行。

①鼓入空气,金属Cu可被氧化生成
 ,其离子方程式为
,其离子方程式为②空气流量过大,会降低Cu元素的浸出率,其原因是
③“氨浸”时向氨水中加入一定量
 固体,有利于
固体,有利于 转化为
转化为 ,其原因是
,其原因是(2)洗涤滤渣所得的滤液与“过滤”所得滤液合并的目的是
(3)滤液中主要阳离子为
 、
、 ,还含有一定量的
,还含有一定量的 。某有机溶剂HR可高效萃取离解出的
。某有机溶剂HR可高效萃取离解出的 (实现
(实现 与
与 的有效分离),其原理为(org表示有机相):
的有效分离),其原理为(org表示有机相):
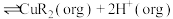 ;再向有机相中加入稀硫酸,反萃取得到
;再向有机相中加入稀硫酸,反萃取得到 溶液。
溶液。
结合图2和图3,补充完整以滤液为原料,制取较纯净
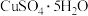 晶体的实验方案:
晶体的实验方案: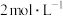 硫酸、
硫酸、 硫酸)。
硫酸)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2的资源化利用是“减少碳排放”背景下的科学研究热点。化学与这些主题密切相关,在其研究与应用中发挥着重要作用。甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应I: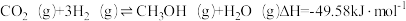
反应Ⅱ: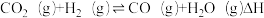
反应Ⅲ:
回答下列问题:
(1)反应Ⅱ的△H=________ ;反应I的活化能E(正)_________ E(逆)(填“>”“=”或“<”)。
(2)恒温恒容密闭容器中,对于反应Ⅱ,下列说法能说明该反应达到化学平衡状态的是___________(填序号)。
(3)250℃时,向2L密闭容器中充入2molH2和1molCO2发生反应I.经过2min达到平衡状态,平衡时测得CO2的转化率为60%。
①该温度下,反应开始至2min时,该反应的平均反应速率v(H2)=___________ 。
②250℃时反应的平衡常数K=___________ 。
③若升高温度,该反应的平衡常数___________ (填“增大”“减小”或“不变”)。
(4)若用NaOH溶液吸收CO2可得Na2CO3或NaHCO3溶液(已知25℃时,Na2CO3溶液Kb=2×10-4)。
①当c( ):c(
):c( )=2:1时,溶液的pH=
)=2:1时,溶液的pH=___________ 。
②在0.1mol·L-1的Na2CO3溶液中,c(OH-)-c(H+)=___________ 。
【用含c( )、2c(
)、2c( )的关系式表示】。
)的关系式表示】。
反应I:
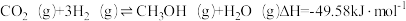
反应Ⅱ:
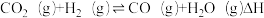
反应Ⅲ:

回答下列问题:
(1)反应Ⅱ的△H=
(2)恒温恒容密闭容器中,对于反应Ⅱ,下列说法能说明该反应达到化学平衡状态的是___________(填序号)。
| A.v(CO2)消耗=v(H2)生成 | B.混合气体的平均相对分子质量不再变化 |
| C.混合气体的密度不再变化 | D.氢气的体积分数保持不变 |
①该温度下,反应开始至2min时,该反应的平均反应速率v(H2)=
②250℃时反应的平衡常数K=
③若升高温度,该反应的平衡常数
(4)若用NaOH溶液吸收CO2可得Na2CO3或NaHCO3溶液(已知25℃时,Na2CO3溶液Kb=2×10-4)。
①当c(
 ):c(
):c( )=2:1时,溶液的pH=
)=2:1时,溶液的pH=②在0.1mol·L-1的Na2CO3溶液中,c(OH-)-c(H+)=
【用含c(
 )、2c(
)、2c( )的关系式表示】。
)的关系式表示】。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.0kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) △H =-129.0kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为______________ 。
(2)将1.0molCH4和2.0molH2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如下图。
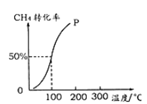
假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率为_______ 。
(3)在压强为0.1MPa、温度为300℃条件下,将amolCO与3amol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的 ,其他条件不变,对平衡体系产生的影响是
,其他条件不变,对平衡体系产生的影响是__________ (填字母序号)。
A.c(H2)减少 B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡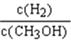 减小 E.平衡常数K增大
减小 E.平衡常数K增大
(4)1mol甲醇完全燃烧产生气体通入1L1.5mol/L的NaOH溶液反应,反应后的溶液中各离子浓度大小关系为____________________ 。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.0kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) △H =-129.0kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为
(2)将1.0molCH4和2.0molH2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如下图。

假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率为
(3)在压强为0.1MPa、温度为300℃条件下,将amolCO与3amol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的
 ,其他条件不变,对平衡体系产生的影响是
,其他条件不变,对平衡体系产生的影响是A.c(H2)减少 B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡
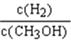 减小 E.平衡常数K增大
减小 E.平衡常数K增大(4)1mol甲醇完全燃烧产生气体通入1L1.5mol/L的NaOH溶液反应,反应后的溶液中各离子浓度大小关系为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某电镀废水中的铬元素以 和
和 的形式存在,其总铬含量的测定方法如下。
的形式存在,其总铬含量的测定方法如下。
步骤一:取 废水,加热浓缩成
废水,加热浓缩成 溶液,然后加入
溶液,然后加入 溶液将
溶液将 转化为
转化为 ;
;
步骤二:加入稍过量的 ,使
,使 在碱性条件下转化成
在碱性条件下转化成 ;
;
步骤三:加入硫酸酸化并煮沸后,加入足量的碘化钾将六价铬还原为 ,同时生成单质
,同时生成单质 ;
;
步骤四:加入指示剂用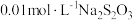 溶液滴定,滴定过程中消耗
溶液滴定,滴定过程中消耗 溶液
溶液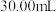 。
。
已知: ,请回答下列问题:
,请回答下列问题:
(1)“步骤三”中加硫酸酸化时存在反应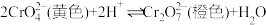 ,则该反应平衡常数的表达式为
,则该反应平衡常数的表达式为
_______ 。升高溶液的温度会导致溶液黄色加深,则该反应的
_______ 0(填“>”或“<”)。
(2)若“步骤三”省略加热煮沸操作会导致废水中铬元素含量的测量结果_______ (填“偏高”、“偏低”或“无影响”)。
(3)“步骤四”中加入的指示剂为_______ ,盛装 溶液的滴定管,滴定前排气泡时,应选择如图中的
溶液的滴定管,滴定前排气泡时,应选择如图中的_______ (填选项字母);滴定终点时的现象为_______ 。
a. b.
b.  c.
c.  d.
d.
(4)硫代硫酸钠晶体( )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分 ,含少量
,含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:

 溶液中
溶液中
_______  (填“>”、“<”或“=”),“反应”过程中体系
(填“>”、“<”或“=”),“反应”过程中体系 过小产品产率降低的原因是
过小产品产率降低的原因是_______ (用离子方程式表示),提纯 时,应用
时,应用_______ 洗涤。
 和
和 的形式存在,其总铬含量的测定方法如下。
的形式存在,其总铬含量的测定方法如下。步骤一:取
 废水,加热浓缩成
废水,加热浓缩成 溶液,然后加入
溶液,然后加入 溶液将
溶液将 转化为
转化为 ;
;步骤二:加入稍过量的
 ,使
,使 在碱性条件下转化成
在碱性条件下转化成 ;
;步骤三:加入硫酸酸化并煮沸后,加入足量的碘化钾将六价铬还原为
 ,同时生成单质
,同时生成单质 ;
;步骤四:加入指示剂用
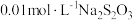 溶液滴定,滴定过程中消耗
溶液滴定,滴定过程中消耗 溶液
溶液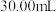 。
。已知:
 ,请回答下列问题:
,请回答下列问题:(1)“步骤三”中加硫酸酸化时存在反应
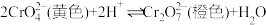 ,则该反应平衡常数的表达式为
,则该反应平衡常数的表达式为

(2)若“步骤三”省略加热煮沸操作会导致废水中铬元素含量的测量结果
(3)“步骤四”中加入的指示剂为
 溶液的滴定管,滴定前排气泡时,应选择如图中的
溶液的滴定管,滴定前排气泡时,应选择如图中的a.
 b.
b.  c.
c.  d.
d.
(4)硫代硫酸钠晶体(
 )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分 ,含少量
,含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:
 溶液中
溶液中
 (填“>”、“<”或“=”),“反应”过程中体系
(填“>”、“<”或“=”),“反应”过程中体系 过小产品产率降低的原因是
过小产品产率降低的原因是 时,应用
时,应用
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】氨是重要的工业原料,在农业、医药,国防和化工等领域有重要应用。回答下列问题:
(1)①常温下, 氨水的pH约为10,则氨水的电离常数
氨水的pH约为10,则氨水的电离常数 约为
约为_______ 。
②常温下,将 盐酸与
盐酸与 氨水等体积混合,若混合溶液
氨水等体积混合,若混合溶液 ,则a
,则a_______ b(填“>”“<”或“=”),若常温下等物质的量浓度的氨水与盐酸等体积混合,所得溶液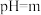 ,则
,则
_______ (用含m的代数式表示)。
(2)常温常压下,将 缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入
缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入 ,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发)。
,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发)。
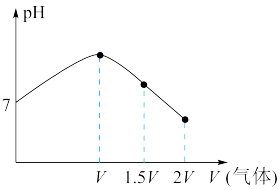
①通入气体体积从0到V的过程中,溶液中
_______ (填“增大”“减小”或“不变”)。
②由图可知 溶液显
溶液显_______ 性(填“酸”“中”或“碱”),原因是_______ 。
(3)若液氨中也存在类似水的电离(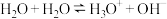 ),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。则碳酸钠的液氨溶液中各离子浓度的大小关系为
),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。则碳酸钠的液氨溶液中各离子浓度的大小关系为_______ 。
(1)①常温下,
 氨水的pH约为10,则氨水的电离常数
氨水的pH约为10,则氨水的电离常数 约为
约为②常温下,将
 盐酸与
盐酸与 氨水等体积混合,若混合溶液
氨水等体积混合,若混合溶液 ,则a
,则a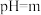 ,则
,则
(2)常温常压下,将
 缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入
缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入 ,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发)。
,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发)。
①通入气体体积从0到V的过程中,溶液中

②由图可知
 溶液显
溶液显(3)若液氨中也存在类似水的电离(
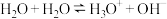 ),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。则碳酸钠的液氨溶液中各离子浓度的大小关系为
),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。则碳酸钠的液氨溶液中各离子浓度的大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.以下是生产、生活中常见的物质。按要求回答下列问题。
①冰醋酸;②Na2CO3;③NaOH;④盐酸;⑤H2C2O4;⑥熔融NaHSO4;⑦石墨;⑧酒精;⑨NH3;⑩BaCO3。
(1)属于强电解质的有_____ ,属于非电解质的有_____ 。(用序号填空)
(2)写出⑤溶液的电离方程式:_____ 。
(3)常温下,pH=2的①溶液和pH=2的④溶液,加水稀释100倍,pH较大的是_____ 。(用序号填空)
(4)等体积的0.1 mol/L①溶液与0.1 mol/L④溶液分别与等浓度的氢氧化钠反应至中性,消耗的NaOH溶液的体积依次为V1和V2,则V1_____ V2(填“>”、“<”或者“=”)。
Ⅱ.已知,常温下几种酸的电离平衡常数如表:
(5)常温下,0.1 mol/L的HCN溶液中,c(H+)约为_____ 。
(6)在NaCN和NaHCO3浓度均为0.1 mol/L的混合溶液中各离子浓度由大到小的顺序为:_____ 。
(7)根据电离平衡常数判断,以下反应不能自发进行的是_____ 。
(8)c( )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,溶质浓度最大的是
)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,溶质浓度最大的是_____ ;室温时,将x mLpH=a的KOH溶液与y mLpH=b的HCOOH溶液充分反应,若x=y且a+b=14,则反应后溶液pH_____ 7(填“>”、“<”或者“=”)。
①冰醋酸;②Na2CO3;③NaOH;④盐酸;⑤H2C2O4;⑥熔融NaHSO4;⑦石墨;⑧酒精;⑨NH3;⑩BaCO3。
(1)属于强电解质的有
(2)写出⑤溶液的电离方程式:
(3)常温下,pH=2的①溶液和pH=2的④溶液,加水稀释100倍,pH较大的是
(4)等体积的0.1 mol/L①溶液与0.1 mol/L④溶液分别与等浓度的氢氧化钠反应至中性,消耗的NaOH溶液的体积依次为V1和V2,则V1
Ⅱ.已知,常温下几种酸的电离平衡常数如表:
| 化学式 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
(6)在NaCN和NaHCO3浓度均为0.1 mol/L的混合溶液中各离子浓度由大到小的顺序为:
(7)根据电离平衡常数判断,以下反应不能自发进行的是
| A.HCOOH+NaCN=HCOONa+HCN | B.NaHCO3+NaCN=Na2CO3+HCN |
| C.NaCN+H2O+CO2=HCN+NaHCO3 | D.HCOOH+CO =HCOO-+ =HCOO-+ |
 )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,溶质浓度最大的是
)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,溶质浓度最大的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】NH4Al(SO4)2常作食品加工中的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是____ (用离子方程式说明)。
(2)相同条件下,0.1mol•L-1NH4Al(SO4)2溶液中的c(NH )
)____ (填“等于”“大于”或“小于”)0.1mol•L-1NH4HSO4溶液中的c(NH )。
)。
(3)几种均为0.1mol•L-1的电解质溶液的pH随温度变化的曲线如图所示。其中符合0.1mol•L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是____ (填罗马数字),导致NH4Al(SO4)2溶液的pH随温度变化的原因是____ 。

(4)室温时,向100mL0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。

①试分析图中a、b、c、d四个点,水的电离程度最大的是____ 点。
②在b点,溶液中各离子浓度由大到小的排列顺序是____ 。
③由b到c发生反应的离子方程式为____ 。
(1)NH4Al(SO4)2可作净水剂,其原理是
(2)相同条件下,0.1mol•L-1NH4Al(SO4)2溶液中的c(NH
 )
) )。
)。(3)几种均为0.1mol•L-1的电解质溶液的pH随温度变化的曲线如图所示。其中符合0.1mol•L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是

(4)室温时,向100mL0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。

①试分析图中a、b、c、d四个点,水的电离程度最大的是
②在b点,溶液中各离子浓度由大到小的排列顺序是
③由b到c发生反应的离子方程式为
您最近一年使用:0次



