第VA族元素氮、磷、砷的化合物用途广泛。回答下列问题:
(1)基态磷原子的电子排布式为_____ ,基态砷原子核外有______ 个未成对电子。
(2)配离子[Cr(NH3)3(H2O)2Cl]2+中,提供孤电子对的原子有______ ,中心离子的配位数为___________ 。
(3) 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为____ ,其立体构型名称为_____ ,与其互为等电子体的分子为______ (写出一种即可)。
(4)无机含氧酸分子中含一个非羟基氧是中强酸,如H3PO4为中强酸,其结构简式为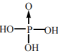 ;则同为中强酸的H3PO2的结构简式为
;则同为中强酸的H3PO2的结构简式为___________ 。
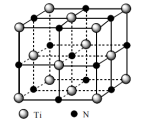
(5)某种由N与Ti形成的化合物,其晶胞结构如下图。阿伏加德罗常数的值为NA,晶胞中Ti原子与N原子的最近距离为anm,晶胞的密度为___________ g/cm3(写出表达式即可)。
(1)基态磷原子的电子排布式为
(2)配离子[Cr(NH3)3(H2O)2Cl]2+中,提供孤电子对的原子有
(3)
 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为(4)无机含氧酸分子中含一个非羟基氧是中强酸,如H3PO4为中强酸,其结构简式为
 ;则同为中强酸的H3PO2的结构简式为
;则同为中强酸的H3PO2的结构简式为(5)某种由N与Ti形成的化合物,其晶胞结构如下图。阿伏加德罗常数的值为NA,晶胞中Ti原子与N原子的最近距离为anm,晶胞的密度为

更新时间:2022/01/27 15:46:09
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】ZnGeP2和KTiOPO4都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:
(1)基态氧原子核外电子有___________ 种不同的空间运动状态;基态Ti原子的价电子排布式为___________ 。
(2)H2O、KH熔点由高到低的顺序为___________ ,原因是___________ 。
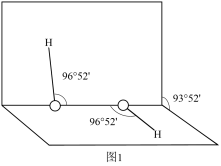
(3)H2O可与H+结合生成H3O+,水中H-O-H的键角比H3O+中的___________ (填“大”或“小”)。H2O2是常用的氧化剂,其分子结构如图1所示。H2O2能与水混溶,却不溶于CCl4的原因是___________ 。
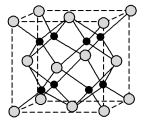
(4)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为___________ ,该晶胞的密度为ρg/cm3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为___________ cm(用含ρ、NA的代数式表示)。
(1)基态氧原子核外电子有
(2)H2O、KH熔点由高到低的顺序为
(3)H2O可与H+结合生成H3O+,水中H-O-H的键角比H3O+中的

(4)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】我国科学家研发的全球首套千吨级太阳能燃料合成项目,为实现“碳中和”目标作出了重大贡献。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)钙钛矿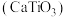 型化合物是一类可用于生产太阳能电池的功能材料。
型化合物是一类可用于生产太阳能电池的功能材料。
①钛在元素周期表中的位置是_____ ,基态钛原子核外有_____ 种空间运动状态不同的电子,基态 中电子占据最高能层的电子排布式为
中电子占据最高能层的电子排布式为_____ 。
② 的前三级电离能数据分别为
的前三级电离能数据分别为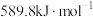 、
、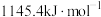 、
、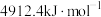 ,第三电离能增大较多的原因是
,第三电离能增大较多的原因是_____ 。
(2) 与
与 同族,
同族, 原子之间可以形成双键、三键,但
原子之间可以形成双键、三键,但 原子之间难以形成双键或三键,从原子结构角度分析,原因是
原子之间难以形成双键或三键,从原子结构角度分析,原因是_____ 。
(3)碳可形成 、
、 、
、 等多种无机化合物。
等多种无机化合物。
①在反应 转化成
转化成 的过程中,下列说法错误的是
的过程中,下列说法错误的是_____ (填字母)。
A.每个分子中孤电子对总数增多
B.分子的极性不变
C.原子间成键方式不完全相同
D.分子的熔沸点变大
②干冰和冰是两种常见的分子晶体,晶体中的空间利用率:干冰_____ 冰(填“>”“<”或“=”)。
③ 的空间结构为
的空间结构为_____ 。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构和 轴方向的投影图如图所示。
轴方向的投影图如图所示。 ,
, 解离为原子,
解离为原子, 原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱心和面心,则形成的储氢化合物的化学式为
原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱心和面心,则形成的储氢化合物的化学式为_____ 。
②若阿伏加德罗常数的值为 ,则镧镍合金的晶体密度
,则镧镍合金的晶体密度
_____  (用含a、c、
(用含a、c、 的代数式表示,列出计算式即可)。
的代数式表示,列出计算式即可)。
(1)钙钛矿
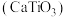 型化合物是一类可用于生产太阳能电池的功能材料。
型化合物是一类可用于生产太阳能电池的功能材料。①钛在元素周期表中的位置是
 中电子占据最高能层的电子排布式为
中电子占据最高能层的电子排布式为②
 的前三级电离能数据分别为
的前三级电离能数据分别为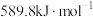 、
、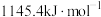 、
、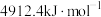 ,第三电离能增大较多的原因是
,第三电离能增大较多的原因是(2)
 与
与 同族,
同族, 原子之间可以形成双键、三键,但
原子之间可以形成双键、三键,但 原子之间难以形成双键或三键,从原子结构角度分析,原因是
原子之间难以形成双键或三键,从原子结构角度分析,原因是(3)碳可形成
 、
、 、
、 等多种无机化合物。
等多种无机化合物。①在反应
 转化成
转化成 的过程中,下列说法错误的是
的过程中,下列说法错误的是A.每个分子中孤电子对总数增多
B.分子的极性不变
C.原子间成键方式不完全相同
D.分子的熔沸点变大
②干冰和冰是两种常见的分子晶体,晶体中的空间利用率:干冰
③
 的空间结构为
的空间结构为(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构和
 轴方向的投影图如图所示。
轴方向的投影图如图所示。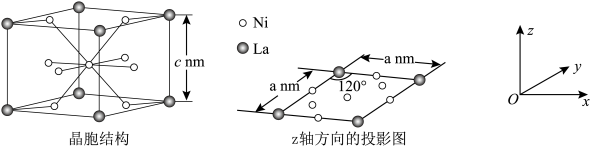
 ,
, 解离为原子,
解离为原子, 原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱心和面心,则形成的储氢化合物的化学式为
原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱心和面心,则形成的储氢化合物的化学式为②若阿伏加德罗常数的值为
 ,则镧镍合金的晶体密度
,则镧镍合金的晶体密度
 (用含a、c、
(用含a、c、 的代数式表示,列出计算式即可)。
的代数式表示,列出计算式即可)。
您最近一年使用:0次
【推荐3】某课题组研究CO2加氢制甲醇。涉及的主要反应有:
反应I:
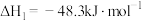
反应Ⅱ: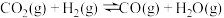
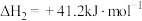
反应Ⅲ:
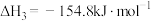
反应Ⅳ:
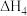
回答下列有关问题:
(1)反应Ⅳ的
___________ 。
(2)下列有关说法正确的是___________。
(3)研究发现:在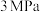 条件下,当起始
条件下,当起始 ,平衡时,
,平衡时, 的转化率、含碳产物的选择性(转化的
的转化率、含碳产物的选择性(转化的 中生成
中生成 、
、 或
或 的百分比,如甲醇的选择性
的百分比,如甲醇的选择性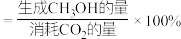 )与温度关系如图所示,回答下列问题。
)与温度关系如图所示,回答下列问题。
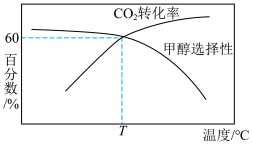
①随着温度升高,甲醇选择性降低而 的转化率却升高的原因可能是
的转化率却升高的原因可能是___________ 。
②在T温度下,若 的选择性为
的选择性为 ,计算此温度下反应Ⅱ的平衡常数K=
,计算此温度下反应Ⅱ的平衡常数K=___________ (写出计算过程)。
(4)一种在铜基催化剂上 加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用“*”标注。
加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用“*”标注。
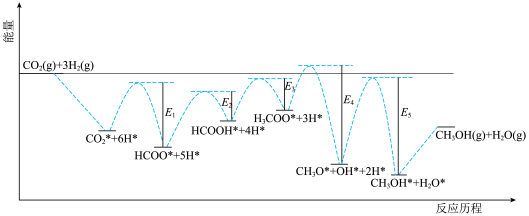
①基态铜原子的价电子排布式为___________ 。
②决速步的反应方程式为___________ 。
(5)写出甲醇在生产或生活中的一种应用___________ 。
反应I:

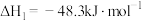
反应Ⅱ:
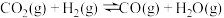
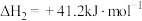
反应Ⅲ:

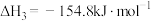
反应Ⅳ:

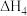
回答下列有关问题:
(1)反应Ⅳ的

(2)下列有关说法正确的是___________。
A.增压时, 的物质的量分数一定增大 的物质的量分数一定增大 |
| B.当甲醇的分压不再改变时,体系达到平衡 |
C.在恒容密闭容器中充入 ,反应Ⅲ速率不变 ,反应Ⅲ速率不变 |
| D.升温时,反应Ⅱ逆反应速率加快的程度大于正反应速率 |
(3)研究发现:在
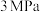 条件下,当起始
条件下,当起始 ,平衡时,
,平衡时, 的转化率、含碳产物的选择性(转化的
的转化率、含碳产物的选择性(转化的 中生成
中生成 、
、 或
或 的百分比,如甲醇的选择性
的百分比,如甲醇的选择性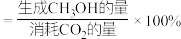 )与温度关系如图所示,回答下列问题。
)与温度关系如图所示,回答下列问题。
①随着温度升高,甲醇选择性降低而
 的转化率却升高的原因可能是
的转化率却升高的原因可能是②在T温度下,若
 的选择性为
的选择性为 ,计算此温度下反应Ⅱ的平衡常数K=
,计算此温度下反应Ⅱ的平衡常数K=(4)一种在铜基催化剂上
 加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用“*”标注。
加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用“*”标注。
①基态铜原子的价电子排布式为
②决速步的反应方程式为
(5)写出甲醇在生产或生活中的一种应用
您最近一年使用:0次
【推荐1】卤素及其化合物广泛存在于自然界中。回答下列问题:
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为______________ ,其三种元素的电负性由小到大的顺序为______________ 。与COCl2互为等电子体的分子和离子(各写一种)__________ 。
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?____________________________ 。
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是_____________ 。
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为___________ ,某同学将基态铜原子价电子错误的写为3d94s2,违背了核外电子排布规律中的______ 。
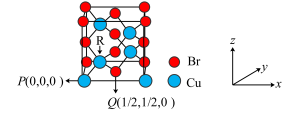
(5)下列关于上述铜的溴化物晶胞结构说法正确的是_________ (选填字母序号)。
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为______ g/cm3。(列出计算式即可)
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为

(5)下列关于上述铜的溴化物晶胞结构说法正确的是
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U的氧化物是第三周期元素形成的常见两性氧化物;W的内层电子全充满,最外层只有1个电子。请回答下列问题:
(1)X、Y、Z的电负性从大到小的顺序是_______ (用元素符号表示,下同)。三种元素的第一电离能由大到小的顺序为__________ 。
(2)写出Y的价电子排布式____ ,W同周期的元素中,与W原子最外层电子数相等的元素还有________ 。
(3)根据等电子体原理,可知化合物XZ的结构式是________ , YZ2-的VSEPR模型是________ 。
(4)X、Y、Z的简单氢化物的键角从大到小的顺序是________ (用化学式表示),原因是_____________ 。
(5)Y的氢化物易液化的原因是___________ 。
(6)XZ32-的立体构型是________ ,其中X原子的杂化轨道类型是________ ,互为等电子体的离子________ 。
(7)用氢键表示式写出Z的氢化物中存在的氢键________ 。
(1)X、Y、Z的电负性从大到小的顺序是
(2)写出Y的价电子排布式
(3)根据等电子体原理,可知化合物XZ的结构式是
(4)X、Y、Z的简单氢化物的键角从大到小的顺序是
(5)Y的氢化物易液化的原因是
(6)XZ32-的立体构型是
(7)用氢键表示式写出Z的氢化物中存在的氢键
您最近一年使用:0次
【推荐3】X、Y、Z、W、R、M 六种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,相关信息如下:
请回答下列问题(答题时,X、Y、Z、W、R、M用所对应的元素符号表示):
(1)X的单质与Z的单质反应的产物为_____________ 。(填化学式)。
(2)Z、W相比,第一电离能较大的是_____________ ,M2+的核外电子排布式为_____________ 。
(3)M2Z的熔点比M2W 的_____________ (填“高”或“低”),请解释原因______________________ 。
(4)Y和Z形成的化合物YZ2的VSEPR模型为__________ ,其中Y原子 的杂化轨道类型为____________ ; N3-和YZ2互为等电子体,则N3-的结构式为_____________ 。
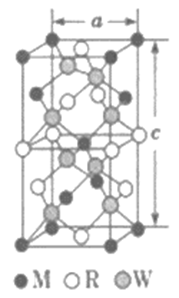
(5)MRW2的晶胞如图所示,晶胞参数a=0.524 nm,c=1.032 nm; MRW2的晶胞中每个M 原子与_________ 个W 原子相连,晶体密度ρ=________ g·cm-3 (只要求列算式,不必计算出数值,NA=6.02×1023mol-1)。
| 元素 | 相关信息 |
| X | 其单质为固体,常作电极材料 |
| Y | 原子核外有6种不同运动状态的电子 |
| Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
| W | 主族元素,与Z原子的价电子数相同 |
| R | 价层电子排布为3d64s2 |
| M | ⅠB族,其单质常用作导线 |
请回答下列问题(答题时,X、Y、Z、W、R、M用所对应的元素符号表示):
(1)X的单质与Z的单质反应的产物为
(2)Z、W相比,第一电离能较大的是
(3)M2Z的熔点比M2W 的
(4)Y和Z形成的化合物YZ2的VSEPR模型为
(5)MRW2的晶胞如图所示,晶胞参数a=0.524 nm,c=1.032 nm; MRW2的晶胞中每个M 原子与

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁及其化合物广泛地应用到各个领域。回答下列问题:
(1)铁元素位于元素周期表的___________ 区。
(2)我国菱铁矿 储量较为丰富,
储量较为丰富, 中
中 的空间结构为
的空间结构为___________ 。
(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是___________ 。 溶于汽油、苯、丙酮等有机溶剂。CO与Fe之间从电子对给予来看形成
溶于汽油、苯、丙酮等有机溶剂。CO与Fe之间从电子对给予来看形成___________ 键。
(5)以 、
、 合成
合成 ,Fe是常用的催化剂。实际生产中采用铁的氧化物
,Fe是常用的催化剂。实际生产中采用铁的氧化物 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为立方体)结构示意如下,两种晶胞所含铁原子个数比为
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为立方体)结构示意如下,两种晶胞所含铁原子个数比为___________ 。___________ 。若该晶体的密度是d g⋅cm ,则两个最近的Fe原子间的距离为
,则两个最近的Fe原子间的距离为___________ nm(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)铁元素位于元素周期表的
(2)我国菱铁矿
 储量较为丰富,
储量较为丰富, 中
中 的空间结构为
的空间结构为(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是
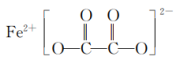
 溶于汽油、苯、丙酮等有机溶剂。CO与Fe之间从电子对给予来看形成
溶于汽油、苯、丙酮等有机溶剂。CO与Fe之间从电子对给予来看形成(5)以
 、
、 合成
合成 ,Fe是常用的催化剂。实际生产中采用铁的氧化物
,Fe是常用的催化剂。实际生产中采用铁的氧化物 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为立方体)结构示意如下,两种晶胞所含铁原子个数比为
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为立方体)结构示意如下,两种晶胞所含铁原子个数比为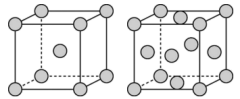
 ,则两个最近的Fe原子间的距离为
,则两个最近的Fe原子间的距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。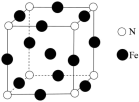
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Ga 基态原子核外电子排布式为_______ ,As 基态原子核外有_______ 个未成对电子。
(2)Ga、As、Se 的电负性由大到小的顺序是__________ 。
(3)GaCl3和AsF3的立体构型分别是____________ ,__________ 。
(4)比较下列镓的卤化物的熔点和沸点,分析其变化的原因:____________ 。
GaF3的熔点超过1000 ℃,可能的原因是_____ 。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。[B(OH)4]-中B原子的杂化类型为______ 。
(6)若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅,若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是__________ (用化学式表示);
(1)Ga 基态原子核外电子排布式为
(2)Ga、As、Se 的电负性由大到小的顺序是
(3)GaCl3和AsF3的立体构型分别是
(4)比较下列镓的卤化物的熔点和沸点,分析其变化的原因:
| 镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
| 熔点/℃ | 77.75 | 122.3 | 211.5 |
| 沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000 ℃,可能的原因是
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。[B(OH)4]-中B原子的杂化类型为
(6)若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅,若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】五氧化二钒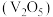 和三氧化钼
和三氧化钼 是两种重要的过渡金属氧化物,通常用作工业催化剂。有企业通过废旧催化剂(主要成分为
是两种重要的过渡金属氧化物,通常用作工业催化剂。有企业通过废旧催化剂(主要成分为 、
、 、
、 ,还有少量的
,还有少量的 、
、 、有机物等)来制备这两种氧化物。工艺流程图如下图:
、有机物等)来制备这两种氧化物。工艺流程图如下图:
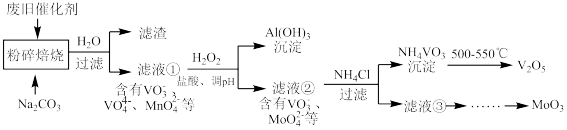
(1)“焙烧”的目的是_______ 。
(2)滤渣的主要成分是_______ (填化学式)。
(3)向滤液①中加 的作用是
的作用是_______ (用离子方程式表示)。
(4)当滤液①pH调控为8时,写出计算过程说明此时铝元素是否沉淀完全_______ 。(已知:
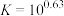 ,离子浓度小于
,离子浓度小于 认为沉淀完全)
认为沉淀完全)
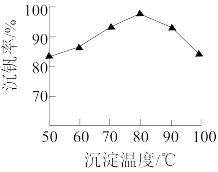
(5) 的沉淀过程中,沉钒率受温度影响,关系如图所示。温度高于80℃沉钒率降低的主要原因是
的沉淀过程中,沉钒率受温度影响,关系如图所示。温度高于80℃沉钒率降低的主要原因是_______ 。 的沉淀分解生成
的沉淀分解生成 的化学方程式是
的化学方程式是_______ 。
(6)仪器分析检测 在水中带有结晶水
在水中带有结晶水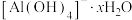 ,
, 与结晶水之间的作用力是_______(填字母)。
与结晶水之间的作用力是_______(填字母)。
(7)Mo原子序数42,气相单分子 空间结构是
空间结构是_______ 。
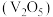 和三氧化钼
和三氧化钼 是两种重要的过渡金属氧化物,通常用作工业催化剂。有企业通过废旧催化剂(主要成分为
是两种重要的过渡金属氧化物,通常用作工业催化剂。有企业通过废旧催化剂(主要成分为 、
、 、
、 ,还有少量的
,还有少量的 、
、 、有机物等)来制备这两种氧化物。工艺流程图如下图:
、有机物等)来制备这两种氧化物。工艺流程图如下图:
(1)“焙烧”的目的是
(2)滤渣的主要成分是
(3)向滤液①中加
 的作用是
的作用是(4)当滤液①pH调控为8时,写出计算过程说明此时铝元素是否沉淀完全

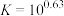 ,离子浓度小于
,离子浓度小于 认为沉淀完全)
认为沉淀完全)(5)
 的沉淀过程中,沉钒率受温度影响,关系如图所示。温度高于80℃沉钒率降低的主要原因是
的沉淀过程中,沉钒率受温度影响,关系如图所示。温度高于80℃沉钒率降低的主要原因是 的沉淀分解生成
的沉淀分解生成 的化学方程式是
的化学方程式是
(6)仪器分析检测
 在水中带有结晶水
在水中带有结晶水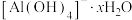 ,
, 与结晶水之间的作用力是_______(填字母)。
与结晶水之间的作用力是_______(填字母)。| A.离子键 | B.配位键 | C.氢键 | D.范德华力 |
 空间结构是
空间结构是
您最近一年使用:0次
【推荐1】随着科学的发展,氟及其化合物的用途日益广泛。
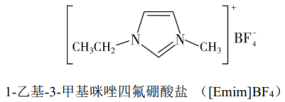
Ⅰ.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。
(1)基态N原子的价层电子轨道表示式为_______ 。
(2)①N、F、P三种元素的电负性由大到小的顺序为_______ 。
②根据VSEPR模型, 的中心原子上的价层电子对数为
的中心原子上的价层电子对数为_______ ,空间结构为_______ 形。
(3) 是制备此离子液体的原料。
是制备此离子液体的原料。
①微粒中F—B—F键角:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
② 可以与NaF反应生成
可以与NaF反应生成 的原因是
的原因是_______ 。
(4)以 和
和 的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为
的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为_______ ,电解质溶液中 向
向_______ (填“阴”或“阳”)极移动。
Ⅱ.NaF等氟化物可以做光导纤维材料,一定条件下,某NaF的晶胞结构示意图如下图所示,晶胞的边长为apm 。
。

(5)与 距离最近且相等的
距离最近且相等的 有
有_______ 个。
(6)已知NaF的摩尔质量是Mg/mol,阿伏伽德罗常数为 。该晶体的密度为
。该晶体的密度为_______  。
。
Ⅰ.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如下图。

(1)基态N原子的价层电子轨道表示式为
(2)①N、F、P三种元素的电负性由大到小的顺序为
②根据VSEPR模型,
 的中心原子上的价层电子对数为
的中心原子上的价层电子对数为(3)
 是制备此离子液体的原料。
是制备此离子液体的原料。①微粒中F—B—F键角:

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②
 可以与NaF反应生成
可以与NaF反应生成 的原因是
的原因是(4)以
 和
和 的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为
的混合体系做电解质溶液,可以实现在不锈钢上镀铜。镀铜时,阳极材料为 向
向Ⅱ.NaF等氟化物可以做光导纤维材料,一定条件下,某NaF的晶胞结构示意图如下图所示,晶胞的边长为apm
 。
。
(5)与
 距离最近且相等的
距离最近且相等的 有
有(6)已知NaF的摩尔质量是Mg/mol,阿伏伽德罗常数为
 。该晶体的密度为
。该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碳单质有广泛的应用,完成下列问题。
(1)碳有很多同素异形体,例如金刚石、石墨和C60,已知金刚石中C-C键的键长为0.154nm,C60中C-C键键长为0.140~0.145nm。C60的熔点_____ 金刚石(填“高于”或“低于”),理由是_____ 。
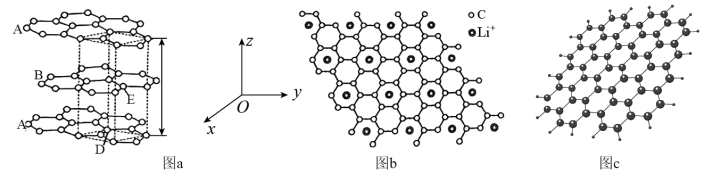
(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,层与层之间靠_____ 维系。图中用虚线标出了石墨的一个六方晶胞。1个六方石墨晶胞中碳原子的个数为_____ ,D处碳原子的分数坐标为(0,0,0),则E处碳原子的分数坐标为_____ (以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标)。
(3)石墨可作锂离子电池的负极材料,锂离子电池充电时,Li+嵌入石墨层间。当嵌入最大量Li+时,晶体部分结构的俯视示意图如图b,此时C与Li+的个数比是_____ 。
(4)石墨烯是一种由单层碳原子构成的二维碳纳米材料,如图c所示。下列有关石墨烯说法正确的是_____。

(1)碳有很多同素异形体,例如金刚石、石墨和C60,已知金刚石中C-C键的键长为0.154nm,C60中C-C键键长为0.140~0.145nm。C60的熔点
(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,层与层之间靠
(3)石墨可作锂离子电池的负极材料,锂离子电池充电时,Li+嵌入石墨层间。当嵌入最大量Li+时,晶体部分结构的俯视示意图如图b,此时C与Li+的个数比是
(4)石墨烯是一种由单层碳原子构成的二维碳纳米材料,如图c所示。下列有关石墨烯说法正确的是_____。
| A.所有碳原子位于同一平面上 | B.石墨烯具有良好的导电性 |
| C.12g石墨烯所含σ键的物质的量为1mol | D.石墨烯属于烯烃类物质 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】请回答下列问题。
(1)基态铁原子的价层电子排布式为_______ 。
(2)元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
① Na的第一电离能小于Li,从原子结构的角度解释其原因_______ 。
② S的第一电离能小于P,解释其原因_______ 。
(3)33As、34Se、35Br三种非金属元素的电负性由大到小的顺序为_______ ;Br可与第三周期Cl元素形成化合物BrCl,其中显正价的元素为_______ ,原因是_______ 。
(4)钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。钛酸钙的晶胞如下图所示,1个晶胞中含有O2-的个数是_______ ,离子半径Ca2+大于Ti4+,理由是_______ 。
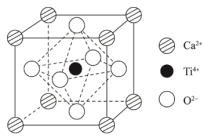
(5)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞的棱长为a pm,则钛酸钙晶体密度ρ=_______ g·cm-3(列出计算式)。
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是_______ (填字母序号)。
a. BaTiO3 b. MgTiO3 c. BaZrO3
(1)基态铁原子的价层电子排布式为
(2)元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
① Na的第一电离能小于Li,从原子结构的角度解释其原因
② S的第一电离能小于P,解释其原因
(3)33As、34Se、35Br三种非金属元素的电负性由大到小的顺序为
(4)钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。钛酸钙的晶胞如下图所示,1个晶胞中含有O2-的个数是

(5)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞的棱长为a pm,则钛酸钙晶体密度ρ=
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是
a. BaTiO3 b. MgTiO3 c. BaZrO3
您最近一年使用:0次



