 CH3OH(g)。
CH3OH(g)。(1)该反应在不同温度下CO的转化率随时间变化如图一所示,则该反应的焓变ΔH
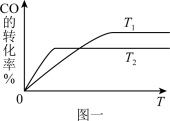
(2)某温度下,在体积为2L的密闭容器中,充入2molCO和4molH2,经测得CO和CH3OH(g)的物质的量随时间的变化如图二所示。则0~10min内v(CH3OH)=
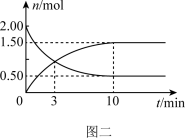
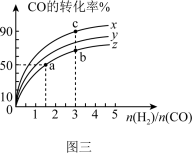
(3)为研究在230℃、250℃和270℃三种温度下合成甲醇的规律,在容积为1L的恒容容器中,测得三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系如图三所示,则曲线z对应的温度是
相似题推荐
(1)对于下列反应:2SO2 + O2
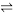 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为(2)已知:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H1;
H2O(g)=H2O(1);△H2;
C2H5OH(g)=C2H5OH(1);△H3
若使23 g C2H5OH(1)完全燃烧生成H2O(1),则放出的热量为

(1)该反应的反应物是
(2)该反应的化学方程式为
(3)达到平衡状态的所需时间是2min,则该2min内A物质的平均反应速率为
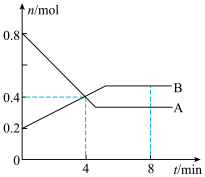
(1)在4min末时,A.B的物质的量浓度c(A)
(2)从反应开始至4min时,A的平均反应速率为
(3)该反应的化学方程式为
 、
、 置于一个容积为5L的密闭容器中发生反应。反应过程中各种物质的物质的量变化如图所示(横纵坐标上的数值为虚线对应):
置于一个容积为5L的密闭容器中发生反应。反应过程中各种物质的物质的量变化如图所示(横纵坐标上的数值为虚线对应):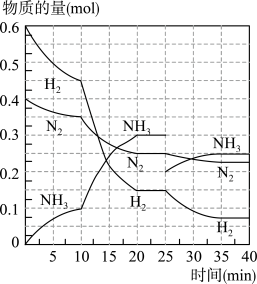
 的对应的时间段为
的对应的时间段为2.10min内以
 表示的平均反应速率为
表示的平均反应速率为3.在反应进行至
 时,推测曲线发生变化的原因可能为
时,推测曲线发生变化的原因可能为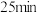 时,推测曲线发生变化的原因可能为
时,推测曲线发生变化的原因可能为4.工业上可采取以下措施以提高原料利用率,且能用勒夏特列原理解释的是 。
| A.加入催化剂 | B.升高温度 |
| C.增大反应容器的压强 | D.设法分离产生的氨 |
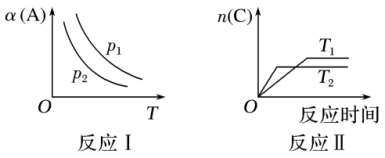
分析图像,回答下列问题:
(1)在反应I中,若p1>p2,则该反应的正反应为
(2)在反应II中,T1
 [Co(H2O)6]2++4Cl- △H<0。现有呈现紫色的氯化钴溶液。
[Co(H2O)6]2++4Cl- △H<0。现有呈现紫色的氯化钴溶液。(1)甲同学向上述溶液中通入HCl,发现溶液变为
(2)乙同学向上述溶液中加水,平衡
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应为
(2)减压时,A 的质量分数
(3)若加入 B(体积不变),则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比[B]/[C]将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(1)如图表示在密闭容器中反应:2SO2(g)+O2(g)
 2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是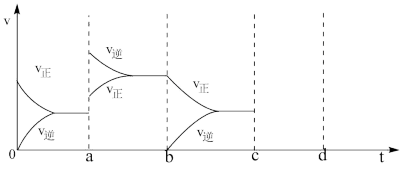
(2)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试填写下列空格:
①SO2的转化率为
②用SO2表示该反应的平均反应速率为
③平衡时体系中SO3的百分含量(体积分数)为
④平衡常数K为
 2NH3(g)
2NH3(g)(1)反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a=
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量为
(3)原混合气体与平衡时混合气体的总物质的量之比,n(始)∶n(平) =
(4)达到平衡时,N2和H2的转化率之比α(N2): α(H2)=
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(6)该反应正反应为
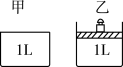
【推荐3】CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH<0。现在体积为1L的恒容密闭容器(如图甲所示)中通入1mol CO和2mol H2,测定不同时间、不同温度(T/℃)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<0。现在体积为1L的恒容密闭容器(如图甲所示)中通入1mol CO和2mol H2,测定不同时间、不同温度(T/℃)下容器中CO的物质的量,如下表:
0min | 10min | 20min | 30min | 40min | |
T1 | 1mol | 0.8mol | 0.62mol | 0.4mol | 0.4mol |
T2 | 1mol | 0.7mol | 0.5mol | a | a |
请回答:
①T1
②若将1mol CO和2mol H2通入原体积为1L的恒压密闭容器(如图乙所示)中,在T2℃下达到平衡,此时反应的平衡常数为
③达到平衡后若再向恒压容器乙中通入1mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量
④达到平衡后若再向恒容容器甲中通入1mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量
⑤在T2温度下,向甲容器中重新加入1mol CO、2mol H2、3mol CH3OH时,υ正



