室温下用 溶液分别滴定20.00mL浓度均为
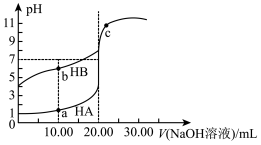
溶液分别滴定20.00mL浓度均为 的HA,HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图所示(溶液体积变化忽略不计)。下列说法不正确的是
的HA,HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图所示(溶液体积变化忽略不计)。下列说法不正确的是
 溶液分别滴定20.00mL浓度均为
溶液分别滴定20.00mL浓度均为 的HA,HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图所示(溶液体积变化忽略不计)。下列说法不正确的是
的HA,HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图所示(溶液体积变化忽略不计)。下列说法不正确的是
| A.导电能力:a点溶液>b点溶液 |
B.b点溶液中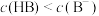 |
C.a点溶液中由水电离出的 约为 约为 |
D.HA对应曲线上c点溶液呈碱性因是 |
2022·天津·一模 查看更多[5]
云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题辽宁省葫芦岛市2022届高三第二次模拟考试化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)天津市市区重点中学2022届高三一模联考化学试题
更新时间:2022-03-05 18:02:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作正确的是
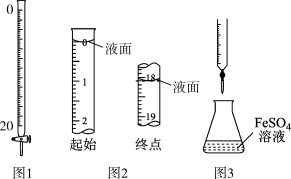

| A.选用图1滴定管量取17.60mLNaCl溶液 |
| B.如图2所示,记录滴定终点读数为19.90mL |
| C.中和滴定时,选用图1滴定管盛装NaOH标准溶液 |
| D.可用图3装置进行KMnO4溶液滴定未知浓度的FeSO4溶液实验 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在t℃时某 的稀溶液中
的稀溶液中 已知
已知 向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示
向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示
混合溶液的部分PH
假设溶液混合前后的体积变化忽略不计,则c的数值为
 的稀溶液中
的稀溶液中 已知
已知 向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示
向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示混合溶液的部分PH
 溶液体积/ml 溶液体积/ml | 盐液的体积/ml | 溶液的PH | |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.0 | 22.00 | 6 |
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】室温下将0.10mol·L-1NaOH溶液滴入20.00mL未知浓度的某一元酸HA溶液中,溶液pH随氢氧化钠溶液体积变化的曲线如图所示(混合过程中溶液体积变化忽略不计)。c点时加入的V(NaOH)=20.00mL,此时HA恰好完全反应。下列说法不正确的是( )
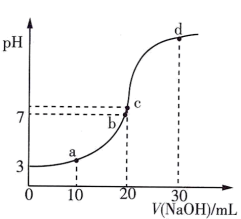

| A.室温下,该酸的电离平衡常数约为10-5 |
| B.b点与c点溶液中n(HA)+n(A-)的值相等 |
| C.a点溶液中存在:c(Na+)-c(H+)=c(HA)-c(OH-) |
| D.d点溶液中存在:c(A-)+3c(HA)=2c(OH-)+2c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时向20.00 mL浓度均为0.01 mol·L-1的HA和HB的混合溶液中逐滴加入0.01 mol·L-1氨水,滴定过程中电导率(导电能力)和pH变化曲线如图所示(已知HA为一元强酸,HB为一元弱酸,其电离平衡常数为Ka)。下列说法正确的是
 pH
pH
 pH
pHA.a点溶液中,c(B-)≈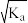 mol·L-1 mol·L-1 |
| B.b点溶液中,溶质的主要成分为NH4B和HA |
C.c点溶液中,c( )+c(NH3·H2O)=2c(B-)+2c(HB) )+c(NH3·H2O)=2c(B-)+2c(HB) |
| D.d点水的电离程度大于c |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】pH=2的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图示,下列说法正确的是

①若a<5,则A、B都是弱酸;
②稀释后[H+]:A>B;
③若a=5,则A是强酸,B是弱酸;
④A、B两种酸溶液的物质的量浓度一定相等。

①若a<5,则A、B都是弱酸;
②稀释后[H+]:A>B;
③若a=5,则A是强酸,B是弱酸;
④A、B两种酸溶液的物质的量浓度一定相等。
| A.①④ | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列各组溶液中的各种溶质的物质的量浓度均为0.1 mol•L-1:①H2S溶液、②KHS溶液、③K2S溶液、④H2S和KHS混合溶液(已知常温下KHS溶液的pH>7)。下列说法正确的是
| A.溶液的pH从大到小的顺序为③>②>①>④ |
| B.在H2S和KHS混合溶液中:c(H2S)+c(HS-)+c(S2-)=c(K+) |
| C.c(H2S)从大到小的顺序为①>④>③>② |
| D.在KHS溶液中:c(H+)+c(K+)=c(HS-)+2c(S2-)+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硒酸(H2SeO4)在水溶液中按下式发生一级和二级电离: ;
; ,
,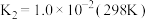 ,室温下,在10mL0.1mol⋅L-1H2SeO4溶液中,滴加0.1mol⋅L-1NaOH溶液。下列说法正确的是
,室温下,在10mL0.1mol⋅L-1H2SeO4溶液中,滴加0.1mol⋅L-1NaOH溶液。下列说法正确的是
 ;
; ,
,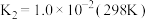 ,室温下,在10mL0.1mol⋅L-1H2SeO4溶液中,滴加0.1mol⋅L-1NaOH溶液。下列说法正确的是
,室温下,在10mL0.1mol⋅L-1H2SeO4溶液中,滴加0.1mol⋅L-1NaOH溶液。下列说法正确的是A. 可经过两步水解得到H2SeO4 可经过两步水解得到H2SeO4 |
B.滴加NaOH溶液10mL时,溶液中离子浓度: |
C.当滴加至中性时,溶液中有 |
D.当用去NaOH溶液体积20mL时,此时溶液中有 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,0.01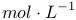 的三种盐溶液
的三种盐溶液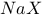 、
、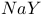 、
、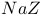 的
的 分别为7、8、9,则下列比较中正确的是
分别为7、8、9,则下列比较中正确的是
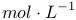 的三种盐溶液
的三种盐溶液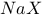 、
、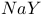 、
、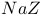 的
的 分别为7、8、9,则下列比较中正确的是
分别为7、8、9,则下列比较中正确的是A. 是弱酸 是弱酸 |
B.离子浓度: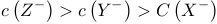 |
| C.电离常数:Ka(HZ)>Ka(HY) |
D.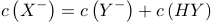  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,分别向20 mL浓度均1.0 mol∙L-1的HA、NaA溶液中逐滴加入浓度均为1.0 mol∙L-1的NaOH、HCl溶液V mL,溶液的pH与lgY[Y= 或
或 ]的关系如图所示。下列说法不正确的是
]的关系如图所示。下列说法不正确的是
 或
或 ]的关系如图所示。下列说法不正确的是
]的关系如图所示。下列说法不正确的是
A.25℃时, 的数量级为 的数量级为 |
B.当 时: 时: |
C.曲线②中的 |
D.当滴入体积 mL时,溶液 mL时,溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知Ksp(CaCO3)=2.8×10﹣9,下列判断正确的是( )
| A.向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32﹣+2H2O⇌H2CO3+2OH﹣ |
| B.常温时,pH = 3的盐酸和pH = 11的氨水等体积混合后所得溶液中,c(H+ )>c(OH—) |
| C.NaHCO3溶液中:c(OH﹣)﹣c(H+)=c(H2CO3)﹣c(CO32﹣) |
| D.2×10﹣4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10﹣5 mol/L |
您最近一年使用:0次

 缓慢通入水中至饱和,再向其中滴加
缓慢通入水中至饱和,再向其中滴加 溶液,溶液
溶液,溶液 的变化如图所示,下列分析正确的是
的变化如图所示,下列分析正确的是






