常温下,0.01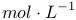 的三种盐溶液
的三种盐溶液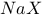 、
、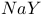 、
、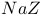 的
的 分别为7、8、9,则下列比较中正确的是
分别为7、8、9,则下列比较中正确的是
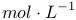 的三种盐溶液
的三种盐溶液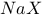 、
、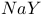 、
、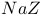 的
的 分别为7、8、9,则下列比较中正确的是
分别为7、8、9,则下列比较中正确的是A. 是弱酸 是弱酸 |
B.离子浓度: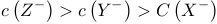 |
| C.电离常数:Ka(HZ)>Ka(HY) |
D.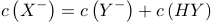  |
更新时间:2018-01-06 11:48:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】25 ℃时,氢离子浓度都为1×10-2 mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入003 g Zn粉,在相同条件下充分反应,下列有关叙述正确的是
| A.稀释2倍后,两溶液的pH:盐酸小于醋酸 |
| B.盐酸和醋酸分别与Zn反应放出的氢气一样多 |
| C.盐酸和醋酸分别与Zn反应的速率一样大 |
| D.稀释2倍前,醋酸溶液中:c(CH3COOH)>c(CH3COO-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下体积相同的溶液:①pH=2的CH3COOH(aq);②0.01mol·L-1的CH3COOH(aq)。下列符合②>①的是
| A.稀释到相同pH所需水的体积 |
| B.与镁条反应生成等量H2所需时间 |
| C.与镁条反应的起始速率 |
| D.与相同浓度NaOH(aq)恰好中和时,消耗NaOH(aq)的体积 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐1】室温下,将1.000mol
 盐酸滴入20.00mL 1.000mol
盐酸滴入20.00mL 1.000mol
 氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是
氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是


 盐酸滴入20.00mL 1.000mol
盐酸滴入20.00mL 1.000mol
 氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是
氨水中,溶液pH和温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是
A.a点由水电离出的 |
B.b点: |
C.c点: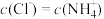 |
D.d点后,容易温度略下降的主要原因是 电离吸热 电离吸热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,将1.0L0.2mol/LHA溶液与0.1molNaOH固体混合充分反应后,再向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液 随通入或加入物质的物质的量的变化如图所示:
随通入或加入物质的物质的量的变化如图所示:

下列说法错误的是
 随通入或加入物质的物质的量的变化如图所示:
随通入或加入物质的物质的量的变化如图所示:
下列说法错误的是
| A.HA为一元弱酸 |
B.b点: |
C.a点、b点水的电离程度: |
D. 过程中, 过程中, 逐渐变大 逐渐变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】298K时,将V0mL0.1mol•L-1的NaX、NaY溶液分别加水稀释至VmL的过程中,溶液的pH与lg 的变化关系如图。下列说法不正确的是
的变化关系如图。下列说法不正确的是

 的变化关系如图。下列说法不正确的是
的变化关系如图。下列说法不正确的是
| A.酸HY的电离常数约为10-5mol•L-1 |
| B.水的电离程度M点大于N点 |
| C.等浓度的NaX溶液和NaY溶液中阴离子浓度后者大 |
| D.M点溶液中c(OH-)>c(H+)+c(X-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,下列溶液中粒子浓度关系不正确的是
A.KAl(SO4)2溶液: c ( )>c (K+)>c (Al3+)>c(H+)>c(OH-) )>c (K+)>c (Al3+)>c(H+)>c(OH-) |
B.用酚酞作指示剂,向氨水中滴入标准盐酸至滴定终点:c( )> c(Cl-) )> c(Cl-) |
C.NH4Cl与Ba(NO3)2的混合溶液:c(Cl-)+2( )= c( )= c( )+ c(NH3⋅H2O)+ c(Ba2+) )+ c(NH3⋅H2O)+ c(Ba2+) |
| D.饱和氯水中:c(H+)= c(ClO-) + c(OH-) +c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下有以下四种溶液,下列说法错误的是
| ① | ② | ③ | ④ | |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | NaOH溶液 | 醋酸溶液 | 盐酸 |
| A.①与②等体积混合后溶液的pH不变 |
| B.分别加水稀释10倍,四种溶液的pH:①>②>④>③ |
C.①与④等体积混合后,所得溶液中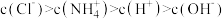 |
D.若 ④与 ④与 ②混合后所得溶液的pH=3,则 ②混合后所得溶液的pH=3,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知联氨(N2H4)为二元弱碱,常温下将盐酸滴加到联氨(N2H4)的水溶液中,混合溶液中微粒的物质的量分数δ(X)随-lgc(OH-)变化的关系如图所示。下列叙述错误的是
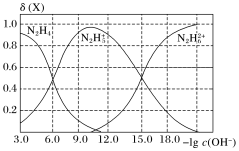

A.反应  +N2H4 +N2H4 2 2 的pK=-0.9(已知pK=-lg K) 的pK=-0.9(已知pK=-lg K) |
B.N2H5Cl溶液中存在:c(Cl-)+c(OH-)=c( )+2c( )+2c( )+c(H+) )+c(H+) |
| C.N2H5Cl溶液中:c(H+)>c(OH-) |
| D.Kb1(N2H4)=10-6.0 |
您最近一年使用:0次

 和AlO
和AlO 在溶液中因为互相抑制水解而大量共存
在溶液中因为互相抑制水解而大量共存 )大小顺序:NH4HSO4>NH4Cl>CH3COONH4
)大小顺序:NH4HSO4>NH4Cl>CH3COONH4

