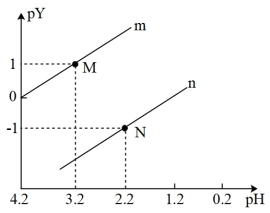
25℃时,向一定浓度的Na2C2O4溶液中滴入稀硫酸,粒子浓度与混合溶液pH的变化关系如图所示。pY=-lgY,Y表示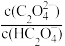 或
或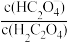 。下列叙述错误的是
。下列叙述错误的是
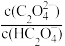 或
或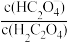 。下列叙述错误的是
。下列叙述错误的是
| A.H2C2O4的第二步电离常数的数量级为10-5 |
B.pH=4.2时,c(C2O )+2c(H2C2O4)<2c(SO )+2c(H2C2O4)<2c(SO ) ) |
C.pH=2.7时,c(HC2O )> c(C2O )> c(C2O )> c(H2C2O4) )> c(H2C2O4) |
D.滴加稀硫酸过程中,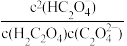 保持不变 保持不变 |
2022·安徽·二模 查看更多[6]
安徽省鼎尖联盟2022届高三下学期4月联考(二模)理综化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)
更新时间:2022-04-16 22:36:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列各组数据中比值为2:1的是( )
| A.K2SO3溶液中c(K+)与c(SO32-)之比 |
| B.0.2mol·L-1的CH3COOH溶液与0.1mol·L-1的盐酸中c(H+)之比 |
| C.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比 |
| D.pH=12的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验事实不能证明醋酸是弱酸的是( )
| A.常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
| B.常温下,测得0.1 mol/L醋酸溶液的pH=4 |
| C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4 |
| D.常温下,测得醋酸钠溶液的pH>7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,向10 mL 0.01 mol·L-1的NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图甲所示,溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如图乙所示。
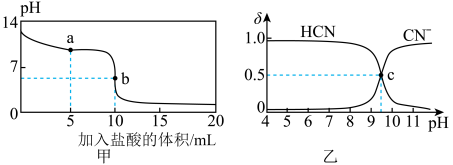
| A.图甲中a点对应的溶液中:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) |
| B.图甲中b点对应的溶液中:c(Na+)+c(H+)=0.01mol·L-1+c(OH-)+c(CN-) |
| C.25℃时 ,HCN的电离常数的数量级为10-9 |
| D.图乙中pH=7的溶液中:c(Cl-)=c(HCN) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后的溶液中c(NH4+)=c(Cl-)。则反应后溶液显
| A.酸性 | B.碱性 | C.中性 | D.无法判断 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用 盐酸滴定
盐酸滴定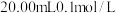 弱碱
弱碱 溶液,溶液中
溶液,溶液中 、分布系数
、分布系数 随滴加盐酸体积
随滴加盐酸体积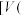 盐酸
盐酸 的变化关系如图所示[比如
的变化关系如图所示[比如 的分布系数:
的分布系数: ],下列说法正确的是
],下列说法正确的是
 盐酸滴定
盐酸滴定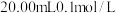 弱碱
弱碱 溶液,溶液中
溶液,溶液中 、分布系数
、分布系数 随滴加盐酸体积
随滴加盐酸体积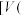 盐酸
盐酸 的变化关系如图所示[比如
的变化关系如图所示[比如 的分布系数:
的分布系数: ],下列说法正确的是
],下列说法正确的是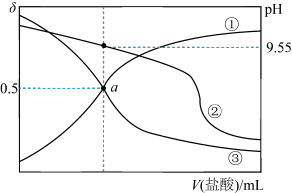
A.曲线①代表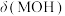 ,曲线②代表 ,曲线②代表 |
B. 的电离平衡常数是 的电离平衡常数是 |
C. 水溶液中: 水溶液中: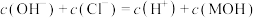 |
D.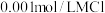 水溶液加水稀释, 水溶液加水稀释, 降低 降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c( )的比值保持增大
)的比值保持增大
②浓度均为0.1 mol·L1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c( )+c(
)+c( )]
)]
③在0.1 mol·L1氨水中滴加0.lmol·L1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c( )均增大
)均增大
⑤浓度相等的a、NH4HSO4溶液;b、NH4HCO3溶液;c、NH4Cl溶液;c( ):a>b>c
):a>b>c
⑥NaHSO3溶液显酸性,c(Na+)>c( )>c(H+)>c(OH﹣)>c(
)>c(H+)>c(OH﹣)>c( )
)
⑦常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
⑧pH=3.6的0.1mol/L HX与0.1mol/L NaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
①NaHCO3溶液加水稀释,c(Na+)/c(
 )的比值保持增大
)的比值保持增大②浓度均为0.1 mol·L1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(
 )+c(
)+c( )]
)]③在0.1 mol·L1氨水中滴加0.lmol·L1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(
 )均增大
)均增大⑤浓度相等的a、NH4HSO4溶液;b、NH4HCO3溶液;c、NH4Cl溶液;c(
 ):a>b>c
):a>b>c⑥NaHSO3溶液显酸性,c(Na+)>c(
 )>c(H+)>c(OH﹣)>c(
)>c(H+)>c(OH﹣)>c( )
)⑦常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
⑧pH=3.6的0.1mol/L HX与0.1mol/L NaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
| A.②④⑥⑦ | B.②⑤⑦⑧ | C.①③⑤⑥ | D.②⑤⑥⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:Ka1(H2SO3)=1.0×10-2、Ka2(H2SO3)=5.0×10-8。室温下,通过下列实验探究Na2SO3、NaHSO3溶液的性质。
实验1:用pH计测得某Na2SO3和NaHSO3混合溶液的pH为7。
实验2:将等体积、等物质的量浓度的Na2SO3和NaHSO3溶液混合,无明显现象。
实验3:向Na2SO3溶液中滴几滴酚酞,加水稀释,溶液红色变浅。
实验4:向NaHSO3溶液中滴加少量Ba(OH)2溶液,产生白色沉淀。
下列说法正确的是
实验1:用pH计测得某Na2SO3和NaHSO3混合溶液的pH为7。
实验2:将等体积、等物质的量浓度的Na2SO3和NaHSO3溶液混合,无明显现象。
实验3:向Na2SO3溶液中滴几滴酚酞,加水稀释,溶液红色变浅。
实验4:向NaHSO3溶液中滴加少量Ba(OH)2溶液,产生白色沉淀。
下列说法正确的是
A.实验1混合溶液中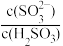 =5.0×104 =5.0×104 |
B.实验2混合后的溶液中存在:3c(Na+)=2[c( )+c( )+c(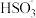 )+c(H2SO3)] )+c(H2SO3)] |
C.实验3中随水的不断加入,溶液中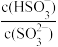 的值逐渐变小 的值逐渐变小 |
D.实验4中反应的离子方程式为Ba2++ =BaSO3↓ =BaSO3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】 下列说法正确的是
A.25℃时 溶液的Kw大于 溶液的Kw大于 时 时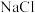 溶液的Kw 溶液的Kw |
B.SO2通入碘水中,反应离子方程式为 |
C.加入铝粉能产生H2的溶液中,可能存在大量的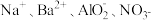 |
D.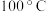 时,将pH=2的盐酸与pH=12的 时,将pH=2的盐酸与pH=12的 溶液等体积混合,溶液显中性 溶液等体积混合,溶液显中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向1L 0.1mol·L−1一元酸HR溶液中逐渐通入氨气(已知常温下NH3·H2O电离平衡常数K=1.76×10-5),使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
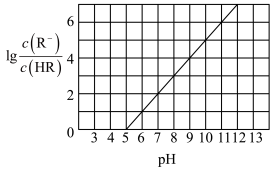

| A.当c(R-)=c(HR)时,溶液必为中性 |
| B.0.1mol·L-1HR溶液的pH为5 |
C.HR为弱酸,常温时随着氨气的通入, 逐渐增大 逐渐增大 |
| D.当通入0.1 mol NH3时,c(NH4+)>c(R-)>c(OH-)>c(H+) |
您最近一年使用:0次

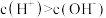 ,水溶液一定呈酸性
,水溶液一定呈酸性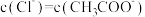
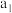 、
、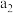 ,则
,则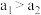
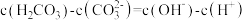
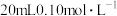 的二元酸
的二元酸 溶液中滴加相同浓度的
溶液中滴加相同浓度的 溶液,
溶液, ,下列说法错误的是
,下列说法错误的是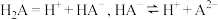
 时,溶液的
时,溶液的
 时,溶液中有
时,溶液中有
 时,溶液中有
时,溶液中有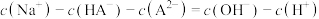
 溶液加水稀释时,
溶液加水稀释时, 将减小
将减小 、
、
 的稀
的稀 与
与 的氨水等体积混合后恰好完全反应,则
的氨水等体积混合后恰好完全反应,则
 ②
② ③
③ ,
, 由小到大的顺序是①③②
由小到大的顺序是①③②

