将 与
与 在一定条件下反应可以制甲醇,从而实现温室气体的资源化利用,相关反应如下:
在一定条件下反应可以制甲醇,从而实现温室气体的资源化利用,相关反应如下:
Ⅰ.
Ⅱ.
下列说法错误的是

 与
与 在一定条件下反应可以制甲醇,从而实现温室气体的资源化利用,相关反应如下:
在一定条件下反应可以制甲醇,从而实现温室气体的资源化利用,相关反应如下:Ⅰ.

Ⅱ.

下列说法错误的是

| A.反应Ⅰ的能量变化如图所示 |
B.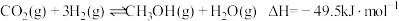 |
| C.升高温度,反应Ⅰ、反应Ⅱ的反应速率都加快 |
D.为提高平衡时 的转化率,应选择较高的温度 的转化率,应选择较高的温度 |
更新时间:2022-04-23 20:27:47
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将一定量的 与
与 通入某密闭容器中合成甲醇,在催化剂作用下发生反应:
通入某密闭容器中合成甲醇,在催化剂作用下发生反应:
Ⅰ.
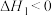 ;
;
Ⅱ.
 。
。
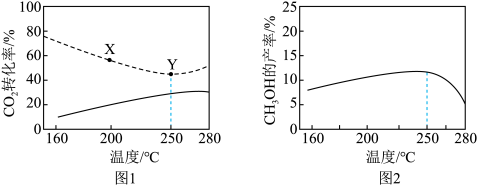
催化反应相同时间,测得不同温度下 的转化率如图1所示(图中虚线表示相同条件下
的转化率如图1所示(图中虚线表示相同条件下 的平衡转化率随温度的变化),
的平衡转化率随温度的变化), 的产率如图2所示。下列有关说法错误的是
的产率如图2所示。下列有关说法错误的是
 与
与 通入某密闭容器中合成甲醇,在催化剂作用下发生反应:
通入某密闭容器中合成甲醇,在催化剂作用下发生反应:Ⅰ.

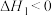 ;
;Ⅱ.

 。
。催化反应相同时间,测得不同温度下
 的转化率如图1所示(图中虚线表示相同条件下
的转化率如图1所示(图中虚线表示相同条件下 的平衡转化率随温度的变化),
的平衡转化率随温度的变化), 的产率如图2所示。下列有关说法错误的是
的产率如图2所示。下列有关说法错误的是
A. |
| B.加入催化剂可以使X点转化为Y点 |
C.250℃前,随温度升高, 的平衡转化率减小,可能是该温度范围内温度对反应Ⅰ的影响大于反应Ⅱ 的平衡转化率减小,可能是该温度范围内温度对反应Ⅰ的影响大于反应Ⅱ |
D.250℃后,随温度升高, 的产率减小,可能是因为催化剂对反应Ⅰ的活性降低 的产率减小,可能是因为催化剂对反应Ⅰ的活性降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 、
、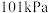 下:
下:
①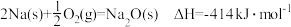
②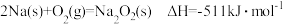
下列说法正确的是
 、
、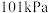 下:
下:①
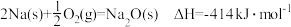
②
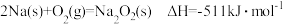
下列说法正确的是
A.各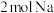 分别同时发生上述反应,转移电子数均为 分别同时发生上述反应,转移电子数均为 |
| B.锂、钠、钾都处于同一主族,根据元素周期律可得锂与钾在过量的氧气中点燃产物均为对应的过氧化物 |
C. 与少量 与少量 点燃产物为 点燃产物为 |
D. 、 、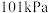 下 下 |
您最近一年使用:0次
【推荐3】二氧化碳加氢合成二甲醚(CH3OCH3)具有重要的现实意义和广阔的应用前景。该方法主要涉及下列反应:
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
反应Ⅲ:2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5kJ·mol-1
下列说法不正确的是
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
反应Ⅲ:2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5kJ·mol-1
下列说法不正确的是
| A.CO2大量排放可导致温室效应 |
| B.干冰升华吸热是因为CO2分子中共价键发生断裂 |
C.反应I的平衡常数可表示为K = |
| D.反应2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)的ΔH= -122.5kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O②适当升温③加NaOH固体④加NaCl溶液⑤滴入几滴硫酸铜溶液⑥改用10mL0.1mol/L盐酸
①加H2O②适当升温③加NaOH固体④加NaCl溶液⑤滴入几滴硫酸铜溶液⑥改用10mL0.1mol/L盐酸
| A.①③⑥ | B.②⑥ | C.③⑥ | D.④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在不同条件下进行 分解实验,
分解实验, 的浓度减少一半所需时间(t)如下表所示,
的浓度减少一半所需时间(t)如下表所示,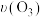 表示该段时间内
表示该段时间内 的平均分解速率。已知
的平均分解速率。已知 的起始浓度为
的起始浓度为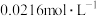 ,下列说法正确的是
,下列说法正确的是
 分解实验,
分解实验, 的浓度减少一半所需时间(t)如下表所示,
的浓度减少一半所需时间(t)如下表所示,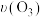 表示该段时间内
表示该段时间内 的平均分解速率。已知
的平均分解速率。已知 的起始浓度为
的起始浓度为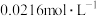 ,下列说法正确的是
,下列说法正确的是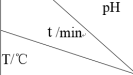 | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
A.依据信息可知, 对 对 分解起催化作用 分解起催化作用 |
B.在30℃、pH=4.0条件下, |
C.50℃、PH=5.5条件下的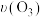 比25℃、pH=6.0条件下的 比25℃、pH=6.0条件下的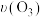 的大 的大 |
D.相同pH条件下,温度每升高10℃,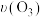 增大一倍 增大一倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在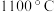 ,一定容积的密闭容器中发生反应:
,一定容积的密闭容器中发生反应: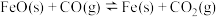
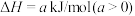 ,该温度下
,该温度下 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
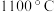 ,一定容积的密闭容器中发生反应:
,一定容积的密闭容器中发生反应: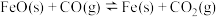
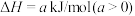 ,该温度下
,该温度下 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是A.若生成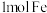 ,则吸收的热量小于 ,则吸收的热量小于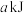 |
| B.若升高温度,正反应速率加快,化学平衡常数减小,化学平衡正向移动 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
D.达到化学平衡状态时,若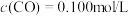 ,则 ,则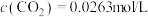 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g) 2Z(g)△H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g)△H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
下列说法正确 的是( )
 2Z(g)△H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g)△H<0。一段时间后达到平衡,反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.其他条件不变,向平衡体系中再充入0.16mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数减小 |
| B.其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正) |
| C.其他条件不变,起始时向容器中充入0.32mol气体X和0.32mol气体Y,到达平衡时,c(Z)=0.24mol•L-l |
| D.该温度下此反应的平衡常数:K=1.44 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g) 4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:
4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:
下列说法中错误的是
 4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:
4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
| A.500s时O2的浓度为0.075mol/L |
| B.平衡后,升高温度,逆反应速率增大 |
| C.平衡后,要使平衡常数减小,改变的条件是降低温度 |
| D.1000s时将容器的体积缩小一半,重新达到平衡时0.25mol/L<c(N2O5)<0.50mol/L |
您最近一年使用:0次



