 是一种可溶于水的二元弱碱,在水中能电离出
是一种可溶于水的二元弱碱,在水中能电离出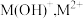 。已知
。已知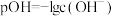 。常温下,向
。常温下,向 溶液中滴加某浓度的硫酸溶液,调节
溶液中滴加某浓度的硫酸溶液,调节 的值,测得溶液的
的值,测得溶液的 随x{
随x{ 或
或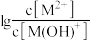 }的变化关系如图所示。下列说法正确的是
}的变化关系如图所示。下列说法正确的是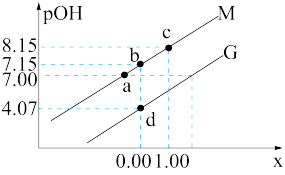
| A.溶液中水的电离程度:a点大于b点 |
B.曲线M代表 与 与 的变化关系 的变化关系 |
C.常温下,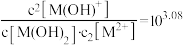 |
D.b点处有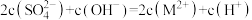 |
更新时间:2022-10-13 21:37:16
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】向NaOH溶液中缓慢通入 气体,溶液中
气体,溶液中 的物质的量与通入
的物质的量与通入 物质的量的关系图如下。下列关于图中a、b两点溶液的说法错误的是
物质的量的关系图如下。下列关于图中a、b两点溶液的说法错误的是

 气体,溶液中
气体,溶液中 的物质的量与通入
的物质的量与通入 物质的量的关系图如下。下列关于图中a、b两点溶液的说法错误的是
物质的量的关系图如下。下列关于图中a、b两点溶液的说法错误的是
| A.a、b溶液与同浓度盐酸完全反应时,消耗盐酸的体积相同 |
| B.a溶液中水的电离程度与b溶液中水的电离程度相同 |
C.a、b两溶液都满足: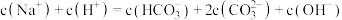 |
D.将a、b两点混合后溶液满足: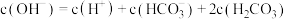 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在一定条件下,用0.1000mol/L的高氯酸溶液滴定10.0mL某弱酸酸式盐KHP溶液,测得电压变化与滴入HClO4溶液的体积关系如图所示。做空白对照实验,消耗HClO4溶液的体积为0.25mL。已知N为滴定终点。下列说法正确的是

| A.初始时该酸式盐KHP的浓度为0.1725mol/L |
B.M点时溶液中存在: |
C.水的电离程度: |
D.已知 的 的 ,若M点处为中性,则有 ,若M点处为中性,则有 约为1 约为1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,用10mL0.1mol·L-1Na2A溶液吸收H2A气体,吸收液的pH与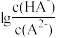 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
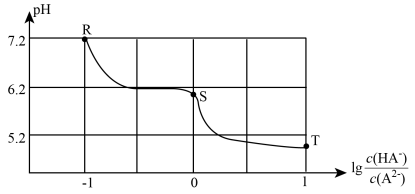
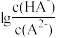 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.在R、S、T点对应溶液中,水的电离程度最小的是R点 |
| B.常温下,H2A第二步电离的平衡常数为Ka2=1.0×10–6.2 |
| C.T、S之间某点对应的溶液中存在:c(Na+)=c(HA-)+2c(A2-) |
| D.T点对应的溶液中:c(Na+)>c(A2-)>c(HA-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】25℃时,分别向浓度均为 ,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的
,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的 与加入氨水的体积变化关系如图所示。下列说法正确的是
与加入氨水的体积变化关系如图所示。下列说法正确的是
 ,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的
,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的 与加入氨水的体积变化关系如图所示。下列说法正确的是
与加入氨水的体积变化关系如图所示。下列说法正确的是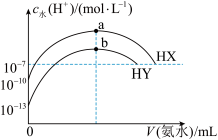
A.HY的电离方程式为 |
B.b点时溶液中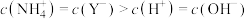 |
C.HX的电离平衡常数约为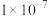 |
| D.a、b两点对应溶液中存在的微粒种类、数目相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】乙二胺(H2NCH2CH2NH2)是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是


| A.Kb2[H2NCH2CH2NH2]的数量级为10-8 |
B.曲线G代表pH与lg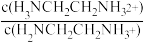 的变化关系 的变化关系 |
| C.H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-) |
| D.0.01mol·L-1H2NCH2CH2NH2电离度约为10% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】化学中常用AG表示溶液的酸度[ AG= ]。室温下,向20.00mL0.1000mol·L-1的某一元碱MOH溶液中滴加未知浓度的稀硫酸,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法不正确的是
]。室温下,向20.00mL0.1000mol·L-1的某一元碱MOH溶液中滴加未知浓度的稀硫酸,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法不正确的是

 ]。室温下,向20.00mL0.1000mol·L-1的某一元碱MOH溶液中滴加未知浓度的稀硫酸,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法不正确的是
]。室温下,向20.00mL0.1000mol·L-1的某一元碱MOH溶液中滴加未知浓度的稀硫酸,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法不正确的是
| A.室温下MOH的电离平衡常数Kb≈1.0×10-5 |
B.当AG=0时,溶液中存在: c(M+ )>c(SO )>c(H+)=c(OH- ) )>c(H+)=c(OH- ) |
C.a点对应的溶液中:c(M+)+c(MOH)= 8c(SO ) ) |
| D.b、c、d三点对应的溶液中,水的电离程度大小关系: c>b=d |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】25℃时,将1.0Lcmol·L-1CH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入CH3COOH或NaOH固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述不正确的是
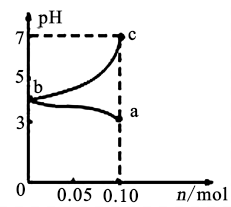

A.该温度下,醋酸的电离平衡常数Ka=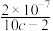 |
| B.若在c点对应的溶液中继续加入NaOH固体,则水电离出的c(H+)不可能为1×10-7mol·L-1 |
| C.a点对应的溶液中:c(CH3COOH)+c(CH3COO-)>3c(Na+) |
| D.a、b、c三点均存在c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知Kb(NH3·H2O)=1.7×10-5,Ka(CH3COOH)=1.7×10-5。25℃时,向20mL浓度均为0.01mol/L的盐酸和醋酸的混合溶液中逐滴加入0.01mol/L的氨水,测定过程中电导率和pH变化曲线如图所示,下列说法错误的是
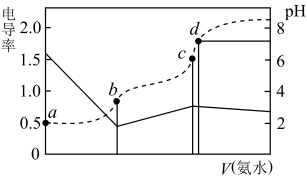

| A.a点溶液中,c(CH3COO-)数量级约为10-5 |
B.b点溶液中,c(Cl-)>c(NH )>c(CH3COOH)>c(H+)>c(OH-) )>c(CH3COOH)>c(H+)>c(OH-) |
C.c点溶液中,c(NH )+c(NH3·H2O)=c(CH3COO-)+c(CH3COOH) )+c(NH3·H2O)=c(CH3COO-)+c(CH3COOH) |
D.d点溶液中,c(NH )=c(CH3COOH)+2c(CH3COO-) )=c(CH3COOH)+2c(CH3COO-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,向1L 1.0 molLNaClO溶液中缓慢通入SO2气体,使其充分吸收,溶液pH与通入SO2物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解),下列说法正确的是


| A.常温下,NaClO水解平衡常数的数量级为10-4 |
| B.a点溶液中存在c(HClO)=c(ClO-) |
C.b点时溶液发生反应的离子方程式为SO2+H2O+ClO- =SO +Cl- +2H+ +Cl- +2H+ |
D.c点溶液中存在c(H+)>c(Na+)=c(SO )=c(Cl- )>c(OH-) )=c(Cl- )>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】用NaHCO3溶液处理NaAlO2溶液(由Al2O3过量NaOH溶液反应制得),测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积的变化情况如图所示。下列说法正确的是
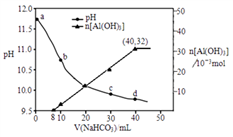

| A.Al(OH)3的生成是因为NaHCO3促进了NaAlO2的水解 |
| B.b点和c点溶液所含微粒种类不同 |
| C.NaHCO3溶液的物质的量浓度为1.0mol·L-1 |
| D.d点时:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向 100mL Na2CO3 与 NaAlO2 的混合溶液中逐滴加入 1mol/L 的盐酸,测得溶液中的 CO32-、HCO3- 、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。下列说法正确的是


| A.原 混 合 溶 液 中 的 n (CO32-): n (AlO2-)=2:1 |
| B.a 点溶液中:c(HCO3-)+c(H2CO3)+c(H+)=c(OH-) |
| C.b 点溶液中离子浓度顺序为:c(Cl-)>c(HCO3-)>c(CO32-)>c(OH- ) |
| D.d→e 的过程中水的电离程度逐渐减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】用一定浓度的H2SO4溶液分别滴定体积均为20.00mL、浓度均为0.100mol•L-1的Ba(OH)2、NaOH和NH3•H2O三种溶液,滴定过程中三种溶液的电导率如图所示。(已知:溶液电导率越大,导电能力越强)下列说法错误的是
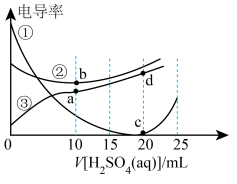

| A.曲线①②③分别代表Ba(OH)2、NaOH和NH3•H2O |
| B.H2SO4的浓度为0.100mol•L-1 |
| C.a、b、c、d四点中,d点水的电离程度最小 |
D.d点对应的溶液中粒子浓度大小关系:c(H+)=c(NH )+c(NH3•H2O)+c(OH﹣) )+c(NH3•H2O)+c(OH﹣) |
您最近一年使用:0次



