常温下,向20mL NaB溶液中滴入等浓度的HA溶液,所得溶液中
NaB溶液中滴入等浓度的HA溶液,所得溶液中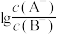 与1g
与1g 的关系如图所示。已知
的关系如图所示。已知 ,下列说法错误的是
,下列说法错误的是
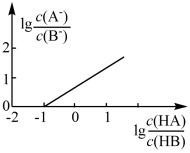
 NaB溶液中滴入等浓度的HA溶液,所得溶液中
NaB溶液中滴入等浓度的HA溶液,所得溶液中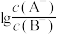 与1g
与1g 的关系如图所示。已知
的关系如图所示。已知 ,下列说法错误的是
,下列说法错误的是
A.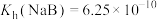 |
B.与 时相比, 时相比,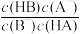 的值在 的值在 时更小 时更小 |
C.滴入20mLHA溶液后存在关系: |
D.滴入20mLHA溶液离子浓度存在关系: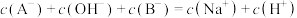 |
22-23高二上·山东烟台·期中 查看更多[2]
更新时间:2022/11/10 17:41:51
|
相似题推荐
单选题-单题
|
较难
(0.4)
解题方法
【推荐1】天然溶洞的形成与岩石中的 和空气中
和空气中 溶于天然水体形成的含碳粒子的浓度有密切关系。常温下,某溶洞水体中
溶于天然水体形成的含碳粒子的浓度有密切关系。常温下,某溶洞水体中 随
随 的变化关系如图所示。[已知:
的变化关系如图所示。[已知: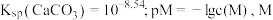 为
为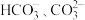 或
或 ],下列说法正确的是
],下列说法正确的是
 和空气中
和空气中 溶于天然水体形成的含碳粒子的浓度有密切关系。常温下,某溶洞水体中
溶于天然水体形成的含碳粒子的浓度有密切关系。常温下,某溶洞水体中 随
随 的变化关系如图所示。[已知:
的变化关系如图所示。[已知: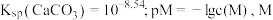 为
为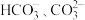 或
或 ],下列说法正确的是
],下列说法正确的是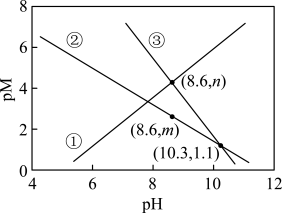
A.曲线③代表 与 与 的关系 的关系 |
B.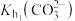 的数量级为 的数量级为 |
C.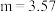 |
D. 由4到8的过程中 由4到8的过程中 增大的比 增大的比 快 快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】25℃时,0.10L某二元弱酸 用1.00
用1.00
 溶液调节其
溶液调节其 ,溶液中
,溶液中 、
、 和
和 的物质的量浓度及溶液
的物质的量浓度及溶液 与所加
与所加 溶液体积的变化关系如图所示,下列说法正确的是
溶液体积的变化关系如图所示,下列说法正确的是

 用1.00
用1.00
 溶液调节其
溶液调节其 ,溶液中
,溶液中 、
、 和
和 的物质的量浓度及溶液
的物质的量浓度及溶液 与所加
与所加 溶液体积的变化关系如图所示,下列说法正确的是
溶液体积的变化关系如图所示,下列说法正确的是
A.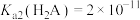 |
B.在Z点时,由水电离出的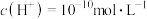 |
C.在Y点时,对应溶液中: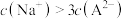 |
D.0.1  溶液中: 溶液中: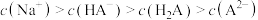 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】已知:联氨(N2H4)是二元弱碱(pKb1=6,pKb2=15;pK=-lgK),在水中的电离方式类似于氨气,常温下,向0.1mol·L-1N2H5Cl溶液通入HCl或加入NaOH固体(假设溶液总体积不变),溶液中c(N2H )随pOH变化的曲线如图所示,下列说法错误的是
)随pOH变化的曲线如图所示,下列说法错误的是

 )随pOH变化的曲线如图所示,下列说法错误的是
)随pOH变化的曲线如图所示,下列说法错误的是
A.N2H5Cl溶液c(N2H )>c(N2H4)>c(N2H )>c(N2H4)>c(N2H ) ) |
| B.b点加入NaOH(或HCl)的物质的量与d点加入HCl(或NaOH)物质的量相等 |
| C.水的电离程度:b>a |
D.若c(N2H )>c(N2H4),则pH小于3.5 )>c(N2H4),则pH小于3.5 |
您最近一年使用:0次
单选题-单题
|
较难
(0.4)
名校
【推荐1】25℃时,用0.1mol⋅L-1的NaOH溶液滴定10mL浓度均为0.1mol⋅L-1的HX、HY的混合溶液,滴定过程中溶液的pH与微粒浓度关系如图所示,已知Ka(HX)>Ka(HY)。下列说法正确的是
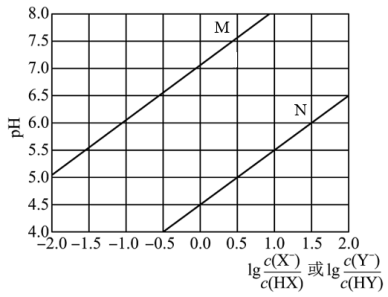
A.M表示溶液的pH与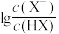 的关系 的关系 |
| B.等浓度的NaX与HY的混合溶液显碱性 |
C.当混合溶液pH=7时,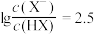 |
D.加入20mLNaOH溶液时,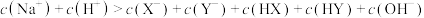 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,已知有关弱酸的电离常数如表:
下列说法不正确的是
| 弱酸 |  | HCN |  |  |
| 电离常数 |  |  | 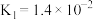 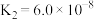 |  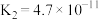 |
A.向 溶液中通入少量 溶液中通入少量 反应的离子方程式: 反应的离子方程式: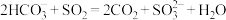 |
B.等体积等物质的量浓度的 溶液和NaCN溶液中,前者的离子总数大于后者 溶液和NaCN溶液中,前者的离子总数大于后者 |
C.等物质的量浓度的各溶液pH关系为: |
D. 、 、 、 、 、 、 四种离子中,结合H⁺的能力最强的是 四种离子中,结合H⁺的能力最强的是 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】 时,将
时,将 气体缓慢通入
气体缓慢通入 的氨水中,溶液的
的氨水中,溶液的 、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [
、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [ ]的关系如下图所示。若忽略溶液体积变化,下列错误的是
]的关系如下图所示。若忽略溶液体积变化,下列错误的是
 时,将
时,将 气体缓慢通入
气体缓慢通入 的氨水中,溶液的
的氨水中,溶液的 、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [
、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [ ]的关系如下图所示。若忽略溶液体积变化,下列错误的是
]的关系如下图所示。若忽略溶液体积变化,下列错误的是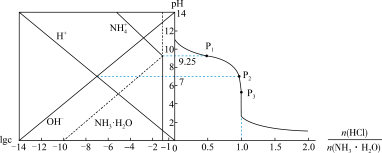
A. 时, 时, 的电离平衡常数为 的电离平衡常数为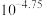 |
B. 时, 时,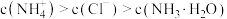 |
C. 所示溶液: 所示溶液: |
D.水的电离程度: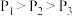 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】在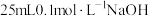 溶液中逐滴加入
溶液中逐滴加入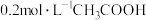 溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
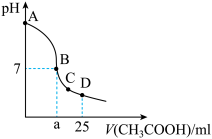
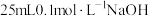 溶液中逐滴加入
溶液中逐滴加入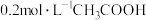 溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是 
A.在曲线的A、B间,溶液中可能有 |
B.在B点,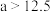 ,且有 ,且有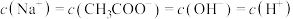 |
C.在C点, |
D.在D点,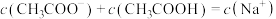 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】室温时,用 的标准
的标准 溶液滴定15.00mL浓度相等的
溶液滴定15.00mL浓度相等的 、
、 和
和 混合溶液,通过电位滴定法获得
混合溶液,通过电位滴定法获得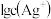 与
与 的关系曲线如图所示[忽略沉淀对离子的吸附作用。若溶液中离子浓度小于
的关系曲线如图所示[忽略沉淀对离子的吸附作用。若溶液中离子浓度小于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。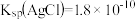 ,
,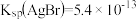 ,
,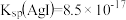 ]。下列说法错误的是
]。下列说法错误的是

 的标准
的标准 溶液滴定15.00mL浓度相等的
溶液滴定15.00mL浓度相等的 、
、 和
和 混合溶液,通过电位滴定法获得
混合溶液,通过电位滴定法获得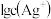 与
与 的关系曲线如图所示[忽略沉淀对离子的吸附作用。若溶液中离子浓度小于
的关系曲线如图所示[忽略沉淀对离子的吸附作用。若溶液中离子浓度小于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。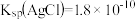 ,
,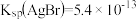 ,
,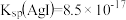 ]。下列说法错误的是
]。下列说法错误的是
| A.a点:有黄色沉淀生成 |
B.原溶液中 的浓度为 的浓度为 |
C.b点: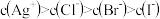 |
D.当 沉淀完全时,已经有部分 沉淀完全时,已经有部分 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】25℃时,下列溶液中各离子的浓度关系不正确的是
| A.将0.2 mol·L-1盐酸与0.2 mol·L-1K2CO3溶液等体积混合:c(K+) >c(Cl-) >c(HCO3-) >c(OH-) >c(H+) |
| B.25℃时,pH=10、浓度均为0.1 mol·L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) |
| C.0.3 mol·L-1HY溶液与0.3 mol·L-1NaOH溶液等体积混合后,溶液的pH=9,则:c(OH-)-c(HY)=c(H+)=1×10-9 mol·L-1 |
| D.用0.1 mol·L-1HCl溶液滴定10.0 mL浓度为0.1 mol·L-1Na2CO3溶液,当混合液呈中性时,c(Na+)> c(Cl-) > c(H+)= c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】25℃时,将0.01mol•L-1的盐酸逐滴加到10mL0.01mol•L-1NaA溶液中,A-、HA物质的量所占分数(δ)、pH变化曲线如甲、乙图所示。下列溶液中微粒的物质的量浓度关系正确的是


| A.溶液显中性时:c(Cl-)=c(HA) |
| B.图甲中a点对应的溶液:c(A-)<c(Cl-) |
| C.图乙中b点对应的溶液:c(Cl-)>c(HA) >c(A-)>c(OH-)>c(H+) |
| D.a点对应的pH=9.5,则常温下,HA的电离平衡常数:Ka(HA)=10-4.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】25℃时,向H2CO3溶液中滴入NaOH溶液,溶液中H2CO3、HCO3-及CO32-的物质的量分数δ(X)随溶液pH 的变化如图所示{δ(X)=[c(X)/c(H2CO3)+c(HCO3-)+c(CO32-)]×100%}。

下列说法错误的是

下列说法错误的是
| A.H2CO3的一级电离平衡常数的对数值lgK1(H2CO3)=-6.38 |
| B.pH=13时,c(Na+)十c(H+)=c(OH-)+2c(CO32-) |
C.25℃时,反应CO32-+H2O HCO3-+OH-的平衡常数对数值1gK=-3.79 HCO3-+OH-的平衡常数对数值1gK=-3.79 |
| D.pH=7时,c(HCO3-)>c(H2CO3)> c(CO32-) |
您最近一年使用:0次

 与lgc(OH-)的关系如图所示。下列说法正确的是
与lgc(OH-)的关系如图所示。下列说法正确的是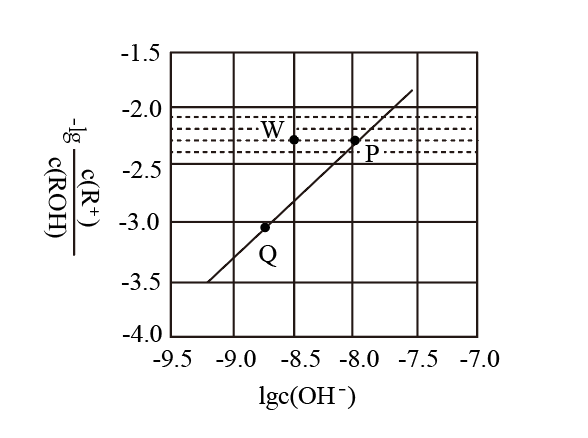
 )
)

