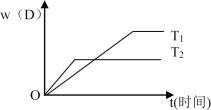
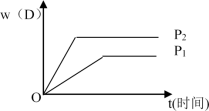
在T℃下,向装有5mL0.005mol·L-1 FeCl3 溶液的试管中加入5mL0.01mol·L-1 KSCN 溶液,发生如下反应:FeCl3+3KSCN Fe(SCN)3+3KCl,溶液呈红色。下列叙述正确的是
Fe(SCN)3+3KCl,溶液呈红色。下列叙述正确的是
 Fe(SCN)3+3KCl,溶液呈红色。下列叙述正确的是
Fe(SCN)3+3KCl,溶液呈红色。下列叙述正确的是| A.升高温度,逆反应速率减小 | B.加入Fe2(SO4)3 固体,溶液血红色加深 |
| C.加入 KCl固体,溶液血红色变浅 | D.增大压强,溶液血红色加深 |
21-22高二上·浙江绍兴·期中 查看更多[2]
更新时间:2022-12-02 20:53:04
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】某构建碳骨架的反应历程如图所示。

下列说法错误的是

下列说法错误的是
| A.上述总反应的原子利用率为100% |
| B.上述过程断裂了极性键和非极性键 |
| C.上述过程中钻原子形成的化学键数目保持不变 |
| D.上述反应过程中HCo(CO)3降低了反应的活化能 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某课题组利用CO2催化氢化制甲烷,研究发现HCOOH是CO2转化为CH4的中间体,即: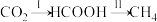 ,镍粉是反应I、II的催化剂。CH4、HCOOH、H2的产量和镍粉用量的关系如图所示(仅改变镍粉用量,其他条件不变):
,镍粉是反应I、II的催化剂。CH4、HCOOH、H2的产量和镍粉用量的关系如图所示(仅改变镍粉用量,其他条件不变):

由图可知,当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是
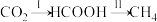 ,镍粉是反应I、II的催化剂。CH4、HCOOH、H2的产量和镍粉用量的关系如图所示(仅改变镍粉用量,其他条件不变):
,镍粉是反应I、II的催化剂。CH4、HCOOH、H2的产量和镍粉用量的关系如图所示(仅改变镍粉用量,其他条件不变):
由图可知,当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是
| A.反应I的速率增加,反应II的速率不变 |
| B.反应I的速率不变,反应II的速率增加。 |
| C.反应I、II的速率均增加,且反应I的速率增加得快 |
| D.反应I、II的速率均增加,且反应II的速率增加得快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列关于化学反应速率的说法正确的是
①恒温时,增大压强,化学反应速率一定加快
②化学反应是活化分子有合适取向的有效碰撞
③普通分子有时也能发生有效碰撞
④活化分子间的碰撞一定能发生化学反应
⑤升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
⑥有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
⑦增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
⑧催化剂能降低活化能,增大活化分子的百分数,从而增大反应速率
①恒温时,增大压强,化学反应速率一定加快
②化学反应是活化分子有合适取向的有效碰撞
③普通分子有时也能发生有效碰撞
④活化分子间的碰撞一定能发生化学反应
⑤升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
⑥有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
⑦增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
⑧催化剂能降低活化能,增大活化分子的百分数,从而增大反应速率
| A.②⑤⑧ | B.②⑥⑧ | C.②③⑤⑦⑧ | D.①②④⑤⑧ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,密闭容器中发生反应:
 ,下列图示与对应的说法相符的是
,下列图示与对应的说法相符的是

 ,下列图示与对应的说法相符的是
,下列图示与对应的说法相符的是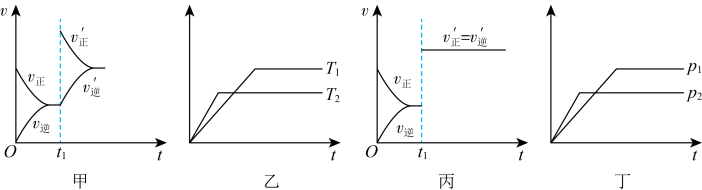
A.图甲中, 时,减小P的浓度 时,减小P的浓度 | B.图乙中,纵坐标表示生成物Q的物质的量 |
C.图丙中, 时,一定使用了催化剂 时,一定使用了催化剂 | D.图丁中,纵坐标表示反应物N的转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向一恒容密闭容器中充入A、B、C三种气体,在一定条件下发生反应,各物质的物质的量浓度随时间的变化如图a所示。若从 时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是
时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是

 时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是
时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是
A.O至 内,A与B的平均反应速率之比为3∶2 内,A与B的平均反应速率之比为3∶2 |
B.该反应的化学方程式为 |
C. 时,改变的条件可能是加入催化剂 时,改变的条件可能是加入催化剂 |
| D.该反应的正反应为放热反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2。废气中的NO2被吸附后,经处理能全部转化为HNO3。原理如图。已知: ,△H<0,下列说法不正确的是
,△H<0,下列说法不正确的是
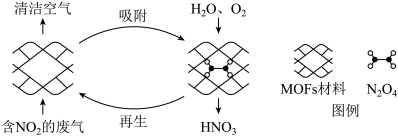
 ,△H<0,下列说法不正确的是
,△H<0,下列说法不正确的是
| A.气体温度升高后有利于N2O4的固定 |
B.使用多孔材料不能改变 的焓变 的焓变 |
C.使用多孔材料能促进 平衡正向移动,有利于NO2的去除 平衡正向移动,有利于NO2的去除 |
D.加入 H2O和O2,发生化学反应方程式为: |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】5mL0.1mol/L的KI溶液与1mL0.1mol/L的FeCl3溶液发生反应:2Fe3+(aq)+2I-(aq) 2Fe2+(aq)+I2(aq),达到平衡,下列说法中
2Fe2+(aq)+I2(aq),达到平衡,下列说法中不正确 的是
 2Fe2+(aq)+I2(aq),达到平衡,下列说法中
2Fe2+(aq)+I2(aq),达到平衡,下列说法中| A.该反应的平衡常数K=c2(Fe2+)/c(Fe3+)•c(I2) |
| B.经CCl4多次萃取后,向水溶液中滴入KSCN溶液,呈血红色,说明该反应存在限度 |
| C.加入碘化钾固体,平衡正向移动 |
| D.当溶液的颜色不再发生变化时,可以判断该反应已经达到平衡状态 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中,将一定量A、B气体混合后发生反应xA(g)+yB(g)⇌zC(g)+mD(s)。平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.3mol/L。则下列有关判断正确的是
| A.x+y>z+m | B.B的浓度增大了 |
| C.平衡向正反应方向移动 | D.B的转化率一定减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定量的混合气体在密闭容器中发生如下反应:xA(g)+yB(g) zC(g),达到平衡后测得A气体的浓度为0.5 mol/L,保持温度不变,将密闭容器的容积压缩为原来的一半再次达到平衡后,测得A浓度为0.75 mol/L,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为0.5 mol/L,保持温度不变,将密闭容器的容积压缩为原来的一半再次达到平衡后,测得A浓度为0.75 mol/L,则下列叙述正确的是
 zC(g),达到平衡后测得A气体的浓度为0.5 mol/L,保持温度不变,将密闭容器的容积压缩为原来的一半再次达到平衡后,测得A浓度为0.75 mol/L,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为0.5 mol/L,保持温度不变,将密闭容器的容积压缩为原来的一半再次达到平衡后,测得A浓度为0.75 mol/L,则下列叙述正确的是| A.平衡向逆反应方向移动 | B.x+y<z |
| C.B的物质的量浓度减小 | D.C的体积分数增大 |
您最近半年使用:0次


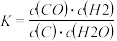
 溶液,蓝色褪去(已知碘水中存在平衡:
溶液,蓝色褪去(已知碘水中存在平衡:
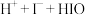 )。为探究褪色原因,设计的实验过程如图所示:
)。为探究褪色原因,设计的实验过程如图所示: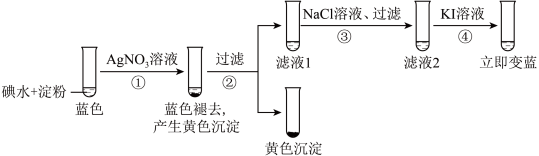
 正向移动,所得溶液中
正向移动,所得溶液中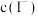 增大
增大 溶液代替
溶液代替 ,过程④中的现象仍为立即变蓝
,过程④中的现象仍为立即变蓝 的微粒可能是
的微粒可能是