弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题:
(1)生活中明矾常作净水剂,其净水的原理是_______ (用离子方程式表示)。
(2)某温度下, 和
和 的电离常数数值相等,物质的量浓度相同的
的电离常数数值相等,物质的量浓度相同的 溶液和氨水混合后,溶液中
溶液和氨水混合后,溶液中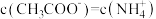 ,则所加入
,则所加入 溶液的体积
溶液的体积_______ (填“大于”“小于”或“等于”)氨水的体积。
(3)常温下,取 溶液与
溶液与 溶液等体积混合,测得混合后溶液的
溶液等体积混合,测得混合后溶液的 。写出
。写出 的电离方程式
的电离方程式_______ ,并写出所得溶液中离子浓度大小关系_______ 。
(4)含 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含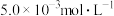 的
的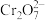 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理:

①绿矾为 ,反应(I)中
,反应(I)中 与
与 的物质的量之比为
的物质的量之比为_______ 。
②常温下若处理后的废水中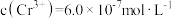 ,则处理后的废水的pH=
,则处理后的废水的pH=_______ 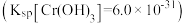 。
。
(1)生活中明矾常作净水剂,其净水的原理是
(2)某温度下,
 和
和 的电离常数数值相等,物质的量浓度相同的
的电离常数数值相等,物质的量浓度相同的 溶液和氨水混合后,溶液中
溶液和氨水混合后,溶液中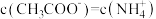 ,则所加入
,则所加入 溶液的体积
溶液的体积(3)常温下,取
 溶液与
溶液与 溶液等体积混合,测得混合后溶液的
溶液等体积混合,测得混合后溶液的 。写出
。写出 的电离方程式
的电离方程式(4)含
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含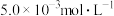 的
的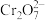 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理:
①绿矾为
 ,反应(I)中
,反应(I)中 与
与 的物质的量之比为
的物质的量之比为②常温下若处理后的废水中
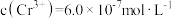 ,则处理后的废水的pH=
,则处理后的废水的pH=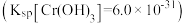 。
。
更新时间:2022-12-14 18:18:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4HSO4,⑨NH3 H2O,请回答下列问题:
H2O,请回答下列问题:
(1)NH4Cl溶液中离子浓度大小顺序为______________________ 。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)=_____ ;在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_____ 。
(3)已知水存在如下平衡:H2O+H2O H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
(4)若浓度均为0.1mol/L、等体积的NaOH和NH3 H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则 m
H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则 m_____ n(填“<”、“>”或“=”)。
(5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号)_____ 。
(6)已知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则a:b=_____ 。
 H2O,请回答下列问题:
H2O,请回答下列问题:(1)NH4Cl溶液中离子浓度大小顺序为
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)=
(3)已知水存在如下平衡:H2O+H2O
 H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
H3O++OH﹣△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。| A.向水中加入NaHSO4固体 | B.向水中加NaHCO3固体 |
| C.加热至100℃[其中c(H+)=1×10﹣6mol/L] | D.向水中加入NH4Cl固体 |
 H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则 m
H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则 m(5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH
 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号)(6)已知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则a:b=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】常温下,两种溶液 ① 0.1 mol•L-1 NH3·H2O ② 0.1 mol•L-1 NH4Cl中:
(1)溶液①的pH____ 7(填“>”、“<”或“=”),其原因是:_______________ (用电离方程式表示)
(2)溶液②呈______ 性(填“酸”、“碱”或“中”)。其原因是:__________ (用离子方程式表示)
(3)下列关于两种溶液中c(NH ) 的叙述正确的是
) 的叙述正确的是______ (填字母)。
a.两种溶液中c(NH ) 都等于0.1 mol•L-1
) 都等于0.1 mol•L-1
b.两种溶液中c(NH ) 都小于0.1 mol•L-1
) 都小于0.1 mol•L-1
c.NH4Cl溶液中c(NH ) 小于NH3·H2O溶液中c(NH
) 小于NH3·H2O溶液中c(NH )
)
(1)溶液①的pH
(2)溶液②呈
(3)下列关于两种溶液中c(NH
 ) 的叙述正确的是
) 的叙述正确的是a.两种溶液中c(NH
 ) 都等于0.1 mol•L-1
) 都等于0.1 mol•L-1b.两种溶液中c(NH
 ) 都小于0.1 mol•L-1
) 都小于0.1 mol•L-1c.NH4Cl溶液中c(NH
 ) 小于NH3·H2O溶液中c(NH
) 小于NH3·H2O溶液中c(NH )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列物质:①H2S、②NH3、③H2SO4、④NaHCO3、⑤CH3COOH、⑥KNO3溶液、⑦盐酸、⑧酒精、⑨二元酸H2A等。请回答下列问题(请填入序号)。
(1)其中一定属于弱电解质的是_______ 。不能确定的是________ ,请设计一个实验以证明它是强电解质还是弱电解质。你的实验和结论是_______ ;
(2)H2S在水中的电离方程式为________ ;NaHCO3在水中的电离方程式为_______ ;
已知H2A的电离方程式为:H2A⇌H++HA-; HA-⇌H++A2-。试判断H2A是_______ 电解质(填“强”或“弱”)。
(3)2mol/L的盐酸和2mol/L的醋酸各100ml,分别与过量的Zn反应,生成H2的体积,V(盐酸)_____ V(醋酸)(填>、=或<);氢离子浓度相等的盐酸和醋酸各100ml,分别与过量的Zn反应,生成H2的体积V(盐酸)_____ V(醋酸) (填>、=或<);理由是________ ;
(4)已知CH3COO-+H+⇌CH3COOH;现要使平衡向右移动且氢离子浓度增大,应采取的措施是_____
A.加NaOH B.加盐酸 C.加水 D.升高温度
已知CH3COOH在溶剂A中可以全部电离,盐不溶解于A溶剂。则CH3COOH在溶剂A中的电离方程式为________ ;CH3COOH和Na2CO3在溶剂A中生成CO2反应的离子方程式是__________ 。
(1)其中一定属于弱电解质的是
(2)H2S在水中的电离方程式为
已知H2A的电离方程式为:H2A⇌H++HA-; HA-⇌H++A2-。试判断H2A是
(3)2mol/L的盐酸和2mol/L的醋酸各100ml,分别与过量的Zn反应,生成H2的体积,V(盐酸)
(4)已知CH3COO-+H+⇌CH3COOH;现要使平衡向右移动且氢离子浓度增大,应采取的措施是
A.加NaOH B.加盐酸 C.加水 D.升高温度
已知CH3COOH在溶剂A中可以全部电离,盐不溶解于A溶剂。则CH3COOH在溶剂A中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填写下面的空。
(1)温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4④NH4NO3⑤NaClO ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是________
A.③①④②⑥⑤ B.③①④②⑤⑥ C.③②①⑥④⑤ D.⑤⑥②④①③
(2)25℃时,利用pH试纸测得0.1mol•L-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为_______ ;向10mL此溶液中加水稀释。pH值将_____ (填“增大”、“减小”或“无法确定”)
(3)25 ℃时,pH=3的NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______ (取近似值)
(4)pH=2的盐酸和CH3COOH溶液各1mL,分别加水至pH再次相等,则加入水的体积V(HCl)__________ V(CH3COOH)(填“>”、“<”或“=”,下同)
(5)浓度均为0.1mol/L的盐酸和CH3COOH溶液各1mL,加入等体积的水稀释后pH(HCl)_____ pH(CH3COOH)
(1)温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4④NH4NO3⑤NaClO ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
A.③①④②⑥⑤ B.③①④②⑤⑥ C.③②①⑥④⑤ D.⑤⑥②④①③
(2)25℃时,利用pH试纸测得0.1mol•L-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为
(3)25 ℃时,pH=3的NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=
(4)pH=2的盐酸和CH3COOH溶液各1mL,分别加水至pH再次相等,则加入水的体积V(HCl)
(5)浓度均为0.1mol/L的盐酸和CH3COOH溶液各1mL,加入等体积的水稀释后pH(HCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常温下,浓度均为0.1mol/L的六种溶液:
① 溶液②
溶液② 溶液③盐酸④氨水⑤
溶液③盐酸④氨水⑤ ⑥
⑥
试回答下列问题:
(1)上述溶液中有水解反应发生的是___ (填编号,下同),溶液中溶质存在电离平衡的是_____ 。
(2)比较①、②溶液,pH值较大的是______ 。
(3)加热、蒸干、灼烧⑤后所得的产物是______ 。
(4)常温时,分别向20mL0.11mol/L⑥溶液和20mL0.1mol/L③中逐滴加入0.1mol/LNaOH溶液,其pH变化曲线如图所示(忽略温度变化)。
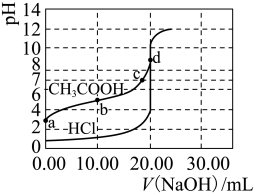
①a、b、c、d四点对应的溶液中,水的电离程度由大到小的顺序为:______ 。
②a点对应的溶液中存在关系式:
______ 0.1mol/L(填“>”、“<”或“=”下同),b点对应的溶液中:
______  。
。
(5)相同条件下,下列五种溶液中 由大到小的顺序是
由大到小的顺序是______ 。
①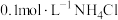 溶液②
溶液② 溶液③
溶液③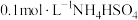 溶液④
溶液④ 氨水⑤
氨水⑤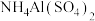 溶液
溶液
①
 溶液②
溶液② 溶液③盐酸④氨水⑤
溶液③盐酸④氨水⑤ ⑥
⑥
试回答下列问题:
(1)上述溶液中有水解反应发生的是
(2)比较①、②溶液,pH值较大的是
(3)加热、蒸干、灼烧⑤后所得的产物是
(4)常温时,分别向20mL0.11mol/L⑥溶液和20mL0.1mol/L③中逐滴加入0.1mol/LNaOH溶液,其pH变化曲线如图所示(忽略温度变化)。

①a、b、c、d四点对应的溶液中,水的电离程度由大到小的顺序为:
②a点对应的溶液中存在关系式:


 。
。(5)相同条件下,下列五种溶液中
 由大到小的顺序是
由大到小的顺序是①
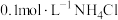 溶液②
溶液② 溶液③
溶液③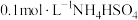 溶液④
溶液④ 氨水⑤
氨水⑤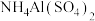 溶液
溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
Ⅰ.现有下列物质:① 晶体;②液态
晶体;②液态 ;③冰醋酸;④铜;⑤
;③冰醋酸;④铜;⑤ 固体;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨
固体;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨ 溶液。其中:
溶液。其中:
(1)能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
Ⅱ.25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(2)物质的量浓度均为的四种溶液;①②③④,溶液的由大到小的顺序是___________ (填编号,下同);
(3) 溶液显碱性的原因:
溶液显碱性的原因:___________ ;泡沫灭火器工作原理___________ (均用离子方程式表示)。
(4)下列反应不能发生的是填序号___________
(5)在25℃下,pH=8的NaOH的溶液中,水电离产生的OH -浓度为___________ ;pH=8的CH2COON的溶液中,水电离出来OH -的浓度为___________ 。
(6)25℃下,将的苛性钠溶液与的稀硫酸混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则
___________ 。
Ⅰ.现有下列物质:①
 晶体;②液态
晶体;②液态 ;③冰醋酸;④铜;⑤
;③冰醋酸;④铜;⑤ 固体;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨
固体;⑥蔗糖;⑦乙醇;⑧熔融的氯化钠;⑨ 溶液。其中:
溶液。其中:(1)能导电的是
Ⅱ.25℃时,三种酸的电离平衡常数如下:
| 化学式 |  |  |  |
| 电离平衡常数 |  |  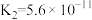 |
回答下列问题:
(2)物质的量浓度均为的四种溶液;①②③④,溶液的由大到小的顺序是
(3)
 溶液显碱性的原因:
溶液显碱性的原因:(4)下列反应不能发生的是填序号___________
A. |
B. |
C.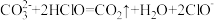 |
D.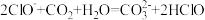 |
(6)25℃下,将的苛性钠溶液与的稀硫酸混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
 ,则
,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】25℃时,三种酸的电离平衡常数如表所示,据此回答下列问题。
(1)一般情况下,当温度升高时,电离平衡常数
________ (填“增大”“减小”或“不变”)
(2)下列四种离子结合质子能力最强的是________ (填字母)。
a. b.
b. c.
c. d.
d.
(3)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。
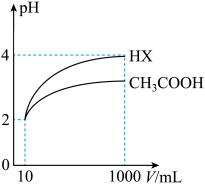
则HX的电离平衡常数________ (填或“<”,“=”或“<”下同)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的
________ 醋酸溶液中水电离出来的 ;用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸溶液
;用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸溶液________ HX溶液。
化学式 |
|
|
|
电离平衡常数 | 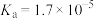 | 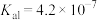  |  |
(1)一般情况下,当温度升高时,电离平衡常数

(2)下列四种离子结合质子能力最强的是
a.
 b.
b. c.
c. d.
d.
(3)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

则HX的电离平衡常数

 ;用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸溶液
;用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(NH4)2SO4是一种优良的氮肥,能使枝叶生长旺盛,提高果实的品质和产量,(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气。
(1)请写出(NH4)2SO4溶液的水解方程式:_______ (用离子方程式表示);写出(NH4)2SO3溶液中的电荷守恒:_______ 。
(2)常温下,相同物质的量浓度的(NH4)2SO3溶液与(NH4)2SO4溶液中,c(NH )较大的是
)较大的是_______ 溶液。
(3)SO2用pH相同、体积相同的三种碱:①氨水;②NaOH;③Ba(OH)2来吸收,吸收SO2的量由大到小的顺序为_______ (用编号表示)。
(1)请写出(NH4)2SO4溶液的水解方程式:
(2)常温下,相同物质的量浓度的(NH4)2SO3溶液与(NH4)2SO4溶液中,c(NH
 )较大的是
)较大的是(3)SO2用pH相同、体积相同的三种碱:①氨水;②NaOH;③Ba(OH)2来吸收,吸收SO2的量由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CH3COOH、HClO、H2CO3 是中学化学常见的弱酸,其电离平衡常数如表所示。
回答下列问题:
(1)土壤的 pH 一般在 4~9 之间。但土壤中 Na2CO3 含量较高时,pH 可高达 10.5,可喷洒___________ 以调节土壤的 pH。
A.水 B.NH4Cl 溶液 C.NaCl 溶液 D. CaCl2 溶液
(2)向 NaClO 溶液中通入少量 CO2 的化学方程式为___________ 。
(3)常温下在 20 mL 0.1 mol·L-1Na2CO3 溶液中逐滴加入0.1 mol·L-1HCl 溶液 40 mL,溶液中含碳元素的各种微粒(CO2 因逸出未画出)物质的量分数(纵轴)随溶液pH 变化的部分情况如图所示。
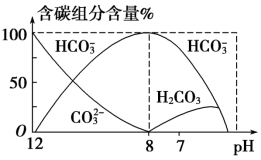
①在同一溶液中,H2CO3、 、
、
___________ (填“能”或“不能”)大量共存。
②pH= 7 时,溶液中可测出其含量的含碳元素的微粒为___________ ,溶液中各种离 子的浓度大小关系为___________ 。
③溶液中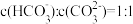 时,溶液的 pH=
时,溶液的 pH=___________ (保留小数后两位,已知 lg4.4=0.64,lg4.7=0.67)。
| 酸 | CH3COOH | HClO | H2CO3 |
电离平衡常数(常温) | K= 1.8×10-5 | K= 3.0×10-8 | K1= 4.4×10-7 K2= 4.7×10-11 |
回答下列问题:
(1)土壤的 pH 一般在 4~9 之间。但土壤中 Na2CO3 含量较高时,pH 可高达 10.5,可喷洒
A.水 B.NH4Cl 溶液 C.NaCl 溶液 D. CaCl2 溶液
(2)向 NaClO 溶液中通入少量 CO2 的化学方程式为
(3)常温下在 20 mL 0.1 mol·L-1Na2CO3 溶液中逐滴加入0.1 mol·L-1HCl 溶液 40 mL,溶液中含碳元素的各种微粒(CO2 因逸出未画出)物质的量分数(纵轴)随溶液pH 变化的部分情况如图所示。

①在同一溶液中,H2CO3、
 、
、
②pH= 7 时,溶液中可测出其含量的含碳元素的微粒为
③溶液中
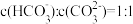 时,溶液的 pH=
时,溶液的 pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 样品中常含少量
样品中常含少量 杂质,为测定产品纯度进行如下实验:准确称取
杂质,为测定产品纯度进行如下实验:准确称取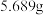 样品溶于水中,配成
样品溶于水中,配成 溶液,从中取出
溶液,从中取出 于锥形瓶中,加入适量葡萄糖,加热使
于锥形瓶中,加入适量葡萄糖,加热使 ,全部转化为
,全部转化为 ,反应为
,反应为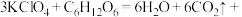
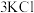 ,加入少量
,加入少量 溶液作指示剂,用
溶液作指示剂,用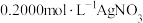 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积
溶液体积 。滴定达到终点时,产生砖红色
。滴定达到终点时,产生砖红色 ,沉淀。
,沉淀。
(1)已知: ,
,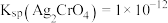 ,若终点时
,若终点时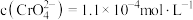 ,则此时
,则此时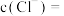
_______________  。
。
(2)计算 样品的纯度(请写出计算过程)
样品的纯度(请写出计算过程) _____________ 。
 样品中常含少量
样品中常含少量 杂质,为测定产品纯度进行如下实验:准确称取
杂质,为测定产品纯度进行如下实验:准确称取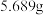 样品溶于水中,配成
样品溶于水中,配成 溶液,从中取出
溶液,从中取出 于锥形瓶中,加入适量葡萄糖,加热使
于锥形瓶中,加入适量葡萄糖,加热使 ,全部转化为
,全部转化为 ,反应为
,反应为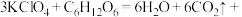
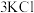 ,加入少量
,加入少量 溶液作指示剂,用
溶液作指示剂,用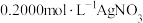 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积
溶液体积 。滴定达到终点时,产生砖红色
。滴定达到终点时,产生砖红色 ,沉淀。
,沉淀。(1)已知:
 ,
,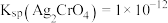 ,若终点时
,若终点时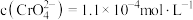 ,则此时
,则此时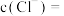
 。
。(2)计算
 样品的纯度(请写出计算过程)
样品的纯度(请写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 时,向
时,向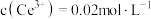 的溶液中加入氢氧化钠来调节溶液的
的溶液中加入氢氧化钠来调节溶液的 ,若反应后溶液
,若反应后溶液 ,此时
,此时 是否沉淀完全?
是否沉淀完全?__________ (填“是”或“否”),判断的理由是________ 。(要求列式计算,已知: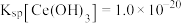 ,
,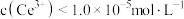 时视为沉淀完全)
时视为沉淀完全)
 时,向
时,向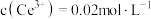 的溶液中加入氢氧化钠来调节溶液的
的溶液中加入氢氧化钠来调节溶液的 ,若反应后溶液
,若反应后溶液 ,此时
,此时 是否沉淀完全?
是否沉淀完全?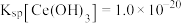 ,
,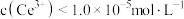 时视为沉淀完全)
时视为沉淀完全)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】含铁化合物在生活生产中应用广泛。如高铁酸盐(FeO42—)被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
(1)KClO饱和溶液与Fe(NO3)3饱和溶液反应可制备K2FeO4,两种溶液的混合方式为_______________ ,反应的离子方程为__________________________________________ 。
(2)高铁酸盐有极强的氧化性,能迅速有效地去除淤泥中的臭味物质,自身被还原成新生态的Fe(OH)3。已知Ksp[Fe(OH)3]=1.0×10-38。若要使溶液中Fe3+沉淀完全(使其浓度小于10-5 mol·L-1),需调节溶液的pH>________ 。
(3)聚合硫酸铁[Fex(OH)y(SO4)z]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用0.1000 mol·L-1的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
通过计算确定该聚合硫酸铁的化学式(写出计算过程)______________ 。
(1)KClO饱和溶液与Fe(NO3)3饱和溶液反应可制备K2FeO4,两种溶液的混合方式为
(2)高铁酸盐有极强的氧化性,能迅速有效地去除淤泥中的臭味物质,自身被还原成新生态的Fe(OH)3。已知Ksp[Fe(OH)3]=1.0×10-38。若要使溶液中Fe3+沉淀完全(使其浓度小于10-5 mol·L-1),需调节溶液的pH>
(3)聚合硫酸铁[Fex(OH)y(SO4)z]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用0.1000 mol·L-1的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
通过计算确定该聚合硫酸铁的化学式(写出计算过程)
您最近一年使用:0次




