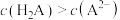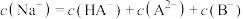时,某实验小组利用虚拟感应器技术探究用
时,某实验小组利用虚拟感应器技术探究用 的碳酸钠溶液滴定
的碳酸钠溶液滴定 的
的 溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中 的逸出)如图所示。下列说法正确的是
的逸出)如图所示。下列说法正确的是已知:
 时,
时, 的
的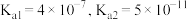 ;
;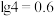 。
。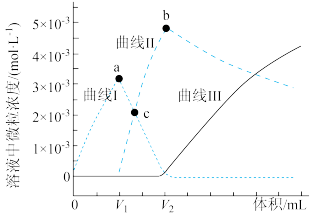
A.碳酸钠的水解常数 |
B.曲线I为 浓度变化曲线, 浓度变化曲线, |
| C.a点和b点溶液中,水的电离程度较大的是a点 |
D.c点溶液 |
更新时间:2023-01-12 19:50:40
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是
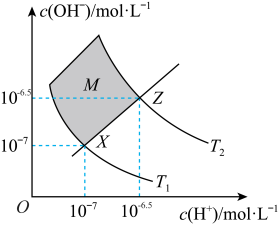

| A.XZ线上任意点均有c(H+)=c(OH-) |
| B.M区域内(不包括边界)任意点均有c(H+)<c(OH-) |
| C.温度为T2时,pH=9的NaOH溶液与pH=12的NaOH溶液等体积混合,该混合液的pH为11.7 |
| D.温度为T2时,某溶液由水电离出H+的浓度为10-8mol/L,则该溶液的pH=8 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】物质间常常相互联系、互相影响中,微粒也不例外。下列各组离子可能大量共存的是
| A.常温下水电离出的c(H+)·c(OH-)=10-2(mol·L-1)2的溶液中:Na+、Cl-、S2-、SO32- |
| B.不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、NH4+- |
| C.能与金属铝反应放出氢气的溶液中:K+、CO32-、Cl-、NH4+- |
| D.无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】HA是一元弱酸,BOH是一元弱碱,常温下,不同浓度的NaA或BCl溶液的pH与-lg 或-lg
或-lg 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是

 或-lg
或-lg 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
A.线ab表示BCl溶液的pH与-lg 的关系 的关系 |
| B.B+的水解平衡常数Kh=10-5 |
| C.等体积等浓度的HA溶液和BOH溶液混合后溶液呈中性 |
| D.水的电离程度:b=d<c=a |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】碳酸和亚硫酸电离平衡常数(25℃)如表所示:
常温下,下列说法正确的是
| 名称 | 碳酸 | 亚硫酸 |
| 电离常数 |   |   |
A.pH相同的① ② ② 溶液中 溶液中 :①>② :①>② |
B.少量 通入 通入 溶液中反应的离子方程式为: 溶液中反应的离子方程式为: |
C.在 溶液中 溶液中 |
D.等浓度的 和 和 溶液等体积混合: 溶液等体积混合: |
您最近一年使用:0次
单选题
|
较难
(0.4)
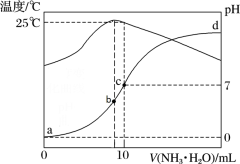
【推荐2】缓冲溶液指的是由弱酸及其盐、弱碱及其盐组成的混合溶液,能在一定程度上抵消、减轻外加强酸或强碱对溶液酸碱度的影响,从而保持溶液的pH值相对稳定。缓冲溶液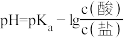 ,当酸和盐浓度相等时缓冲能力最强。丙酸(
,当酸和盐浓度相等时缓冲能力最强。丙酸(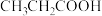 ,简写成HR)的酸性比亚硝酸(
,简写成HR)的酸性比亚硝酸( )弱。298K时,用pH为13的NaOH溶液滴定16.00ml
)弱。298K时,用pH为13的NaOH溶液滴定16.00ml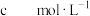 HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知:
HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知: ,
,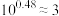 。下列叙述错误的是
。下列叙述错误的是
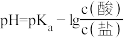 ,当酸和盐浓度相等时缓冲能力最强。丙酸(
,当酸和盐浓度相等时缓冲能力最强。丙酸(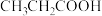 ,简写成HR)的酸性比亚硝酸(
,简写成HR)的酸性比亚硝酸( )弱。298K时,用pH为13的NaOH溶液滴定16.00ml
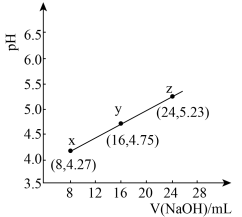
)弱。298K时,用pH为13的NaOH溶液滴定16.00ml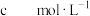 HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知:
HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知: ,
,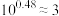 。下列叙述错误的是
。下列叙述错误的是
| A.当溶液pH为4.75时,缓冲能力最强 |
B.上述丙酸溶液浓度为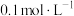 |
C.y点溶液中: |
D.其他相同, 替代HR,曲线位于图中曲线下方 替代HR,曲线位于图中曲线下方 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,向20mL 0.2mol/L H2X溶液中滴加0.2mol/L NaOH溶液,在不同pH环境下不同形态的粒子组成分数如图所示,下列说法不正确 的是
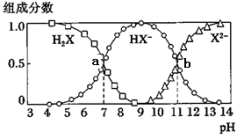

| A.水的电离程度: b点大于点a |
| B.将等物质的量的NaHX、Na2X溶于水中,所得溶液pH恰好为11 |
| C.常温下HY的K=1.1×10-10,将少量H2X溶液加入到足量NaY溶液中,发生的反应为:H2X+Y—=HY+HX— |
D.常温下,反应X2— + H2O  HX— + OH—的平衡常数对数值1gK= -3 HX— + OH—的平衡常数对数值1gK= -3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,0.2mol•L-1Na2CrO4溶液中,H2CrO4、 、
、 和
和 的分布曲线如图所示。
的分布曲线如图所示。
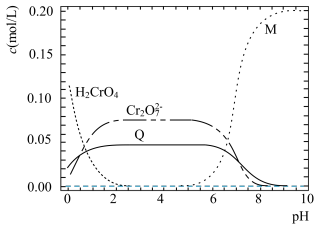
(已知:2 +2H+
+2H+
 +H2O),下列叙述错误的是
+H2O),下列叙述错误的是
 、
、 和
和 的分布曲线如图所示。
的分布曲线如图所示。
(已知:2
 +2H+
+2H+
 +H2O),下列叙述错误的是
+H2O),下列叙述错误的是A.曲线M表示pH与 的变化关系 的变化关系 |
| B.Ka2(H2CrO4)为10-1 |
C. 的电离程度大于水解程度 的电离程度大于水解程度 |
D.pH=2和pH=5时,2   +H2O的平衡常数相等 +H2O的平衡常数相等 |
您最近一年使用:0次

 和HB的混合溶液中,溶液中
和HB的混合溶液中,溶液中 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ,
,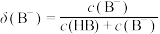 ]随pH变化的关系如图所示。下列说法正确的是
]随pH变化的关系如图所示。下列说法正确的是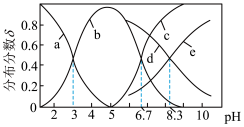
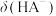 、
、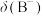 随pH变化的关系
随pH变化的关系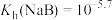 ,NaHA溶液中
,NaHA溶液中