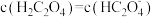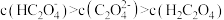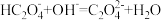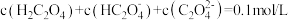25℃时,部分物质的电离平衡常数如表所示:
下列说法不正确的是
| 化学式 |  |  |
| 电离平衡常数 |   |  |
A.同浓度的 、 、 、 、 、 、 结合 结合 的能力,由强到弱的顺序为: 的能力,由强到弱的顺序为: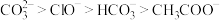 |
B.酸性由强到弱的顺序为: |
C.向 溶液中通入少量 溶液中通入少量 发生反应的离子方程式为: 发生反应的离子方程式为: |
D. 溶液中: 溶液中: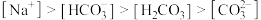 |
22-23高二上·上海松江·期末 查看更多[2]
(已下线)专题06 酸碱中和与盐类水解及难溶电解质的沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)上海市松江二中2022-2023学年高二上学期期末考试化学试题
更新时间:2023-01-13 22:47:28
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】部分弱酸的电离平衡常数如下表:
下列说法正确的是( )
| 弱酸 | CH3COOH | HBrO(性质与HClO相仿) | H2S |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.3×10-9 | Ka1=1.3×10-7 Ka2=7.1×10-13 |
| A.中和等体积、等pH的CH3COOH溶液和HBrO溶液消耗NaOH的量前者大于后者 |
| B.等体积、等浓度的CH3COONa和NaBrO溶液中所含离子总数前者等于后者 |
| C.物质的量浓度相等的CH3COONa、NaBrO和NaHS溶液的pH:NaBrO>NaHS>CH3COONa |
| D.Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】次磷酸 是一种精细磷化工产品。某实验小组以酚酞为指示剂,用
是一种精细磷化工产品。某实验小组以酚酞为指示剂,用 的
的 溶液滴定
溶液滴定 未知浓度的
未知浓度的 溶液。溶液
溶液。溶液 、各种含磷微粒的分布系数
、各种含磷微粒的分布系数 随滴加
随滴加 溶液体积
溶液体积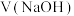 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是
[比如: 的分布系数为
的分布系数为 ;箭头指向为曲线对应的纵坐标]
;箭头指向为曲线对应的纵坐标]

 是一种精细磷化工产品。某实验小组以酚酞为指示剂,用
是一种精细磷化工产品。某实验小组以酚酞为指示剂,用 的
的 溶液滴定
溶液滴定 未知浓度的
未知浓度的 溶液。溶液
溶液。溶液 、各种含磷微粒的分布系数
、各种含磷微粒的分布系数 随滴加
随滴加 溶液体积
溶液体积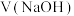 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是[比如:
 的分布系数为
的分布系数为 ;箭头指向为曲线对应的纵坐标]
;箭头指向为曲线对应的纵坐标]
A.曲线①代表 ,曲线②代表 ,曲线②代表 |
B. 溶液的浓度为 溶液的浓度为 |
C. 电离常数 电离常数 |
D. 是酸式盐,溶液显碱性 是酸式盐,溶液显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,下列有关离子浓度之间的关系不正确的是
| A.将CO2通入0.1mol/LNa2CO3溶液至中性(忽略溶液体积变化),溶液中:2c(CO32-)+c(HCO3-)=0.2mol/L |
| B.在0.1mol/LNaHCO3溶液中:c(H2CO3)+c(H+)=c(OH-)+c(CO42-) |
| C.浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后pH=5,则混合溶液中:c(Na+)>c(CH3COO-) |
| D.已知Ka(CH3COOH)=Kb(NH3·H2O),则常温下0.1mol/LCH3COONH4中:c(CH3COO-)=c(NH4+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列装置和物质,能达到相应实验目的的是
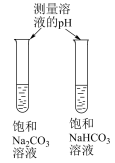 | 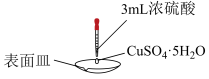 | 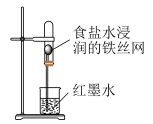 | 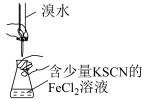 |
A.验证 的水解程度比 的水解程度比 大 大 | B.检验浓硫酸的吸水性 | C.验证铁的析氢腐蚀 | D.测定 溶液浓度 溶液浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科学探究是化学学科核心素养之一,下列实验方案设计、装置中,能达到实验目的的是


| 选项 | 实验目的 | 实验方案设计、装置 |
| A | 证明FeCl3 + 3KSCN  3KCl + Fe(SCN)3平衡向逆反应方向移动 3KCl + Fe(SCN)3平衡向逆反应方向移动 | 向 和KSCN混合溶液中,加入少量KCl的固体,溶液颜色变浅 和KSCN混合溶液中,加入少量KCl的固体,溶液颜色变浅 |
| B | 制备无水FeCl3 | 在HCl气流中加热蒸干FeCl3溶液 |
| C | 中和反应反应热的测定 | 用50 mL 0.50 mol/L醋酸和50 mL0.55 mol/L NaOH溶液反应测定中和热,装置如上图 |
| D | 证明HClO的酸性比 弱 弱 | 室温下,用pH试纸分别测定0.1 NaClO溶液和0.1 NaClO溶液和0.1  溶液的pH,前者大 溶液的pH,前者大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】有关下列两种溶液的说法中,不正确的是
①0.2 mol·L-1CH3COONa溶液 ②0.1 mol·L-1H2SO4溶液
①0.2 mol·L-1CH3COONa溶液 ②0.1 mol·L-1H2SO4溶液
| A.相同温度下,溶液中水的电离程度:①>② |
| B.向①加水后所得溶液c(CH3COO-)/c(CH3COOH)的比值变大 |
| C.等体积混合溶液①和溶液②,所得溶液中2c(SO42-) = c(Na+) |
| D.25℃时,向溶液②中滴加溶液①至pH = 7,溶液中c(Na+) >c(CH3COO-) + c(SO42-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关各溶液说法正确的是
| A.配制FeCl3溶液时,为抑制Fe3+水解,先将FeCl3固体溶解在硫酸中,再加水稀释到所需浓度 |
| B.将AlCl3溶液和Al2(SO4)3溶液蒸干所得产物相同 |
C.相同条件下,同浓度的CH3COONH4和NH4NO3溶液中,c(NH )前者大于后者 )前者大于后者 |
| D.浓NH4Cl溶液可作金属焊接的除锈剂 |
您最近一年使用:0次

 、
、
 mol•L-1的溶液中:Na+、
mol•L-1的溶液中:Na+、 、
、 、Cl-
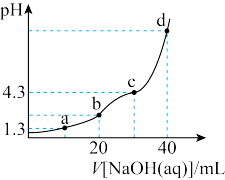
、Cl- 溶液的滴定曲线如图所示。已知
溶液的滴定曲线如图所示。已知 ,
, ,
, 。下列说法错误的是
。下列说法错误的是