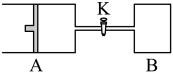
一定温度下,某密闭容器里发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )
CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )
①升高温度②将容器容积压缩到原来的一半③再通入nmolCO2和nmolH2④再通入2nmolCO2和2nmolH2
 CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )
CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )①升高温度②将容器容积压缩到原来的一半③再通入nmolCO2和nmolH2④再通入2nmolCO2和2nmolH2
| A.①②④ | B.②④ | C.③④ | D.①②③ |
更新时间:2019-12-20 13:00:44
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】通过反应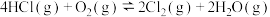 可将有机氯化工业的副产品HCl转化为
可将有机氯化工业的副产品HCl转化为 。体积不变的密闭容器中,保持
。体积不变的密闭容器中,保持 相同,进料比
相同,进料比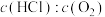 分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是
分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是
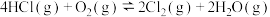 可将有机氯化工业的副产品HCl转化为
可将有机氯化工业的副产品HCl转化为 。体积不变的密闭容器中,保持
。体积不变的密闭容器中,保持 相同,进料比
相同,进料比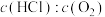 分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是
分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是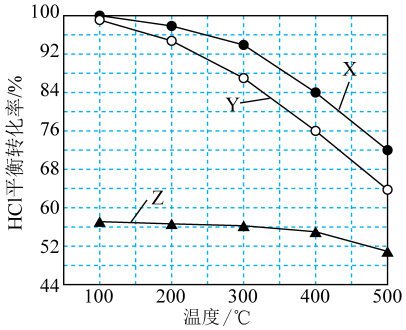
A.上述反应 |
B.曲线X表示的是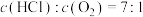 的变化 的变化 |
| C.其他条件不变,使用高效催化剂能使曲线Y与曲线X重叠 |
D.设HCl初始浓度为 ,根据进料 ,根据进料 的数据计算 的数据计算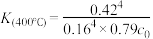 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在100℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:[2NO2(g) N2O4(g) ΔH <0]
N2O4(g) ΔH <0]
下列说法正确的是
 N2O4(g) ΔH <0]
N2O4(g) ΔH <0]| 容器 | 物质 | 起始浓度/(mol·L-1) | 平衡浓度/(mol·L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040[ |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
下列说法正确的是
| A.平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2) |
| B.平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ) = 2K(Ⅱ) |
| C.平衡后,升高相同温度,以N2O4表示的反应速率ν(Ⅰ)<ν(Ⅱ) |
| D.平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】对于平衡体系mA(g)+nB(g)⇌pC(g)+qD(g) △H=b kJ·mol-1,下列结论中错误的是
| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q |
| B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C.保持其它条件不变,升高温度,D的体积分数增大说明该反应的△H<0。 |
| D.若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
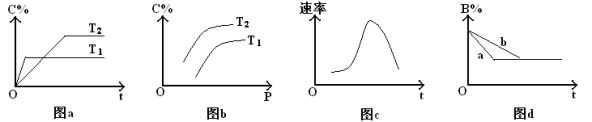
 pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
| A.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图像,由此说明该反应吸热 |
| D.图d中,若m+n=p,则曲线a一定增大了压强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】相同温度和压强下,研究Cl2分别在不同浓度的盐酸和NaCl溶液中的溶解度(用溶解Cl2的物质的量浓度表示)变化如图所示。
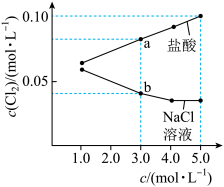
已知氯气溶解存在以下过程:
①Cl2(aq) + H2O(1) H+(aq) + Cl-(aq) + HClO(aq) K1= 4.2×10-4
H+(aq) + Cl-(aq) + HClO(aq) K1= 4.2×10-4
②Cl2(aq) + Cl-(aq)
 (aq) K2= 0.19
(aq) K2= 0.19
③HClO(aq) H+(aq) + ClO-(aq) Ka= 3.2×10-8
H+(aq) + ClO-(aq) Ka= 3.2×10-8
下列说法错误的是

已知氯气溶解存在以下过程:
①Cl2(aq) + H2O(1)
 H+(aq) + Cl-(aq) + HClO(aq) K1= 4.2×10-4
H+(aq) + Cl-(aq) + HClO(aq) K1= 4.2×10-4②Cl2(aq) + Cl-(aq)

 (aq) K2= 0.19
(aq) K2= 0.19③HClO(aq)
 H+(aq) + ClO-(aq) Ka= 3.2×10-8
H+(aq) + ClO-(aq) Ka= 3.2×10-8下列说法错误的是
A.随着NaCl浓度的增大,Cl2溶解度减小,溶液中 减小 减小 |
| B.随着盐酸浓度的增大,反应①被抑制,反应②为主要反应从而促进Cl2溶解 |
C.a点时,c(H+) >c(Cl-)>c( ) > c(ClO-) ) > c(ClO-) |
D.b点时,c(Na+) + c(H+) = c(Cl-) + c( ) + c(OH-) + c(ClO-) ) + c(OH-) + c(ClO-) |
您最近一年使用:0次
【推荐3】T℃时,体积均为0.5L的两个恒容密闭容容器中发生可逆反应:2A(g)+B(g)⇌2C(g) △H=-Q kJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如表:
下列叙述中正确的是
| 容器编号 | 起始时各物质的物质的最/mol | 达到平衡时体系能量的变化 | ||
| A | B | C | ||
| ① | 2 | 1 | 0 | 0.75Q kJ |
| ② | 0.4 | 0.2 | 1.6 | |
| A.容器①、②中反应的平衡常数均为4 |
| B.容器②中达到平衡时放出的热量为0.05Q kJ |
| C.平衡时向容器①中通入一定量的C,平衡向左移动,C的体积分数增大 |
D.其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知反应:2NO2(红棕色)⇌N2O4(无色),该反应为放热反应。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
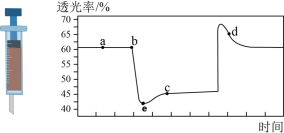
| A.b点的操作是压缩注射器 |
| B.b点v正>c点v正 |
| C.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
| D.e点是平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知一定温度下,2X(g)+Y(g)  mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
 mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是
mZ(g) ΔH=-a kJ/mol(a>0),现有甲、乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ,向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是| A.m = 4 | B.a = b | C.a <  | D.m < 3 |
您最近一年使用:0次


 ;达到平衡时,VA=1.2aL,则下列说法不正确的是
;达到平衡时,VA=1.2aL,则下列说法不正确的是