近年来,改善环境是科学研究的重要课题,对实现碳循环及废气资源的再利用技术的发展都具有重要意义。
(1)以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1 K1
CH3OH(g)+H2O(g) △H1 K1
Ⅱ.CO(g)+2H2(g) CH3OH(g) △H2 K2
CH3OH(g) △H2 K2
Ⅲ.CO2(g)+H2(g) CO(g)+H2O(g) △H3 K3
CO(g)+H2O(g) △H3 K3
则△H2=______ (用含△H1、△H3的代数式表示),K2=______ (用含K1、K3的代数式表示)。
(2)一定条件下,CH4和H2O(g)发生反应:CH4(g)+H2O(g) CO(g)+3H2(g) △H,设起始
CO(g)+3H2(g) △H,设起始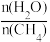 =Z,在恒压下,反应达到平衡时CH4的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
=Z,在恒压下,反应达到平衡时CH4的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是______ (填标号)。
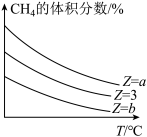
(3)在T1℃时,往10L的某恒容密闭容器中充入3molCH4(g)和5molH2O(g),发生反应CH4(g)+H2O(g) CO(g)+3H2(g),5min后该反应达到平衡,此时测得混合气体的总压强为起始压强的1.5倍,则:
CO(g)+3H2(g),5min后该反应达到平衡,此时测得混合气体的总压强为起始压强的1.5倍,则:
①0~5min内,v(H2)=______ mol•L-1•min-1,H2O(g)的平衡转化率为______ %。
②该反应的平衡常数K=______ (mol•L-1)2。
③反应达到平衡时,再充入1molH2O(g)和2molCO(g),此时v正______ (填“>”、“<”或“=”)v逆。
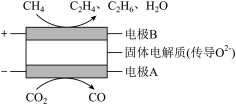
(4)CH4和CO2都是比较稳定的分子,科学家利用化学装置实现两种分子的耦合转化,其原理如图所示。若生成乙烯和乙烷的体积比为7∶3,则消耗CH4和CO2的体积比为______ 。
(1)以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1 K1
CH3OH(g)+H2O(g) △H1 K1Ⅱ.CO(g)+2H2(g)
 CH3OH(g) △H2 K2
CH3OH(g) △H2 K2Ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H3 K3
CO(g)+H2O(g) △H3 K3则△H2=
(2)一定条件下,CH4和H2O(g)发生反应:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H,设起始
CO(g)+3H2(g) △H,设起始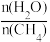 =Z,在恒压下,反应达到平衡时CH4的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
=Z,在恒压下,反应达到平衡时CH4的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
| A.若氢气的物质的量分数不再随时间而改变,则该反应达到平衡 |
| B.加入合适的催化剂,该反应的平衡转化率和△H的值均增大 |
| C.当混合气体的平均相对分子质量不再随时间而改变时,该反应达到平衡 |
| D.a>3>b |
 CO(g)+3H2(g),5min后该反应达到平衡,此时测得混合气体的总压强为起始压强的1.5倍,则:
CO(g)+3H2(g),5min后该反应达到平衡,此时测得混合气体的总压强为起始压强的1.5倍,则:①0~5min内,v(H2)=
②该反应的平衡常数K=
③反应达到平衡时,再充入1molH2O(g)和2molCO(g),此时v正
(4)CH4和CO2都是比较稳定的分子,科学家利用化学装置实现两种分子的耦合转化,其原理如图所示。若生成乙烯和乙烷的体积比为7∶3,则消耗CH4和CO2的体积比为

更新时间:2023-04-16 11:22:46
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】工业上常用合成气(主要成分为CO、 )在一定条件下制备甲醇,其涉及反应如下:
)在一定条件下制备甲醇,其涉及反应如下:
反应Ⅰ.
 ;
;
反应Ⅱ.
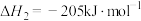 ;
;
反应Ⅲ.
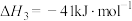 。
。
回答下列问题:
(1)在催化剂作用下也可以由CO2制备甲醇:
 ,则
,则
______  ;该反应在
;该反应在______ (填“高温”“低温”或“任意温度”)下可自发进行。
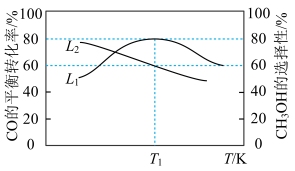
(2)向容积为2 L的刚性密闭容器中充入2 mol CO和4 mol 发生上述反应,测得不同温度下,CO的平衡转化率、
发生上述反应,测得不同温度下,CO的平衡转化率、 的选择性如图所示
的选择性如图所示 。
。______ (填“ ”或“
”或“ ”)。
”)。
② 下,2 min时达到平衡,此时体系压强为aPa,
下,2 min时达到平衡,此时体系压强为aPa,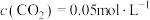 。用
。用 的分压变化表示的化学反应速率为
的分压变化表示的化学反应速率为______ 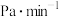 ,反应Ⅲ的
,反应Ⅲ的
______ ( ,指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压
,指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压 的物质的量分数)。
的物质的量分数)。
(3)维持CO和 的物质的量之和为3 mol,若在1 L恒容密闭容器中只发生上述反应Ⅰ,调整进气比
的物质的量之和为3 mol,若在1 L恒容密闭容器中只发生上述反应Ⅰ,调整进气比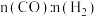 不同,温度不同时,测得相应的CO平衡转化率如图所示。则A和B两点的温度:
不同,温度不同时,测得相应的CO平衡转化率如图所示。则A和B两点的温度: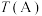
______ (填“<”“>”或“=”) ,其判断依据是
,其判断依据是______ 。
 )在一定条件下制备甲醇,其涉及反应如下:
)在一定条件下制备甲醇,其涉及反应如下:反应Ⅰ.

 ;
;反应Ⅱ.

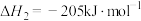 ;
;反应Ⅲ.

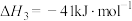 。
。回答下列问题:
(1)在催化剂作用下也可以由CO2制备甲醇:

 ,则
,则
 ;该反应在
;该反应在(2)向容积为2 L的刚性密闭容器中充入2 mol CO和4 mol
 发生上述反应,测得不同温度下,CO的平衡转化率、
发生上述反应,测得不同温度下,CO的平衡转化率、 的选择性如图所示
的选择性如图所示 。
。
 ”或“
”或“ ”)。
”)。②
 下,2 min时达到平衡,此时体系压强为aPa,
下,2 min时达到平衡,此时体系压强为aPa,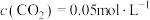 。用
。用 的分压变化表示的化学反应速率为
的分压变化表示的化学反应速率为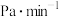 ,反应Ⅲ的
,反应Ⅲ的
 ,指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压
,指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压 的物质的量分数)。
的物质的量分数)。(3)维持CO和
 的物质的量之和为3 mol,若在1 L恒容密闭容器中只发生上述反应Ⅰ,调整进气比
的物质的量之和为3 mol,若在1 L恒容密闭容器中只发生上述反应Ⅰ,调整进气比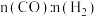 不同,温度不同时,测得相应的CO平衡转化率如图所示。则A和B两点的温度:
不同,温度不同时,测得相应的CO平衡转化率如图所示。则A和B两点的温度: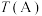
 ,其判断依据是
,其判断依据是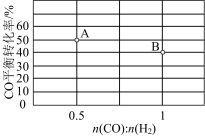
您最近一年使用:0次
【推荐2】将 转化为
转化为 能存效减少
能存效减少 排放。
排放。
(1)已知:Ⅰ.
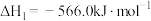
Ⅱ.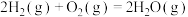
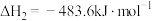
Ⅲ.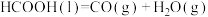
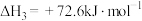
则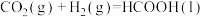

_______ 。
(2)325℃时,水在 粉表面产生
粉表面产生 和
和 ,
, 再与
再与 反应生产甲酸。
反应生产甲酸。
①由 、
、 、
、 制备甲酸的化学方程式为
制备甲酸的化学方程式为_______ 。
②直接加热 与
与 难以生成甲酸,该条件下能较快生成甲酸的原因是
难以生成甲酸,该条件下能较快生成甲酸的原因是_______ 。
(3)科学家利用 在
在 (与
(与 同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
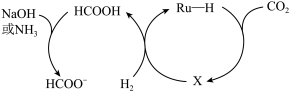
① 与
与 通过加成形成中间体X,画出中间体X的
通过加成形成中间体X,画出中间体X的结构式 :_______ 。
②反应过程中加入 或
或 的目的是
的目的是_______ 。
(4) 通过电解法转化为
通过电解法转化为 的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的
的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的 有较好的阻拦作用,可让
有较好的阻拦作用,可让 自由通过。
自由通过。
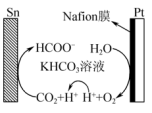
① 电极上生成
电极上生成 的电极反应式为
的电极反应式为_______ 。
②电路中通过的电量与 产率的关系如图所示,相同条件下,Pt电极有Nafion膜
产率的关系如图所示,相同条件下,Pt电极有Nafion膜 产率明显提高,但电量
产率明显提高,但电量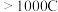 后又显著下降,可能原因是
后又显著下降,可能原因是_______ 。
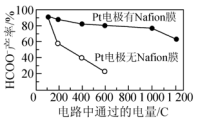
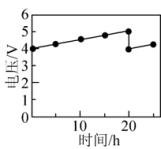
③若电解时将Nafon膜置于两个电极中间,保持电流恒定,20h时向阳极区补充 ,电压与时间关系如图所示,0~20h,电压增大的原因是
,电压与时间关系如图所示,0~20h,电压增大的原因是_______ 。
 转化为
转化为 能存效减少
能存效减少 排放。
排放。(1)已知:Ⅰ.

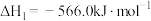
Ⅱ.
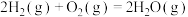
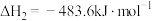
Ⅲ.
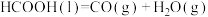
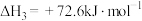
则
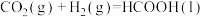

(2)325℃时,水在
 粉表面产生
粉表面产生 和
和 ,
, 再与
再与 反应生产甲酸。
反应生产甲酸。①由
 、
、 、
、 制备甲酸的化学方程式为
制备甲酸的化学方程式为②直接加热
 与
与 难以生成甲酸,该条件下能较快生成甲酸的原因是
难以生成甲酸,该条件下能较快生成甲酸的原因是(3)科学家利用
 在
在 (与
(与 同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
①
 与
与 通过加成形成中间体X,画出中间体X的
通过加成形成中间体X,画出中间体X的②反应过程中加入
 或
或 的目的是
的目的是(4)
 通过电解法转化为
通过电解法转化为 的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的
的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的 有较好的阻拦作用,可让
有较好的阻拦作用,可让 自由通过。
自由通过。
①
 电极上生成
电极上生成 的电极反应式为
的电极反应式为②电路中通过的电量与
 产率的关系如图所示,相同条件下,Pt电极有Nafion膜
产率的关系如图所示,相同条件下,Pt电极有Nafion膜 产率明显提高,但电量
产率明显提高,但电量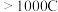 后又显著下降,可能原因是
后又显著下降,可能原因是
③若电解时将Nafon膜置于两个电极中间,保持电流恒定,20h时向阳极区补充
 ,电压与时间关系如图所示,0~20h,电压增大的原因是
,电压与时间关系如图所示,0~20h,电压增大的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】二氧化碳有效转化是“碳中和”的重要研究方向, 与
与 在催化剂条件下可转化为
在催化剂条件下可转化为 、
、 。回答下列问题:
。回答下列问题:
Ⅰ.转化为 的反应方程式为
的反应方程式为
 。
。
(1)在恒压密闭容器中,起始充入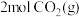 和
和 发生反应,该反应在不同的温度下达到平衡时,各组分的体积分数随温度的变化如图1所示。
发生反应,该反应在不同的温度下达到平衡时,各组分的体积分数随温度的变化如图1所示。
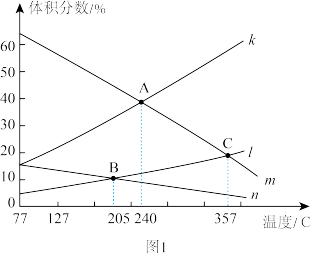
①图中表示 的体积分数随温度变化的曲线是
的体积分数随温度变化的曲线是_______ (填字母)。357℃时可以证明反应达到平衡状态的标志为_______ (填字母)。
a.
b.容器中 的体积分数保持不变
的体积分数保持不变
c.混合气体的密度保持不变
②A、B、C三点对应的化学平衡常数分别为 、
、 、
、 ,则三者从大到小的排列顺序为
,则三者从大到小的排列顺序为_______ 。
③B点反应达到平衡后, 的平衡转化率为
的平衡转化率为_______ (计算结果保留一位小数),若平衡时总压为P,则平衡常数
_______ (列出计算式,以分压表示,气体分压=总压×气体的物质的量分数)。
(2)其他条件相同,分别在X、Y两种催化剂作用下,将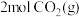 和
和 充入体积为1L的密闭容器内,测得反应相同时间时
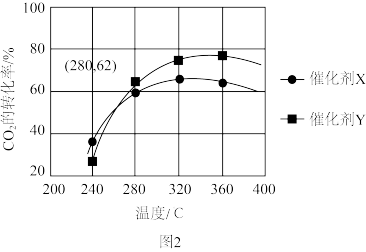
充入体积为1L的密闭容器内,测得反应相同时间时 的转化率与温度的关系如图2所示。使用催化剂X,当温度高于320℃时,
的转化率与温度的关系如图2所示。使用催化剂X,当温度高于320℃时, 的转化率逐渐下降,其原因是
的转化率逐渐下降,其原因是_______ 。根据图像,_______ (填“能”或“不能”)计算280℃时该反应的平衡常数,其理由是_______ 。
Ⅱ. 与
与 在催化剂作用下可转化为
在催化剂作用下可转化为 。主要反应如下:
。主要反应如下:
反应①:
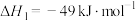
反应②:
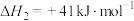
(3) 和
和 反应生成
反应生成 的热化学方程式为
的热化学方程式为_______ 。
 与
与 在催化剂条件下可转化为
在催化剂条件下可转化为 、
、 。回答下列问题:
。回答下列问题:Ⅰ.转化为
 的反应方程式为
的反应方程式为
 。
。(1)在恒压密闭容器中,起始充入
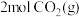 和
和 发生反应,该反应在不同的温度下达到平衡时,各组分的体积分数随温度的变化如图1所示。
发生反应,该反应在不同的温度下达到平衡时,各组分的体积分数随温度的变化如图1所示。
①图中表示
 的体积分数随温度变化的曲线是
的体积分数随温度变化的曲线是a.

b.容器中
 的体积分数保持不变
的体积分数保持不变c.混合气体的密度保持不变
②A、B、C三点对应的化学平衡常数分别为
 、
、 、
、 ,则三者从大到小的排列顺序为
,则三者从大到小的排列顺序为③B点反应达到平衡后,
 的平衡转化率为
的平衡转化率为
(2)其他条件相同,分别在X、Y两种催化剂作用下,将
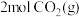 和
和 充入体积为1L的密闭容器内,测得反应相同时间时
充入体积为1L的密闭容器内,测得反应相同时间时 的转化率与温度的关系如图2所示。使用催化剂X,当温度高于320℃时,
的转化率与温度的关系如图2所示。使用催化剂X,当温度高于320℃时, 的转化率逐渐下降,其原因是
的转化率逐渐下降,其原因是
Ⅱ.
 与
与 在催化剂作用下可转化为
在催化剂作用下可转化为 。主要反应如下:
。主要反应如下:反应①:

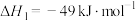
反应②:

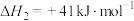
(3)
 和
和 反应生成
反应生成 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】 常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为
常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为 ,含
,含 、
、 氧化物等杂质)为主要原料制备
氧化物等杂质)为主要原料制备 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
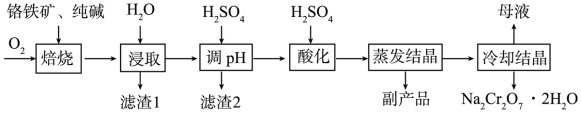
(1)铬铁矿“焙烧”前,为提高焙烧效率,可采取的措施有___________ (任写一点)。
(2)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
(3)“滤渣1”的主要成分为 等难溶于水的物质,则“滤渣2”的主要成分为
等难溶于水的物质,则“滤渣2”的主要成分为___________ (填化学式)。
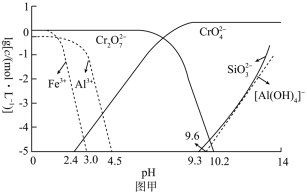
(4)已知各离子浓度的对数 与
与 的关系如图甲所示。当溶液中某种粒子浓度
的关系如图甲所示。当溶液中某种粒子浓度 时,可认为该离子已除尽,则“调
时,可认为该离子已除尽,则“调 ”时
”时 的理论范围为
的理论范围为___________ ;“酸化”的目的是___________ 。
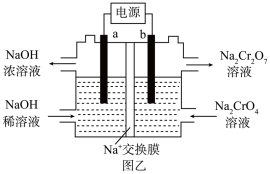
(5)利用膜电解技术,以 为主要原料制备
为主要原料制备 的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的
的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的___________ 极相连,制备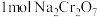 时,理论上左侧溶液总质量增重
时,理论上左侧溶液总质量增重___________ g。
(6)为了测定 产品的纯度,可采用
产品的纯度,可采用 标准溶液通过氧化还原反应滴定
标准溶液通过氧化还原反应滴定 溶液。下列关于滴定分析的操作,正确的是___________(填标号)。
溶液。下列关于滴定分析的操作,正确的是___________(填标号)。
 常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为
常用作制革工业的鞣革剂,工业上以铬铁矿(主要成分为 ,含
,含 、
、 氧化物等杂质)为主要原料制备
氧化物等杂质)为主要原料制备 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题:
(1)铬铁矿“焙烧”前,为提高焙烧效率,可采取的措施有
(2)基态
 原子的价电子排布式为
原子的价电子排布式为(3)“滤渣1”的主要成分为
 等难溶于水的物质,则“滤渣2”的主要成分为
等难溶于水的物质,则“滤渣2”的主要成分为(4)已知各离子浓度的对数
 与
与 的关系如图甲所示。当溶液中某种粒子浓度
的关系如图甲所示。当溶液中某种粒子浓度 时,可认为该离子已除尽,则“调
时,可认为该离子已除尽,则“调 ”时
”时 的理论范围为
的理论范围为

(5)利用膜电解技术,以
 为主要原料制备
为主要原料制备 的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的
的工作原理如图乙所示(a、b电极材料均为石墨):a极与电源的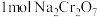 时,理论上左侧溶液总质量增重
时,理论上左侧溶液总质量增重(6)为了测定
 产品的纯度,可采用
产品的纯度,可采用 标准溶液通过氧化还原反应滴定
标准溶液通过氧化还原反应滴定 溶液。下列关于滴定分析的操作,正确的是___________(填标号)。
溶液。下列关于滴定分析的操作,正确的是___________(填标号)。A.用移液管量取 待测液转移至锥形瓶中 待测液转移至锥形瓶中 |
| B.滴定开始时可以让液体成线状快速流下,接近滴定终点时减慢滴加速率,必要时采用半滴操作 |
| C.排气泡时应使管尖弯曲向上,用右手挤压玻璃珠上方,使液体充满管尖 |
| D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】我国钒钛磁铁矿分布广泛,储量丰富,不仅是铁的重要来源,其中伴生的钛、钒、铝等多种成分还具有很高的利用价值。其尾矿是工业提取钛的重要来源
I.钒钛磁铁矿的尾矿(主要成分为FeTiO3,还含有少量FeO、Al2O3、SiO2 等杂质) 经选矿后得到钛精矿过一系列反应制得TiO2:

(1)氢氧化钠净化尾矿的目的是_________________________________ 。
(2)写出钛精矿中FeTiO3与80%硫酸溶液反应的化学方程式:___________________ 。
Ⅱ.以TiO2 为原料制备金属钛,流程如下: TiO2→TiCl4→Ti
(3)已知反应:TiO2(s)十2Cl2(g)=TiCl4(l)十O2(g) △H=十151kJ/mol,但不能由TiO2和Cl2直接反应(即氯化反应)来制取TiCl4试解释原因:___________________________________ 。
(4)当往氯化反应体系中加入碳后,使得该反应在高温条件下能顺利制得TiCl4,从化学平衡的角度解释其原因___________________________________________ 。
(5)已知碳的燃烧热394kJ/mol,请写出TiO2 与Cl2、C反应制取TiCl4的热化学方程式_____________ 。
Ⅲ.以TiO2为原料可以制备Li4Ti5O12(一种锂离子电池的电极材料),过程如下:

(6)不同温度下,TiO2·xH2O与双氧水、氨水反应达到平衡所得实验结果如下表所示:
该过程的理想温度为_______________ ,分析表中数据,解释TiO2·xH2O的转化率随温度变化的原因:_______________________________________ ,该反应的离子方程式为________________________ 。
I.钒钛磁铁矿的尾矿(主要成分为FeTiO3,还含有少量FeO、Al2O3、SiO2 等杂质) 经选矿后得到钛精矿过一系列反应制得TiO2:

(1)氢氧化钠净化尾矿的目的是
(2)写出钛精矿中FeTiO3与80%硫酸溶液反应的化学方程式:
Ⅱ.以TiO2 为原料制备金属钛,流程如下: TiO2→TiCl4→Ti
(3)已知反应:TiO2(s)十2Cl2(g)=TiCl4(l)十O2(g) △H=十151kJ/mol,但不能由TiO2和Cl2直接反应(即氯化反应)来制取TiCl4试解释原因:
(4)当往氯化反应体系中加入碳后,使得该反应在高温条件下能顺利制得TiCl4,从化学平衡的角度解释其原因
(5)已知碳的燃烧热394kJ/mol,请写出TiO2 与Cl2、C反应制取TiCl4的热化学方程式
Ⅲ.以TiO2为原料可以制备Li4Ti5O12(一种锂离子电池的电极材料),过程如下:

(6)不同温度下,TiO2·xH2O与双氧水、氨水反应达到平衡所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
| TiO2·xH2O 的转化率 | 80% | 90% | 97% | 93% | 82% |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
真题
【推荐3】水煤气是 的主要来源,研究
的主要来源,研究 对
对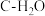 体系制
体系制 的影响,涉及主要反应如下:
的影响,涉及主要反应如下:
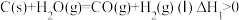

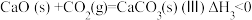
回答列问题:
(1)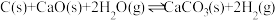 的焓变
的焓变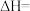
_______ (用代数式表示)。
(2)压力p下,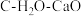 体系达平衡后,图示温度范围内
体系达平衡后,图示温度范围内 已完全反应,
已完全反应, 在
在 温度时完全分解。气相中
温度时完全分解。气相中 ,
, 和
和 摩尔分数随温度的变化关系如图所示,则a线对应物种为
摩尔分数随温度的变化关系如图所示,则a线对应物种为_______ (填化学式)。当温度高于 时,随温度升高c线对应物种摩尔分数逐渐降低的原因是
时,随温度升高c线对应物种摩尔分数逐渐降低的原因是_______ 。 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应
时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应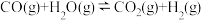 的平衡常数
的平衡常数
_______ ;此时气体总物质的量为 ,则
,则 的物质的量为
的物质的量为_______  ;若向平衡体系中通入少量
;若向平衡体系中通入少量 ,重新达平衡后,分压
,重新达平衡后,分压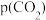 将
将_______ (填“增大”“减小”或“不变”),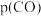 将
将_______ (填“增大”“减小”或“不变”)。
 的主要来源,研究
的主要来源,研究 对
对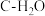 体系制
体系制 的影响,涉及主要反应如下:
的影响,涉及主要反应如下: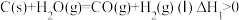

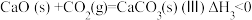
回答列问题:
(1)
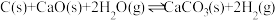 的焓变
的焓变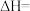
(2)压力p下,
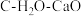 体系达平衡后,图示温度范围内
体系达平衡后,图示温度范围内 已完全反应,
已完全反应, 在
在 温度时完全分解。气相中
温度时完全分解。气相中 ,
, 和
和 摩尔分数随温度的变化关系如图所示,则a线对应物种为
摩尔分数随温度的变化关系如图所示,则a线对应物种为 时,随温度升高c线对应物种摩尔分数逐渐降低的原因是
时,随温度升高c线对应物种摩尔分数逐渐降低的原因是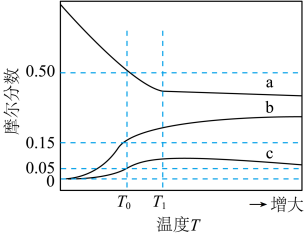
 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应
时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应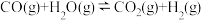 的平衡常数
的平衡常数
 ,则
,则 的物质的量为
的物质的量为 ;若向平衡体系中通入少量
;若向平衡体系中通入少量 ,重新达平衡后,分压
,重新达平衡后,分压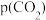 将
将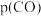 将
将
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】中国科学家首次实现了二氧化碳到淀粉的从头合成,CO2的捕集、利用与封存成为科学家研究的重要课题。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
II.C2H6(g) CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
(1)反应I的反应历程可分为如下两步:
i. C2H6(g) C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)
ii. H2(g)+CO2(g) H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
①∆H1=_______
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是_______ 。
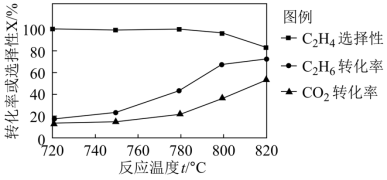
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是_______ 。 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
____ (用含有x的代数式表示);当温度升高时,k正增大m倍,k逆增大n倍,则m_____ n(填“>”、“<”或“=”)。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)II.C2H6(g)
 CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)(1)反应I的反应历程可分为如下两步:
i. C2H6(g)
 C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)ii. H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)①∆H1=
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是
 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示: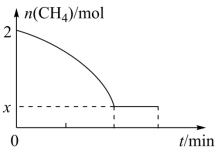

您最近一年使用:0次
【推荐2】氮及其化合物在生产、生活与环境中有着重要研究和应用价值。根据要求回答问题:
(1)CO和NO都是汽车尾气有害物质,它们能缓慢的反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g) △H=-746.5kJ·mol-1。已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ·mol-1,CO的燃烧热△H=_______ kJ·mol-1
(2)N2O4是一种强氧化剂,是重要的火箭推进剂之一。已知反应N2O4(g)⇌2NO2(g) △H>0,v(正)=k(正)·c(N2O4)、v(逆)=k(逆)·c2(NO2)。
①平衡后升高温度k(逆)/k(正)_______ (填“增大”、“不变”或“减小”)
②将一定量N2O4和NO2的混合气体通入体积为1L的恒温密闭容器中,各物质浓度随时间变化关系如图所示。反应从开始进行到10min时v(NO2)=_______ mol/(L·s)
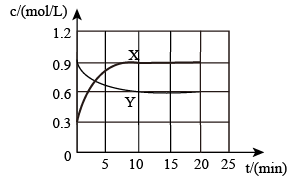
③T℃时,向恒温密闭容器中充入nmolN2O4,维持总压强p0恒定,达平衡时,NO2的平衡分压p(NO2)=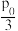 ,则该温度下该反应平衡转化率α(N2O4)=
,则该温度下该反应平衡转化率α(N2O4)=_______ ,保持温度不变,再向密闭容器中充入nmolN2O4,维持总压强为2p0,则在该温度下该反应的压强平衡常数(Kp)=_______ (用各气体物质的分压代替浓度的平衡常数叫压强平衡常数(Kp)。分压=总压×物质的量分数)
(3)氢叠氮酸(HN3)是无色有刺激性气味的液体,可作引爆剂。已知常温下向25.00mL0.1mol·L-1ROH溶液中逐滴滴加0.2mol·L-1的HN3溶液,溶液的pH与所加溶液的体积关系如下表(溶液混合时体积的变化忽略不计)。
①pH=9时溶液中c(N )
)_______ c(R+)(填“>”、“=”或“<”),pH=a时溶液中c(HN3)_______ c(N )(填“大于”“等于”或“小于”)
)(填“大于”“等于”或“小于”)
②HN3的Ka=_______ (精确值)
(4)N2O5是一种新型硝化剂。其制备装置如图所示。
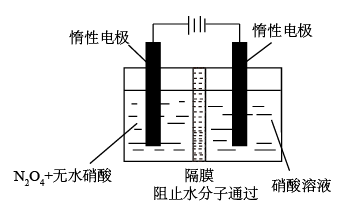
透过隔膜的粒子是_______ ,制取N2O5的电极反应式为_______
(1)CO和NO都是汽车尾气有害物质,它们能缓慢的反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g) △H=-746.5kJ·mol-1。已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ·mol-1,CO的燃烧热△H=
(2)N2O4是一种强氧化剂,是重要的火箭推进剂之一。已知反应N2O4(g)⇌2NO2(g) △H>0,v(正)=k(正)·c(N2O4)、v(逆)=k(逆)·c2(NO2)。
①平衡后升高温度k(逆)/k(正)
②将一定量N2O4和NO2的混合气体通入体积为1L的恒温密闭容器中,各物质浓度随时间变化关系如图所示。反应从开始进行到10min时v(NO2)=

③T℃时,向恒温密闭容器中充入nmolN2O4,维持总压强p0恒定,达平衡时,NO2的平衡分压p(NO2)=
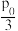 ,则该温度下该反应平衡转化率α(N2O4)=
,则该温度下该反应平衡转化率α(N2O4)=(3)氢叠氮酸(HN3)是无色有刺激性气味的液体,可作引爆剂。已知常温下向25.00mL0.1mol·L-1ROH溶液中逐滴滴加0.2mol·L-1的HN3溶液,溶液的pH与所加溶液的体积关系如下表(溶液混合时体积的变化忽略不计)。
| V(HN3)/mL | 0 | 12.50 | 12.75 | 25.00 |
| pH | 13 | 9 | 7 | a |
 )
) )(填“大于”“等于”或“小于”)
)(填“大于”“等于”或“小于”)②HN3的Ka=
(4)N2O5是一种新型硝化剂。其制备装置如图所示。

透过隔膜的粒子是
您最近一年使用:0次
【推荐3】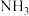 作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。
作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。
(1)催化剂常具有较强的选择性,即专一性。已知:
反应I: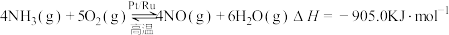
反应 II: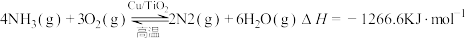
写出NO分解生成 与
与 的热化学方程式
的热化学方程式______ 。
(2)在恒温恒容装置中充入一定量的 和
和 ,在某催化剂的作用下进行反应I,测得不同时间的
,在某催化剂的作用下进行反应I,测得不同时间的 和
和 ,的浓度如表:
,的浓度如表:
则下列有关叙述中正确的是______ 。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 时,说明反应已达平衡
时,说明反应已达平衡
C.当容器内 时,说明反应已达平衡
时,说明反应已达平衡
D.前10分钟内的平均速率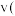

(3)氨催化氧化时会发生上述两个竞争反应I、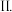 为分析某催化剂对该反应的选择性,在1L密闭容器中充入1mol
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1mol  和2mol
和2mol  ,测得有关物质的量关系如图1:
,测得有关物质的量关系如图1:
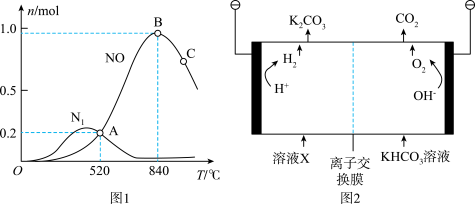
①该催化剂在低温时选择反应______  填“I”或“II”
填“I”或“II” 。
。
② 时,
时, 的平衡常数
的平衡常数
______  不要求得出计算结果,只需列出数字计算式
不要求得出计算结果,只需列出数字计算式 。
。
③ 点比B点所产生的NO的物质的量少的主要原因
点比B点所产生的NO的物质的量少的主要原因______ 。
(4)合成氨工业会产生大量副产物 ,工业上常用高浓度的
,工业上常用高浓度的 溶液吸收
溶液吸收 ,得溶液X,再利用电解法使
,得溶液X,再利用电解法使 溶液再生,其装置如图2所示:
溶液再生,其装置如图2所示:
①在阳极区发生的反应包括______ 和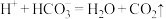 。
。
②简述 在阴极区再生的原理
在阴极区再生的原理______ 。
(5)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的 。
。
已知: 时,
时, ,
,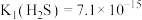 ,
,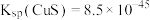
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则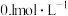 氢硫酸的
氢硫酸的
______  取近似整数
取近似整数 。
。
②已知,某废液接近于中性,若加入适量的氢硫酸,当废液中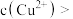
______ 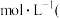 计算结果保留两位有效数字
计算结果保留两位有效数字 ,就会产生CuS沉淀。
,就会产生CuS沉淀。
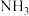 作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。
作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。(1)催化剂常具有较强的选择性,即专一性。已知:
反应I:
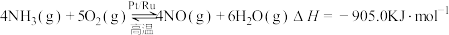
反应 II:
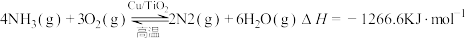
写出NO分解生成
 与
与 的热化学方程式
的热化学方程式(2)在恒温恒容装置中充入一定量的
 和
和 ,在某催化剂的作用下进行反应I,测得不同时间的
,在某催化剂的作用下进行反应I,测得不同时间的 和
和 ,的浓度如表:
,的浓度如表:时间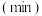 | 0 | 5 | 10 | 15 | 20 | 25 |
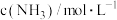 |  | 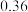 | 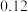 |  | 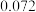 | 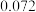 |
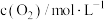 |  | 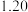 | 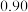 |  | 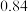 | 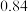 |
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内
 时,说明反应已达平衡
时,说明反应已达平衡C.当容器内
 时,说明反应已达平衡
时,说明反应已达平衡D.前10分钟内的平均速率
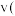

(3)氨催化氧化时会发生上述两个竞争反应I、
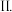 为分析某催化剂对该反应的选择性,在1L密闭容器中充入1mol
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1mol  和2mol
和2mol  ,测得有关物质的量关系如图1:
,测得有关物质的量关系如图1:
①该催化剂在低温时选择反应
 填“I”或“II”
填“I”或“II” 。
。②
 时,
时, 的平衡常数
的平衡常数
 不要求得出计算结果,只需列出数字计算式
不要求得出计算结果,只需列出数字计算式 。
。③
 点比B点所产生的NO的物质的量少的主要原因
点比B点所产生的NO的物质的量少的主要原因(4)合成氨工业会产生大量副产物
 ,工业上常用高浓度的
,工业上常用高浓度的 溶液吸收
溶液吸收 ,得溶液X,再利用电解法使
,得溶液X,再利用电解法使 溶液再生,其装置如图2所示:
溶液再生,其装置如图2所示:①在阳极区发生的反应包括
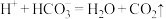 。
。②简述
 在阴极区再生的原理
在阴极区再生的原理(5)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的
 。
。已知:
 时,
时, ,
,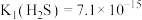 ,
,
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则
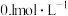 氢硫酸的
氢硫酸的
 取近似整数
取近似整数 。
。②已知,某废液接近于中性,若加入适量的氢硫酸,当废液中
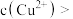
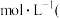 计算结果保留两位有效数字
计算结果保留两位有效数字 ,就会产生CuS沉淀。
,就会产生CuS沉淀。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:
(1)画出B的离子结构示意图______ ;写出D元素最高价氧化物的水化物电子式_________
(2)盐X水溶液显____ (填“酸”“碱”“中”)性,用离子方程式解释其原因________________
(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为________
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同。Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。该燃料电池放电时,正极的电极反应式是________________________________
(5)如右图是一个电解过程示意图。
假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)_______________ L
| 元素 | 有关信息 |
| A | 元素主要化合价为—2,原子半径为0.074 n m |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102 n m,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物的水化物,能按1∶1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075 n m,最高价氧化物的水化物与其氢化物组成一种盐X |
(2)盐X水溶液显
(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同。Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。该燃料电池放电时,正极的电极反应式是
(5)如右图是一个电解过程示意图。

假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
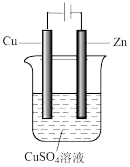
(1)下图转化途径中属于“固氮”的是______。
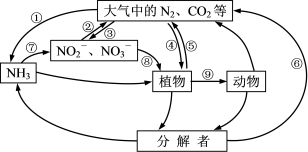
(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中ad表示物质吸附在催化剂表面时的状态)
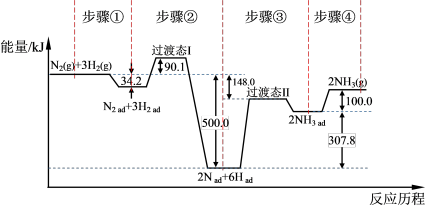
①由图可知合成氨反应N2(g)+3H2(g) 2NH3(g)的ΔH=
2NH3(g)的ΔH=______ kJ·mol-1,对总反应速率影响较大的是步骤______ 。(填写编号)
②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是______ 。(双选)
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
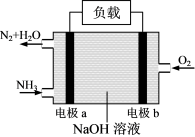
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用NH3的燃烧反应(4NH3+3O2 2N2+6H2O)能设计成燃料电池,其工作原理如图所示。电极b为
2N2+6H2O)能设计成燃料电池,其工作原理如图所示。电极b为______ (选填“正”或“负”)极;电极a的电极反应式为______ ;当正负极共消耗3.136L(标准状况)气体时,通过负载的电子数为______ 个。
(1)下图转化途径中属于“固氮”的是______。
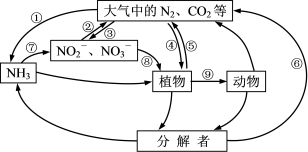
| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |

①由图可知合成氨反应N2(g)+3H2(g)
 2NH3(g)的ΔH=
2NH3(g)的ΔH=②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用NH3的燃烧反应(4NH3+3O2
 2N2+6H2O)能设计成燃料电池,其工作原理如图所示。电极b为
2N2+6H2O)能设计成燃料电池,其工作原理如图所示。电极b为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】工业上常以黄铜矿(主要成分是CuFeS2)为原料制备铜以及副产物铁红(Fe2O3),其工艺流程如下:
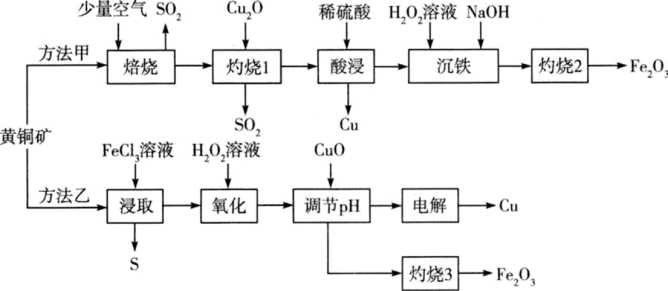
已知“焙烧”时发生反应的化学方程式为

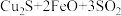 。
。
回答下列问题:
(1)方法甲中为了加快“焙烧”速率,可以采取的措施有___________ (任写两点);“焙烧”时发生的反应中起氧化作用的物质是___________ 。
(2)方法甲中“灼烧1”时Cu2S发生反应的化学方程式为___________ 。
(3)方法甲中“沉铁”时,要使溶液中的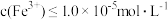 ,则需要调节溶液的pH最小值为
,则需要调节溶液的pH最小值为 ____________ {已知 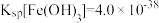 ,
,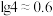 }。
}。
(4)方法乙中“氧化”时加入H2O2溶液发生反应的离子方程式为____________ ;加入CuO调节溶液pH的目的是 ____________ 。
(5)方法甲中得到的粗铜必须电解精炼才能制得纯铜,工艺上一般利用如图装置对粗铜进行电解精炼。
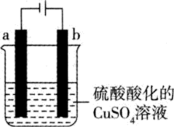
电解精炼时,b极材料是___________ (填“粗铜”或“纯铜”),电池工作时 移向
移向___________ (填“a”或“b”)极区。若电解前两电极质量相等,工作一段时间后测得溶液增重m g(假设阳极只有锌溶解),则电路中转移电子的数目为___________ 。

已知“焙烧”时发生反应的化学方程式为


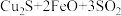 。
。回答下列问题:
(1)方法甲中为了加快“焙烧”速率,可以采取的措施有
(2)方法甲中“灼烧1”时Cu2S发生反应的化学方程式为
(3)方法甲中“沉铁”时,要使溶液中的
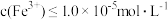 ,则需要调节溶液的pH最小值为
,则需要调节溶液的pH最小值为 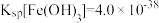 ,
,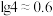 }。
}。(4)方法乙中“氧化”时加入H2O2溶液发生反应的离子方程式为
(5)方法甲中得到的粗铜必须电解精炼才能制得纯铜,工艺上一般利用如图装置对粗铜进行电解精炼。

电解精炼时,b极材料是
 移向
移向
您最近一年使用:0次



