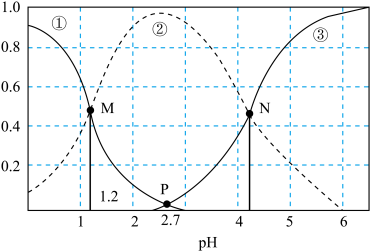
草酸H2C2O4是一种二元弱酸。向草酸溶液中加NaOH,H2C2O4、HC2O 和C2O
和C2O 的分布系数δ与溶液pH的变化关系如图所示。[比如C2O
的分布系数δ与溶液pH的变化关系如图所示。[比如C2O 的分布系数:δ(C2O
的分布系数:δ(C2O )=
)= ],下列说法不正确的是
],下列说法不正确的是
 和C2O
和C2O 的分布系数δ与溶液pH的变化关系如图所示。[比如C2O
的分布系数δ与溶液pH的变化关系如图所示。[比如C2O 的分布系数:δ(C2O
的分布系数:δ(C2O )=
)= ],下列说法不正确的是
],下列说法不正确的是
A.曲线②代表HC2O | B.N点的横坐标为4.2 |
| C.水的电离程度:N<P<M | D.N点:c(Na+)<3c(C2O ) ) |
2023·安徽宣城·一模 查看更多[3]
安徽省宣城市2023届高三上学期一模暨期末考试理科综合化学试题(已下线)第15练 水溶液中的离子平衡图像分析 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)重庆市第一中学校2023-2024学年高三上学期开学考试化学试题
更新时间:2023-05-04 08:42:58
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在某温度时,将n mol∙L-1氨水滴入10 mL 1.0 mol∙L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是
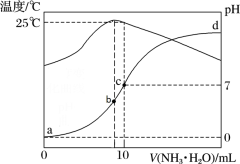

| A.a点Kw = 1.0×10-14 |
| B.b点:c(NH3∙H2O) + c(OH-) < c(H+) |
| C.25℃时,NH4Cl水解平衡常数为(n-1)×10-7(用n表示) |
| D.d点水的电离程度最大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】乙二胺(H2NCH2CH2NH2)是二元弱碱,H2A是二元弱酸。下图既可表示常温下乙二胺溶液中含氮微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线,又可表示常温下H2A溶液中H2A、HA-、A2-微粒的百分含量δ随溶液pH的变化曲线。
已知:H2NCH2CH2NH2+H2O⇌[H2NCH2CH2NH3]++OH-

下列说法正确的是
已知:H2NCH2CH2NH2+H2O⇌[H2NCH2CH2NH3]++OH-

下列说法正确的是
| A.曲线c表示H2NCH2CH2NH2或H2A的百分含量δ随溶液pH的变化情况 |
B.乙二胺的 |
| C.一定浓度的[H3NCH2CH2NH3]Cl2溶液中存在关系式:2c([H2NCH2CH2NH2])+c([H3NCH2CH2NH2]+)=c(H+)-c(OH-) |
| D.[H3NCH2CH2NH2][HA]溶液中各离子浓度大小关系为:c([H3NCH2CH2NH2]+)=c(HA-)>c(H2NCH2CH2NH2)=c(A2-)>c(H+)=c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】相同温度和压强下,研究Cl2分别在不同浓度的盐酸和NaCl溶液中的溶解度(用溶解Cl2的物质的量浓度表示)变化如图所示。

已知氯气溶解存在以下过程:
①Cl2(aq)+H2O(l) H+(aq)+Cl-(aq)+HClO(aq) K1=4.2×10-4
H+(aq)+Cl-(aq)+HClO(aq) K1=4.2×10-4
②Cl2(aq)+C1-(aq) Cl
Cl (aq) K2=0.19
(aq) K2=0.19
③HClO(aq) H+(aq)+ClO-(aq) Ka=3.2×10-8
H+(aq)+ClO-(aq) Ka=3.2×10-8
下列说法错误的是

已知氯气溶解存在以下过程:
①Cl2(aq)+H2O(l)
 H+(aq)+Cl-(aq)+HClO(aq) K1=4.2×10-4
H+(aq)+Cl-(aq)+HClO(aq) K1=4.2×10-4②Cl2(aq)+C1-(aq)
 Cl
Cl (aq) K2=0.19
(aq) K2=0.19③HClO(aq)
 H+(aq)+ClO-(aq) Ka=3.2×10-8
H+(aq)+ClO-(aq) Ka=3.2×10-8下列说法错误的是
A.随着NaCl浓度的增大,Cl2溶解度减小,溶液中 减小 减小 |
| B.随着盐酸浓度的增大,反应①被抑制,反应②为主要反应从而促进Cl2溶解 |
C.a点时,c(H+)>c(Cl-)>c(Cl )>c(ClO-) )>c(ClO-) |
D.b点时,c(HClO)+c(ClO-)+c(Na+)=c(Cl-)+c(Cl ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,向体积均为V0、浓度均为0.10 mol·L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随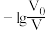 的变化如图所示,
的变化如图所示,
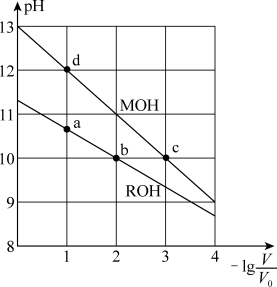
下列叙述正确的是
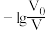 的变化如图所示,
的变化如图所示,
下列叙述正确的是
A.b、c两点的溶液中: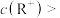 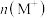 |
| B.MOH的电离程度:c点小于d点 |
| C.溶液中水的的电离程度:b>c>a>d |
D.当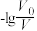 =2时,若两溶液同时升高温度,则 =2时,若两溶液同时升高温度,则 增大 增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】在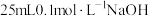 溶液中逐滴加入
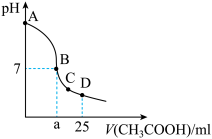
溶液中逐滴加入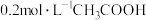 溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
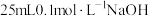 溶液中逐滴加入
溶液中逐滴加入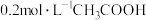 溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是 
A.在曲线的A、B间,溶液中可能有 |
B.在B点,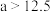 ,且有 ,且有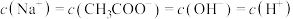 |
C.在C点, |
D.在D点,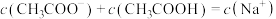 |
您最近一年使用:0次

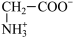 、
、 和
和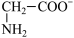 三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是(
三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是(
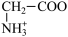 +H2O
+H2O


