已知:室温下氢硫酸 的电离常数
的电离常数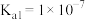 ,
,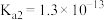 ;
; 和
和 的
的 分别为
分别为 、
、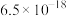 ,下列说法不正确的是
,下列说法不正确的是
 的电离常数
的电离常数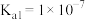 ,
,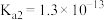 ;
; 和
和 的
的 分别为
分别为 、
、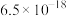 ,下列说法不正确的是
,下列说法不正确的是A.反应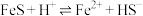 的平衡常数 的平衡常数 的数值为 的数值为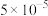 |
B.可以用 除去污水中的 除去污水中的 |
C.从上述数据可得出 难溶于稀硫酸中 难溶于稀硫酸中 |
D. 的 的 溶液中加入等体积 溶液中加入等体积 的 的 溶液,则有: 溶液,则有: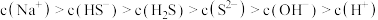 |
更新时间:2023-05-06 19:05:25
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定条件下,在0.5 L的密闭容器中进行反应:Cl2(g)+CO(g) COCl2(g),反应过程中的有关数据见表:
COCl2(g),反应过程中的有关数据见表:
下列说法正确的是
 COCl2(g),反应过程中的有关数据见表:
COCl2(g),反应过程中的有关数据见表:| 时间 | n(Cl2)/mol | n(CO)/mol | n(COCl2)/mol |
| 0 | 1.2 | 1 | 0 |
| 2 | 0.8 | ||
| 6 | 0.1 | ||
| 8 | 0.3 |
| A.反应在前2 min内,用CO表示的化学反应速率为0.4 molL1s1 |
| B.该温度下,该反应的平衡常数为30 |
| C.保持其他条件不变,升高温度,平衡时c(COCl2)=1.5mol·L-1,则反应的ΔH<0 |
| D.若保持其他条件不变,在第8 min再充入1.2 mol Cl2和1.0 mol CO气体,达到新平衡时COCl2的体积分数小于原平衡COCl2的体积分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】恒温T ℃、恒压101kPa,将足量的CuSO4·5H2O、NaHCO3置于一个密闭容器中,再充入已除去CO2的干燥空气。仅发生以下反应,达平衡时两者分解的物质的量比为2:1。
CuSO4·5H2O(s) CuSO4·3H2O(s)+2H2O(g) Kp1=81 kPa2
CuSO4·3H2O(s)+2H2O(g) Kp1=81 kPa2
2NaHCO3(s) Na2CO3(s)+H2O(g)+CO2(g) Kp2
Na2CO3(s)+H2O(g)+CO2(g) Kp2
第一次平衡后,用总压为101 kPa的潮湿空气[其中p(H2O)=8 kPa、p(CO2)=4 kPa]替换容器中的气体,T ℃下达到第二次平衡。
下列说法不正确的是
CuSO4·5H2O(s)
 CuSO4·3H2O(s)+2H2O(g) Kp1=81 kPa2
CuSO4·3H2O(s)+2H2O(g) Kp1=81 kPa22NaHCO3(s)
 Na2CO3(s)+H2O(g)+CO2(g) Kp2
Na2CO3(s)+H2O(g)+CO2(g) Kp2第一次平衡后,用总压为101 kPa的潮湿空气[其中p(H2O)=8 kPa、p(CO2)=4 kPa]替换容器中的气体,T ℃下达到第二次平衡。
下列说法不正确的是
A.第一次平衡时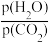 =9 =9 | B.Kp2=9 kPa2 |
| C.第二次平衡建立的过程中CuSO4·5H2O的质量将减少 | D.第二次平衡建立的过程中NaHCO3的质量将减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在不同温度下,向V L密闭容器中加入0.5mol NO和0.5mol活性炭,发生反应:2NO(g)+C(s)  N2(g)+CO2(g) ΔH=-Q kJ·mol-1(Q>0),达到平衡时的数据如下表:
N2(g)+CO2(g) ΔH=-Q kJ·mol-1(Q>0),达到平衡时的数据如下表:
下列有关说法正确的是( )
 N2(g)+CO2(g) ΔH=-Q kJ·mol-1(Q>0),达到平衡时的数据如下表:
N2(g)+CO2(g) ΔH=-Q kJ·mol-1(Q>0),达到平衡时的数据如下表:| 温度/℃ | n(C)/mol | n(CO2)/mol |
| T1 | 0.15 | |
| T2 | 0.375 |
| A.由上述信息可推知:T1>T2 |
| B.T2℃条件下,若反应达到平衡后再缩小容器的体积,c(N2):c(NO)增大 |
| C.T1℃条件下,若开始时反应物的用量均减小一半, 平衡后NO的转化率增大 |
D. ℃条件下,该反应的平衡常数 ℃条件下,该反应的平衡常数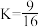 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列各溶液的叙述中正确的是
| A.NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-) |
| B.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(CH3COOH) >c(Cl-)>c(H+) |
| C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D.向1.00 L 0.3 mol/LNaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下,乙二胺( )第一步电离方程式为:
)第一步电离方程式为: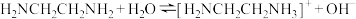 ,乙二胺的电离平衡常数为:
,乙二胺的电离平衡常数为: ,
, ,向20 mL乙二胺溶液中加入同浓度的盐酸,借用计算机技术得到滴定曲线如图所示,下列说法正确的是
,向20 mL乙二胺溶液中加入同浓度的盐酸,借用计算机技术得到滴定曲线如图所示,下列说法正确的是

 )第一步电离方程式为:
)第一步电离方程式为: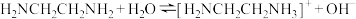 ,乙二胺的电离平衡常数为:
,乙二胺的电离平衡常数为: ,
, ,向20 mL乙二胺溶液中加入同浓度的盐酸,借用计算机技术得到滴定曲线如图所示,下列说法正确的是
,向20 mL乙二胺溶液中加入同浓度的盐酸,借用计算机技术得到滴定曲线如图所示,下列说法正确的是
| A.图中四点,c点水的电离程度最大 |
| B.可用酚酞作指示剂 |
| C.c点对应的横坐标数值为20 |
D.d点: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关离子方程式书写或离子共存说法正确的是
| A.在0.1mol/LNa2CO3溶液中:Al3+、NH4+、SO42-、NO3-一定能大量共存 |
B.常温下, =0.1mol/L的溶液中,下列离子一定能大量共存:K+、Cl-、Fe2+、NO3- =0.1mol/L的溶液中,下列离子一定能大量共存:K+、Cl-、Fe2+、NO3- |
| C.清洗锅炉时先用纯碱溶液浸泡的主要原因:CaSO4(s)+CO32-(aq)⇌SO42-(aq)+CaCO3(s) |
| D.向Al2(SO4)3溶液中加入少量Ba(OH)2溶液:Ba2++SO42-+Al3++3OH-=BaSO4↓+Al(OH)3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作和现象及所得到的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向蛋白质溶液中滴加过量的氯化铵,有固体析出 | 蛋白质变性 |
| B | 向NaI和NaCl混合液中加入大量AgNO3溶液,出现了黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向蔗糖溶液中加入稀H2SO4,加热几分钟,冷却后加入新制Cu(OH)2,加热后没有红色沉淀生成 | 蔗糖还未水解 |
| D | 用pH测得:0.1mol/LCH3COOH溶液的pH约为3 | 发生电离CH3COOH分子约为1% |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验中,通过对应的现象分析,能得出正确结论是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2已变质 |
| B | 在0.1mol/LNa2S溶液中滴加少量等浓度的ZnSO4溶液,再加入少量等浓度的CuSO4溶液 | 先产生白色沉淀,后产生黑色沉淀 | Ksp(ZnS)>Ksp(CuS) |
| C | 向NaHCO3溶液中通入足量的SO2,将气体通入品红溶液后再通入澄清石灰水 | 澄清石灰水变浑浊 | 酸性:H2SO3>H2CO3 |
| D | 分别向等物质的量浓度、等体积的KCl和KI的溶液,滴加2滴稀的Ag(NH3)2]OH溶液,充分振荡后 | KCl溶液中无白色沉淀,KI溶液中有黄色沉淀 | Ag+结合微粒的能力:I->NH3>Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】下列叙述中正确的是
A.向饱和的AgCl、AgBr混合液中加入少量AgNO3,溶液中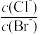 不变 不变 |
| B.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| C.在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu |
D.反应2A(g)+B(s)=C(g)+D(s)在一定条件下可自发进行,则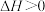 |
您最近一年使用:0次
【推荐2】已知: 、
、 在水溶液中的溶解平衡分别为
在水溶液中的溶解平衡分别为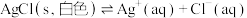 、
、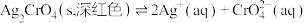 。常温下,分别向
。常温下,分别向 等浓度的
等浓度的 溶液和
溶液和 溶液中滴加等浓度的
溶液中滴加等浓度的 溶液,所加硝酸银溶液的体积与阴离子的浓度关系如图所示。下列说法错误的是
溶液,所加硝酸银溶液的体积与阴离子的浓度关系如图所示。下列说法错误的是
 、
、 在水溶液中的溶解平衡分别为
在水溶液中的溶解平衡分别为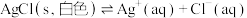 、
、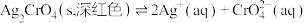 。常温下,分别向
。常温下,分别向 等浓度的
等浓度的 溶液和
溶液和 溶液中滴加等浓度的
溶液中滴加等浓度的 溶液,所加硝酸银溶液的体积与阴离子的浓度关系如图所示。下列说法错误的是
溶液,所加硝酸银溶液的体积与阴离子的浓度关系如图所示。下列说法错误的是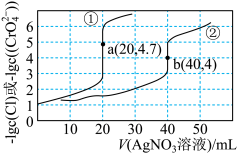
A.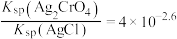 |
B. 与 与 溶液反应对应曲线② 溶液反应对应曲线② |
C. 可作为 可作为 溶液标定 溶液标定 溶液浓度的指示剂 溶液浓度的指示剂 |
D.欲使图中a点或b点向左平移可增大 溶液的浓度 溶液的浓度 |
您最近一年使用:0次




