25℃时,二元弱酸H2A的 ,
, ,下列说法正确的是
,下列说法正确的是
 ,
, ,下列说法正确的是
,下列说法正确的是A. 溶液中 溶液中 |
B.将等浓度的 溶液和硫酸溶液稀释10倍,前者pH较小 溶液和硫酸溶液稀释10倍,前者pH较小 |
C. 的化学平衡常数 的化学平衡常数 |
D.向 溶液滴加 溶液滴加 溶液至中性时 溶液至中性时 |
更新时间:2023-05-11 07:48:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】H2A为二元弱酸,其电离过程: ,
, 。常温时,向
。常温时,向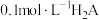 水溶液中逐滴滴加等浓度的
水溶液中逐滴滴加等浓度的 溶液,混合溶液中
溶液,混合溶液中 、
、 和
和 的物质的量分数
的物质的量分数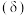 随
随 变化的关系如图所示。下列叙述正确的是
变化的关系如图所示。下列叙述正确的是

 ,
, 。常温时,向
。常温时,向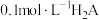 水溶液中逐滴滴加等浓度的
水溶液中逐滴滴加等浓度的 溶液,混合溶液中
溶液,混合溶液中 、
、 和
和 的物质的量分数
的物质的量分数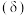 随
随 变化的关系如图所示。下列叙述正确的是
变化的关系如图所示。下列叙述正确的是
A.曲线Ⅱ表示 |
B.常温下 的 的 |
C.当 时,溶液中 时,溶液中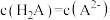 |
D.向 的溶液中持续滴加 的溶液中持续滴加 溶液,水的电离程度先增大后减小 溶液,水的电离程度先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
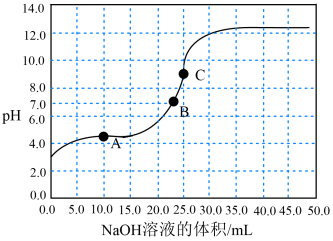
【推荐2】以酚酞为指示剂,用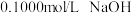 溶液滴定
溶液滴定 未知浓度的
未知浓度的 溶液,滴定过程中的
溶液,滴定过程中的 变化如下图所示。下列分析正确的是
变化如下图所示。下列分析正确的是

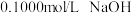 溶液滴定
溶液滴定 未知浓度的
未知浓度的 溶液,滴定过程中的
溶液,滴定过程中的 变化如下图所示。下列分析正确的是
变化如下图所示。下列分析正确的是
A. 的浓度为 的浓度为 |
B. 的电离常数 的电离常数 |
| C.溶液从粉红色变为无色,且半分钟内不变色,表示已达滴定终点 |
D. 时,溶液中 时,溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,下列有关电解质溶液的说法不正确的是( )
| A.pH=9.25、浓度均为0.1mol/L的NH4Cl、NH3∙H2O的混合溶液: c(NH4+)+c(H+)>c(NH3∙H2O)+c(OH-) |
| B.0.1mol/L硫酸溶液与0.1mol/LNaOH溶液等体积混合后的溶液:c(H+)=c(OH-)+c(SO42-) |
| C.向0.1mol/L NaHSO3溶液中通入NH3至pH=7的溶液:c(Na+)>c(SO32-)>c(NH4+) |
| D.CO2通入KOH溶液,当由水电离的c(H+)=10-7mol/L,一定存在:c(K+)=2c(CO32-)+c(HCO3-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知下表为25℃时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是
| CH3COOH | HClO | H2CO3 |
| Ka= 1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A.向NaClO溶液中通入少量二氧化碳的离子方程式为: 2ClO-+CO2+H2O=2HClO+CO32- |
| B.相同浓度 的 CH3COONa 和 NaClO 的混合溶液中,c(CH3OOH)+c(HClO) =c(OH-)-c(H+) |
| C.向0.1mol/LCH3COONa溶液中加入少量水,溶液pH增大 |
| D.25℃时,0.10mol/LNa2CO3溶液通入CO2至溶液的pH=7时,溶液中:c(Na+)=c(CO32-)+ c(HCO3-)+c(H2CO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知常温下浓度为0.1mol/L的下列溶液的pH如下表所示:
下列有关说法正确的是
| 溶质 | NaF | NaClO |  |  |
| pH | 7.5 | 9.7 | 8.3 | 11.6 |
A.将少量的 通入到NaClO溶液中离子方程式为: 通入到NaClO溶液中离子方程式为: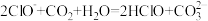 |
B.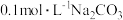 溶液中,存在关系: 溶液中,存在关系: |
C.根据上表数掉得出三种酸电离平衡常数大小关系为 (第一级电离平衡常数) (第一级电离平衡常数) |
D. 的HF溶液与 的HF溶液与 的NaOH溶液以体积1:1混合,则有 的NaOH溶液以体积1:1混合,则有 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知磷酸二氢钾( )可用作高磷钾复合肥料,工业上可通过
)可用作高磷钾复合肥料,工业上可通过 制备。已知25℃时,
制备。已知25℃时, 、
、 、
、 。下列关于0.1
。下列关于0.1
 溶液的说法正确的是
溶液的说法正确的是
 )可用作高磷钾复合肥料,工业上可通过
)可用作高磷钾复合肥料,工业上可通过 制备。已知25℃时,
制备。已知25℃时, 、
、 、
、 。下列关于0.1
。下列关于0.1
 溶液的说法正确的是
溶液的说法正确的是A.该溶液中 |
B.该溶液中 |
C.向该溶液中滴加少量NaOH溶液,其离子方程式为 |
D.25℃, 的化学平衡常数为 的化学平衡常数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用烟道气中SO2的生产NaHSO3晶体的工艺流程如下所示。下列说法正确的是


A.步骤I可得NaHSO3溶液中有c(OH-)=c(H+)+c(SO )+c(H2SO3) )+c(H2SO3) |
| B.步骤Ⅲ所得溶液中有Ka1(H2SO3)·Ka2(H2SO3)<Kw |
C.步骤Ⅱ中发生的反应为HSO +CO +CO =SO =SO +HCO +HCO ,则H2SO3的Ka2大于H2CO3的Ka2 ,则H2SO3的Ka2大于H2CO3的Ka2 |
| D.向Na2CO3饱和溶液中通入SO2的过程,水的电离程度先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】25℃时,将浓度均为0.1 mol/L的HA溶液与BOH溶液按不同体积比混合,以Va和Vb、分别代表酸和碱的体积,保持Va+Vb=100 mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是


| A.c点时,c(A-)>c(B+) |
| B.Ka(HA)=Kb(BOH)=1×10-6 |
C.a→c过程中 不变 不变 |
| D.b点时,c(A-)=c(B+)=c(H+)=c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,某实验人员在两个相同的容器中分别加入20 mL 0.2 mol⋅L-1  溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知
溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知 溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
 溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知
溶液和40 mL 0.1 mol⋅L-1 NaHA溶液,再分别用0.2 mol⋅L-1盐酸滴定,利用pH计和压力传感器检测,绘制曲线如图所示。(已知 溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)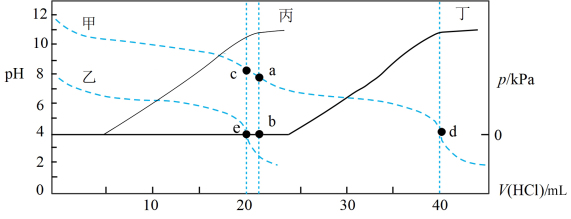
| A.图中曲线乙和丙代表向NaHA溶液中滴加盐酸 |
B.由图可知,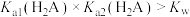 |
C.a点溶液中存在: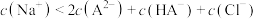 |
| D.根据pH-V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图为某实验测得0.1mol·L-1NaHCO3溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正确的是
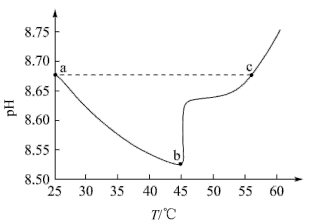

A.ab段,pH减小说明升温抑制了HCO 的水解 的水解 |
| B.a点时,KW<Ka1(H2CO3)∙Ka2(H2CO3) |
C.b点溶液中,c(Na+)>c(HCO )+2c(CO )+2c(CO ) ) |
| D.a点溶液的c(OH-)比c点溶液的大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,Ka(HCOOH)=1.77×10-4,Ka(CH3COOH)=1.75×10-5,Kb(NH3·H2O)=1.76×10-5,下列说法正确的是( )
A.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
| B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 |
| C.0.2 mol/L HCOOH 与 0.1 mol/L NaOH 等体积混合后:c(HCOO-) + c(OH-)=c(HCOOH) + c(H+) |
| D.0.2 mol/L CH3COONa 与 0.1 mol/L盐酸等体积混合后 (pH<7):c(CH3COO-)>c(Cl- )>c(CH3COOH)>c(H+) |
您最近一年使用:0次